名校
1 . 镁及其合金是用途很广的金属材料,可以通过以下步骤从海水中提取镁。下列说法不正确 的是
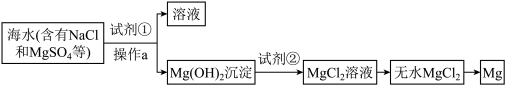
| A.试剂①常用石灰乳 |
| B.操作a是过滤 |
C.试剂②是盐酸,加入后发生反应: |
D.工业上常用加热无水 获得金属镁 获得金属镁 |
您最近一年使用:0次
2023-07-11更新
|
224次组卷
|
5卷引用:北京市西城区2022-2023学年高一下学期期末测试化学试题
北京市西城区2022-2023学年高一下学期期末测试化学试题北京市第三十五中学2023-2024学年高一下学期(选考)期中测试化学试题北京市回民学校2023-2024学年高一下学期期中考试化学试题(已下线)高一化学期末押题卷01(“25+5”模式)-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(北京专用)(已下线)专题06 化学与可持续发展-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(北京专用)
名校
解题方法
2 . 铜和三氧化二铁在工农业生产中用途广泛,用黄铜矿(主要成分为CuFeS2,其中Cu为+2价、Fe为+2价)制取铜和三氧化二铁的工艺流程如图所示:
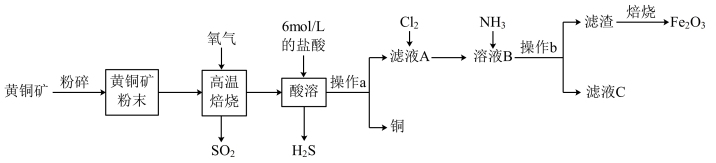
(1)将黄铜矿粉碎的目的是____ 。
(2)高温熔烧时发生的反应是CuFeS2+O2 SO2+FeS+Cu、1molO2参加反应时,反应中转移电子
SO2+FeS+Cu、1molO2参加反应时,反应中转移电子____ mol。
(3)操作a为____ 。
(4)向滤液A中通入Cl2的目的是____ 。
(5)向溶液B中通入NH3后发生反应的离子方程式为____ 。
(6)工业上用生物法处理H2S的原理为(硫杆菌作催化剂):
H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4=2Fe2(SO4)3+2H2O
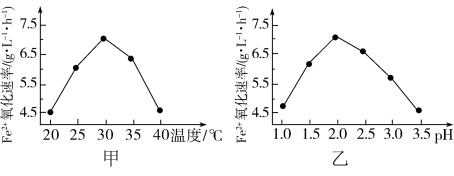
由图甲和图乙判断使用硫杆菌的最佳条件为___ ,若反应温度过高,反应速率下降,其原因是___ 。

(1)将黄铜矿粉碎的目的是
(2)高温熔烧时发生的反应是CuFeS2+O2
 SO2+FeS+Cu、1molO2参加反应时,反应中转移电子
SO2+FeS+Cu、1molO2参加反应时,反应中转移电子(3)操作a为
(4)向滤液A中通入Cl2的目的是
(5)向溶液B中通入NH3后发生反应的离子方程式为
(6)工业上用生物法处理H2S的原理为(硫杆菌作催化剂):
H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4=2Fe2(SO4)3+2H2O
由图甲和图乙判断使用硫杆菌的最佳条件为

您最近一年使用:0次
2022-06-16更新
|
1326次组卷
|
5卷引用:北京市第一七一中学2021-2022学年高一下学期6月月考化学试题
北京市第一七一中学2021-2022学年高一下学期6月月考化学试题河南省项城市第三高级中学2021-2022学年高二下学期期末考试化学试题(已下线)模拟卷02-2023年高三化学对接新高考全真模拟试卷(云南,安徽,黑龙江,山西,吉林五省通用)(已下线)模拟卷06-2023年高三化学对接新高考全真模拟试卷(云南,安徽,黑龙江,山西,吉林五省通用)(已下线)模拟卷05-2023年高三化学对接新高考全真模拟试卷(云南,安徽,黑龙江,山西,吉林五省通用)
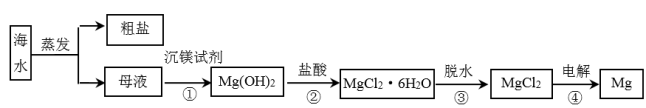
3 . 镁及其合金是一种用途很广的金属材料,目前世界上生产的镁有60%来自海水。一种从海水的母液中提取金属镁的工艺流程如下:_______ 。
a.氢氧化钙 b.氨水 c.氢氧化铜
(2)加入沉镁试剂后,能够分离得到Mg(OH)2沉淀的方法是_______ 。
(3)步骤②发生的化学反应方程式是_______ 。
(4)某海水中镁的含量为1.2g·L-1,则1L海水理论上可制得MgCl2的质量是_______ g。
a.氢氧化钙 b.氨水 c.氢氧化铜
(2)加入沉镁试剂后,能够分离得到Mg(OH)2沉淀的方法是
(3)步骤②发生的化学反应方程式是
(4)某海水中镁的含量为1.2g·L-1,则1L海水理论上可制得MgCl2的质量是
您最近一年使用:0次



