解题方法
1 . 早在战国时期,《周礼·考工记》就记载了我国劳动人民制取氢氧化钾以漂洗丝帛的工艺。大意是:先将干燥的木头烧成灰(含 ),用其灰汁浸泡丝帛,再加入石灰即可。其反应过程如图。
),用其灰汁浸泡丝帛,再加入石灰即可。其反应过程如图。

(1)操作a要用到的玻璃仪器有烧杯、玻璃棒和________ 。
(2)反应过程中未涉及的基本反应类型是________ 。
(3)反应过程中能够循环利用的物质是________ (填化学式)。
(4)氢氧化钙与灰汁(含 )反应的化学方程式为
)反应的化学方程式为________ 。
(5)古人不提前制备大量氢氧化钾的原因是________ (用化学方程式表达)。
 ),用其灰汁浸泡丝帛,再加入石灰即可。其反应过程如图。
),用其灰汁浸泡丝帛,再加入石灰即可。其反应过程如图。
(1)操作a要用到的玻璃仪器有烧杯、玻璃棒和
(2)反应过程中未涉及的基本反应类型是
(3)反应过程中能够循环利用的物质是
(4)氢氧化钙与灰汁(含
 )反应的化学方程式为
)反应的化学方程式为(5)古人不提前制备大量氢氧化钾的原因是
您最近半年使用:0次
名校
解题方法
2 . 水是生命之源。
(1)自然界中的天然水通常含有许多杂质。要除去水中的不溶性杂质,可以进行___________ 操作,该操作使用的玻璃仪器有烧杯、玻璃棒和___________ 其中玻璃棒的作用是___________ ;要吸附掉一些有色有味的可溶性杂质,可以用___________ 净水。
(2)工业上和科学实验中软化硬水的方法很多,生活中通过___________ 也可以降低水的硬度。
(3)“天宫课堂”直播中宇航员告诉我们天宫中所用的氧气来自于电解水。
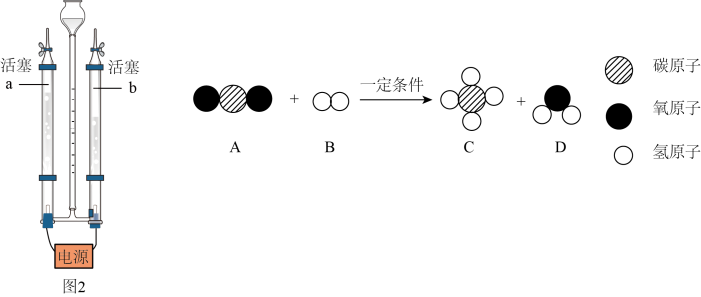
①联系到化学课上的电解水实验,如图2所示:产生 的玻璃管是
的玻璃管是___________ (填“a”或“b”),该反应的基本反应类型为___________ 。
②生成的 还可以与人呼出的
还可以与人呼出的 在一定条件下进行反应,实现了舱内物质循环利用,反应的微观过程如图所示。该反应中涉及到的氧化物有
在一定条件下进行反应,实现了舱内物质循环利用,反应的微观过程如图所示。该反应中涉及到的氧化物有___________ 种,写出C物质的化学式___________ 。
(4)爱护水资源是每个公民应尽的义务,请你写出一个防止水体污染的做法:___________ 。
(1)自然界中的天然水通常含有许多杂质。要除去水中的不溶性杂质,可以进行
(2)工业上和科学实验中软化硬水的方法很多,生活中通过
(3)“天宫课堂”直播中宇航员告诉我们天宫中所用的氧气来自于电解水。

①联系到化学课上的电解水实验,如图2所示:产生
 的玻璃管是
的玻璃管是②生成的
 还可以与人呼出的
还可以与人呼出的 在一定条件下进行反应,实现了舱内物质循环利用,反应的微观过程如图所示。该反应中涉及到的氧化物有
在一定条件下进行反应,实现了舱内物质循环利用,反应的微观过程如图所示。该反应中涉及到的氧化物有(4)爱护水资源是每个公民应尽的义务,请你写出一个防止水体污染的做法:
您最近半年使用:0次
名校
3 . 下图是初中化学实验的几种常用仪器,请按要求填空。
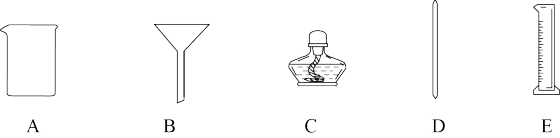
(1)①仪器C的名称叫_______ 。
②在读取E中液体体积时,视线应与凹液面的最低处_______ 。
(2)①进行过滤操作,除铁架台、A和D外,还需要用到上述仪器中的_______ (填字母)。
②配制一定质量分数的NaCl溶液,还必须补充的一种仪器是_______ 。

(1)①仪器C的名称叫
②在读取E中液体体积时,视线应与凹液面的最低处
(2)①进行过滤操作,除铁架台、A和D外,还需要用到上述仪器中的
②配制一定质量分数的NaCl溶液,还必须补充的一种仪器是
您最近半年使用:0次
2022-09-07更新
|
67次组卷
|
2卷引用:山东省临沂市重点中学2022-2023学年高一上学期9月入学考试化学试题
4 . 用于分离或提纯物质的方法有:A.蒸馏(分馏) B.萃取C.过滤 D.重结晶 E.分液。下列各组混合物的分离或提纯应选用上述哪一种方法最合适?(填方法的标号 )
(1)除去Ca(OH)2溶液中悬浮的CaCO3微粒___ ;
(2)分离四氯化碳与水的混合物____ ;
(3)分离汽油和煤油____ ;
(4)分离碘水中的碘单质____ ;
(5)提纯氯化钠和硝酸钾混合物中的硝酸钾____ 。
(1)除去Ca(OH)2溶液中悬浮的CaCO3微粒
(2)分离四氯化碳与水的混合物
(3)分离汽油和煤油
(4)分离碘水中的碘单质
(5)提纯氯化钠和硝酸钾混合物中的硝酸钾
您最近半年使用:0次
2021-03-25更新
|
78次组卷
|
2卷引用:新疆维吾尔自治区呼图壁县第一中学2020-2021学年高二下学期期初考试化学试题
解题方法
5 . 溶液与人类生产、生活密切相关。
(1)A、B、C三种固体物质的溶解度曲线如图所示。
①t1℃时,A、B、C三种物质的溶解度由大到小的顺序是_________________ 。
②A、B、C三种物质中,溶解度随温度升高而减小的是____ 。
③t2℃时,完全溶解agA物质最少需要水的质量是_____ g。
(2)实验室欲除去粗盐样品中含有的不溶性泥沙,在过滤操作中需要用到的实验仪器和用品有:烧杯、铁架台(带铁圈)、玻璃棒、____ 和滤纸。
(3)在实验室中,配制溶质质量分数为10%的氯化钠溶液45g,需要氯化钠固体的质量是____ g.

(1)A、B、C三种固体物质的溶解度曲线如图所示。
①t1℃时,A、B、C三种物质的溶解度由大到小的顺序是
②A、B、C三种物质中,溶解度随温度升高而减小的是
③t2℃时,完全溶解agA物质最少需要水的质量是
(2)实验室欲除去粗盐样品中含有的不溶性泥沙,在过滤操作中需要用到的实验仪器和用品有:烧杯、铁架台(带铁圈)、玻璃棒、
(3)在实验室中,配制溶质质量分数为10%的氯化钠溶液45g,需要氯化钠固体的质量是

您最近半年使用:0次
6 . 根据下图回答相关问题:
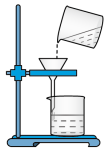
(1)该图所示进行的是过滤操作,图中还缺少的仪器是____ ,其作用是___ 。
(2)添加该仪器后,一名学生用此装置对浑浊的河水进行过滤,过滤两次后,发现滤液仍然浑浊,可能的原因是_______ (写出一点即可)。

(1)该图所示进行的是过滤操作,图中还缺少的仪器是
(2)添加该仪器后,一名学生用此装置对浑浊的河水进行过滤,过滤两次后,发现滤液仍然浑浊,可能的原因是
您最近半年使用:0次
7 . 工业上用“碳捕捉”技术将CO和CO2混合气体中的CO2捕捉并回收CO,其基本过程如下图所示(部分条件及物质未标出):
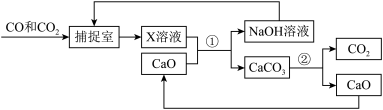
(1)反应②分离出的CO2可制成干冰,干冰常用于_____ 。
(2)反应①在“反应分离室"内进行,将NaOH溶液和CaCO3分离的操作是_____ 。
(3)“捕捉室"中发生反应的化学方程式为_____ 。
(4)下列有关该捕捉过程的叙述正确的有_____
A.捕捉到的CO2可用于制备其他化工产品,减少了温室气体的排放
B.“反应分离室”中的反应要吸收大量热
C.整个过程中只有一种物质可循环利用
D.能耗大是该捕捉技术的一大缺点

(1)反应②分离出的CO2可制成干冰,干冰常用于
(2)反应①在“反应分离室"内进行,将NaOH溶液和CaCO3分离的操作是
(3)“捕捉室"中发生反应的化学方程式为
(4)下列有关该捕捉过程的叙述正确的有
A.捕捉到的CO2可用于制备其他化工产品,减少了温室气体的排放
B.“反应分离室”中的反应要吸收大量热
C.整个过程中只有一种物质可循环利用
D.能耗大是该捕捉技术的一大缺点
您最近半年使用:0次
8 . 金刚石、SiC具有优良的耐磨、耐腐蚀特性,应用广泛。
(1)一定条件下,Na与CCl4可制备金刚石,反应结束冷却至室温后,回收其中的CCl4的实验操作名称为____ 。推测该反应的类型为____ 。(填标号)
A..分解反应 B.置换反应 C.氧化还原反应 D.离子反应
(2)已知:Si+2NaOH+H2O===Na2SiO3+2H2↑。在高温电炉中碳和SiO2反应可制得SiC,同时生成CO,其粗产品中杂质为Si和SiO2。
①请写出电炉中所发生反应的化学方程式:___________ ,每有1 mol SiC生成时,转移电子的物质的量为____ 。
②现将20.0 g SiC粗产品加入到过量的NaOH溶液中充分反应,收集到0.1 mol氢气,过滤得SiC固体11.4 g,滤液稀释到1 L,则硅酸盐的物质的量浓度为______ 。
(3)下列关于金刚石、SiC和单质Si的说法不正确 的是_____ 。(填标号)
A.金刚石、SiC和单质Si都属于无机非金属材料
B.金刚石和石墨、晶体硅和无定形硅分别互为同素异形体
C.金刚石和单质硅都是良好的半导体材料
D.金刚石、SiC和Si晶体结构类似
(1)一定条件下,Na与CCl4可制备金刚石,反应结束冷却至室温后,回收其中的CCl4的实验操作名称为
A..分解反应 B.置换反应 C.氧化还原反应 D.离子反应
(2)已知:Si+2NaOH+H2O===Na2SiO3+2H2↑。在高温电炉中碳和SiO2反应可制得SiC,同时生成CO,其粗产品中杂质为Si和SiO2。
①请写出电炉中所发生反应的化学方程式:
②现将20.0 g SiC粗产品加入到过量的NaOH溶液中充分反应,收集到0.1 mol氢气,过滤得SiC固体11.4 g,滤液稀释到1 L,则硅酸盐的物质的量浓度为
(3)下列关于金刚石、SiC和单质Si的说法
A.金刚石、SiC和单质Si都属于无机非金属材料
B.金刚石和石墨、晶体硅和无定形硅分别互为同素异形体
C.金刚石和单质硅都是良好的半导体材料
D.金刚石、SiC和Si晶体结构类似
您最近半年使用:0次
名校
9 . 如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
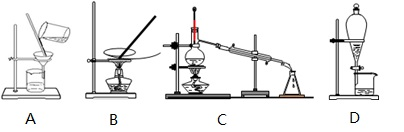
(1)①分离饱和食盐水与沙子的混合物用装置_______ (填代表装置图的字母,下同)
②分离汽油和水的混合物用装置_______ 。
③在装置A和装置B中都用到玻璃棒,装置B中玻璃棒的作用是__________ ,防止蒸发皿内溶液因局部过热而溅出。
(2)装置C中铁圈上方的玻璃容器的名称是__________ ,冷却水的进出口方向是__________ 。
(3)从自来水中得到蒸馏水,选择装置___ ,检验自来水中Cl-是否除净的方法:取少量锥形瓶中的水于洁净试管中,滴加_____ ,不产生白色沉淀表明Cl-已除净。

(1)①分离饱和食盐水与沙子的混合物用装置
②分离汽油和水的混合物用装置
③在装置A和装置B中都用到玻璃棒,装置B中玻璃棒的作用是
(2)装置C中铁圈上方的玻璃容器的名称是
(3)从自来水中得到蒸馏水,选择装置
您最近半年使用:0次
2018-12-19更新
|
229次组卷
|
2卷引用:四川省泸州市泸县第一中学2021-2022学年高一下学期开学考试化学试题



