1 . 无水 常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含有少量碳和
常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含有少量碳和 杂质)为原料制备无水
杂质)为原料制备无水 。
。___________ 。
 常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含有少量碳和
常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含有少量碳和 杂质)为原料制备无水
杂质)为原料制备无水 。
。已知:氯化亚砜(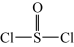 )熔点-101℃,沸点76℃,易水解。
)熔点-101℃,沸点76℃,易水解。

您最近半年使用:0次
2024高三下·全国·专题练习
解题方法
2 . 以焙烧黄铁矿 (杂质为石英等)产生的红渣为原料制备铵铁蓝
(杂质为石英等)产生的红渣为原料制备铵铁蓝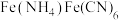 颜料。工艺流程如下:
颜料。工艺流程如下:_______ ,所得母液循环使用。
 (杂质为石英等)产生的红渣为原料制备铵铁蓝
(杂质为石英等)产生的红渣为原料制备铵铁蓝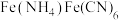 颜料。工艺流程如下:
颜料。工艺流程如下:
您最近半年使用:0次
3 . 图为某学生进行粗盐提纯实验时过滤操作的示意图。试回答:
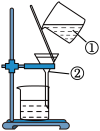
(1)写出标号仪器的名称:
①___________ ;②___________ 。
(2)漏斗中液体的液面应该___________ (填“高”或“低”)于滤纸的边缘。

(1)写出标号仪器的名称:
①
(2)漏斗中液体的液面应该
您最近半年使用:0次
4 . 为除去粗盐中的CaCl2、MgCl2、Na2SO4以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):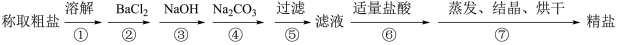
(1)判断BaCl2已过量的方法是___________ 。
(2)第④步中,相关的化学方程式是___________ 。
(3)过滤操作中,需要用到的玻璃仪器有___________ 。
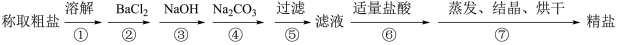
(1)判断BaCl2已过量的方法是
(2)第④步中,相关的化学方程式是
(3)过滤操作中,需要用到的玻璃仪器有
您最近半年使用:0次
5 . Ⅰ.现有下列物质:①蔗糖、②Na2CO3溶液、③稀硫酸、④CO2、⑤CuSO4·5H2O固体、⑥石墨棒、⑦含泥沙的氯化钠溶液、⑧淀粉溶液
(1)属于电解质的是___________ (填序号,下同),属于非电解质的是___________ 。
(2)除去⑦中的泥沙杂质的实验操作方法是___________ 。
(3)将气体④通入②会发生化学反应,其化学方程式为___________ 。
Ⅱ.央视《每周质量报告》曝光了一些明胶企业将皮革废料熬制成工业明胶,出售给某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,会对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(4)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是___________ 价。Fe(CrO2)2属于___________ (填“酸”、“碱”、“盐”或“氧化物”)。
(5)明胶的水溶液和K2SO4溶液共同具备的性质是___________(填序号)。
(1)属于电解质的是
(2)除去⑦中的泥沙杂质的实验操作方法是
(3)将气体④通入②会发生化学反应,其化学方程式为
Ⅱ.央视《每周质量报告》曝光了一些明胶企业将皮革废料熬制成工业明胶,出售给某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,会对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(4)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是
(5)明胶的水溶液和K2SO4溶液共同具备的性质是___________(填序号)。
| A.都不稳定,密封放置会产生沉淀 | B.分散质粒子可通过滤纸 |
| C.分散质粒子可通过半透膜 | D.二者均有丁达尔效应 |
您最近半年使用:0次
6 . 请选择正确的分离方法:①过滤②蒸馏③降温结晶④萃取⑤分液(请填序号)
(1)除去氯化钾中的二氧化锰___________ 。
(2)分离汽油和氯化钠溶液___________ 。
(3)除去自来水中的杂质___________ 。
(1)除去氯化钾中的二氧化锰
(2)分离汽油和氯化钠溶液
(3)除去自来水中的杂质
您最近半年使用:0次
名校
解题方法
7 . 物质的分离和提纯都是利用物质状态(相)的不同进行操作的,固体与液体、液体与气体、气体与固体的分离都是比较容易,相对的固固分离、液液分离、气气分离都比较困难。因此我们在进行物质的分离与提纯时经常会使用物质的状态不同进行分离。
(1)HCl中含有少量水蒸气选用的试剂为:___________ 。
(2)酒精和水分离的操作名称为:___________ 。
(3)除去CO2中的CO可采取的操作是:___________ 。
(4)氯化钠、硝酸钾的混合物中去除氯化钠的操作名称为___________ 。
(5)上述实验操作的具体操作为:___________ 。
(6)上述操作如果除不干净,可以采用的操作为___________ 。
(1)HCl中含有少量水蒸气选用的试剂为:
(2)酒精和水分离的操作名称为:
(3)除去CO2中的CO可采取的操作是:
(4)氯化钠、硝酸钾的混合物中去除氯化钠的操作名称为
(5)上述实验操作的具体操作为:
(6)上述操作如果除不干净,可以采用的操作为
您最近半年使用:0次
8 . 高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂。工业上制备高铁酸钾以及高铁酸钾处理污水的部分流程如下:

过程①制取1mol Na2FeO4,理论上需要Na2O2的物质的量为__________ 。步骤②中反应能够发生的原因是__________ 。分离出K2FeO4固体的操作中使用的玻璃仪器有__________ 。

过程①制取1mol Na2FeO4,理论上需要Na2O2的物质的量为
您最近半年使用:0次
9 . 选择下列实验方法分离物质,将分离方法的字母序号填在横线上。
A.过滤法B.分液法C.蒸馏法D.结晶法
(1)___________ 分离水和豆油的混合物;
(2)___________ 从含有硝酸钾和少量氯化钾的混合溶液中获得硝酸钾;
(3)___________ 分离饱和食盐水和沙子的混合物;
(4)_______ 分离四氯化碳(沸点为 )和甲苯(沸点为
)和甲苯(沸点为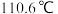 ),已知四氯化碳和甲苯互溶。
),已知四氯化碳和甲苯互溶。
A.过滤法B.分液法C.蒸馏法D.结晶法
(1)
(2)
(3)
(4)
 )和甲苯(沸点为
)和甲苯(沸点为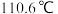 ),已知四氯化碳和甲苯互溶。
),已知四氯化碳和甲苯互溶。
您最近半年使用:0次
名校
10 . 回答下列问题
(1)已知硫酸钠溶解度随温度升高而增大,若想从混有少量氯化钠的硫酸钠溶液中获得纯净的硫酸钠,可采取的操作为___________ 、___________ 、过滤、___________ 、干燥。
(2)将Wg芒硝(Na2SO4·10H2O,M=322g/mol)溶解在VmL水中,得到饱和溶液,测得该饱和溶液的密度为ρg/cm3,测溶液的物质的量浓度为___________ ,该温度下,Na2SO4的溶解度为___________ 。
(1)已知硫酸钠溶解度随温度升高而增大,若想从混有少量氯化钠的硫酸钠溶液中获得纯净的硫酸钠,可采取的操作为
(2)将Wg芒硝(Na2SO4·10H2O,M=322g/mol)溶解在VmL水中,得到饱和溶液,测得该饱和溶液的密度为ρg/cm3,测溶液的物质的量浓度为
您最近半年使用:0次



