名校
1 . 今有A、B、C、D、E五种装置如图所示
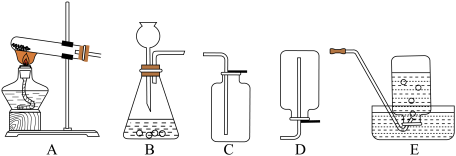
按下列要求回答问题(所选装置用其代号字母表示)
(1)实验室用高锰酸钾的加热分解来制取氧气时,发生装置选用___________ ,收集装置选用___________ ,该装置制取氧气的化学方程式为___________ 。
(2)实验室用大理石和稀盐酸来制取二氧化碳时,发生装置选用___________ ,收集装置选用___________ ,该制取二氧化碳的化学方程式为___________ 。
(3)胶体是一种特殊的分散系,实验室制备氢氧化铁胶体的原理是___________ ,制备的氢氧化铁胶体中会含有少量氯化铁溶液,提纯氢氧化铁胶体的方法是___________ ,向氢氧化铁胶体中加入稀硫酸,刚开始的现象是___________ ,是因为___________ ,接下来的现象是___________ ,反应的化学反应方程式是___________ 。

按下列要求回答问题(所选装置用其代号字母表示)
(1)实验室用高锰酸钾的加热分解来制取氧气时,发生装置选用
(2)实验室用大理石和稀盐酸来制取二氧化碳时,发生装置选用
(3)胶体是一种特殊的分散系,实验室制备氢氧化铁胶体的原理是
您最近一年使用:0次
2021-10-20更新
|
166次组卷
|
3卷引用:贵州省六盘水红桥学校2021-2022学年高一上学期期中考试化学试题
解题方法
2 . 下列各组物质可用渗析法分离的是( )
| A.NaCl和水 | B.淀粉胶体和NaCl溶液 |
| C.乙醇和水 | D.碳酸钙和NaCl固体混合物 |
您最近一年使用:0次
3 . 下列应用或事实与胶体的性质无关的是( )
| A.清晨的阳光穿过茂密的林木枝叶所产生的美丽的光线 |
| B.向FeCl3溶液中滴加NaOH溶液出现红褐色沉淀 |
| C.肾功能衰竭等疾病引起的尿中毒,可利用半透膜进行血液透析 |
| D.在海水与河水交界处,易形成三角洲 |
您最近一年使用:0次
2019-09-21更新
|
211次组卷
|
6卷引用:贵州省毕节市实验高级中学2020-2021学年高一上学期期中考试化学试题
贵州省毕节市实验高级中学2020-2021学年高一上学期期中考试化学试题云南省漾濞二中2019-2020学年高二上学期开学考试化学试题云南省昆明市寻甸县第三中学2019-2020学年高一上学期期末考试化学试题广东省惠州市惠阳区中山中学2021-2022学年高一上学期期中质量检测化学试题(已下线)第06讲 分散系 胶体-【暑假自学课】2022年新高一化学暑假精品课(沪科版2020必修第一册)(已下线)1.1.2 分散系-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)
名校
解题方法
4 . 塑化剂的成分主要是邻苯二甲酸二异丁酯等酯类,塑料管道、塑胶容器、瓶盖或其他塑料包装材料都含有塑化剂,塑化剂超标对人体有害.调查发现,最近深受关注的白酒中含有的塑化剂主要是由塑料制品中的塑化剂迁移到酒中所致,此处“迁移”所涉及的主要原理是( )
| A.萃取 | B.蒸馏 | C.溶解 | D.渗析 |
您最近一年使用:0次
2016-12-09更新
|
145次组卷
|
4卷引用:贵州省龙里中学2019-2020学年高二上学期期末考试化学试题
贵州省龙里中学2019-2020学年高二上学期期末考试化学试题(已下线)2014年人教版高中化学选修二第三章3.3练习卷云南省红河哈尼族彝族自治州绿春县一中2019-2020学年高二上学期12月月考化学试题云南省河口县第一中学2019-2020学年高二上学期12月月考化学试题
5 . 填写下列空白:
(1)Fe(OH)3胶体呈红褐色,插入两个惰性电极,通直流电一段时间,阴极附近的颜色逐渐变深,这种现象叫______________ 。
(2)强光通过Fe(OH)3胶体,可看到光带,这种现象叫________________ 。
(3)淀粉与食盐的混合液放在肠衣(半透膜)中,并把它悬挂在盛有蒸馏水的烧瓶里,从而使淀粉与食盐分离,这种方法_______________ 。
(4)Fe(OH)3胶体加硅酸胶体,胶体变得浑浊,这是发生了____________ 。
(5)已知冰的熔化热为6.0 kJ/mol,冰中氢键键能为20 kJ/mol,假设1 mol冰中有2 mol氢键,且熔化热完全用于破坏冰的氢键,则最多只能破坏冰中_____ %的氢键
(1)Fe(OH)3胶体呈红褐色,插入两个惰性电极,通直流电一段时间,阴极附近的颜色逐渐变深,这种现象叫
(2)强光通过Fe(OH)3胶体,可看到光带,这种现象叫
(3)淀粉与食盐的混合液放在肠衣(半透膜)中,并把它悬挂在盛有蒸馏水的烧瓶里,从而使淀粉与食盐分离,这种方法
(4)Fe(OH)3胶体加硅酸胶体,胶体变得浑浊,这是发生了
(5)已知冰的熔化热为6.0 kJ/mol,冰中氢键键能为20 kJ/mol,假设1 mol冰中有2 mol氢键,且熔化热完全用于破坏冰的氢键,则最多只能破坏冰中
您最近一年使用:0次



