名校
1 . Ⅰ.(1)某校研究性学习小组的学生欲制取、收集氨气,并探究氨气的有关性质,请你参与回答实验中的有关问题。
①要收集较纯的干燥氨气,使用的收集方法是____________________ 。
②甲、乙两小组的学生用相同容积的圆底烧瓶各收集一瓶干燥氨气,进行实验,结果都产生了喷泉,说明氨气_____________ 溶于水。
(2)某兴趣小组为验证SO2和Cl2的漂白性,设计了如下方案,请你参与回答下列问题(尾气处理装置未画出)。

①如图甲所示,向品红溶液中通入SO2,同学们发现品红溶液褪色了,停止通气体,加热试管,发现溶液又变为红色,说明SO2的漂白是___________________ (填“可恢复的”或“不可恢复的”)。
②如图乙所示,将干燥的Cl2和SO2按其体积比1:1混合,通入石蕊溶液中,发现石蕊溶液变红,但不褪色,试用化学方程式解释之:_____________________________________________________________ 。
Ⅱ.某小组同学为了获取在Fe(OH)2制备过程中,沉淀颜色的改变与氧气有关的实验证据,用图1所示装置进行了如下实验(夹持装置已略去,气密性已检验)。

【进行实验】
实验步骤:(1)Ⅰ向瓶中加入饱和FeSO4溶液,按图1所示连接装置;
(2)打开磁力搅拌器,立即加入10% NaOH溶液;
(3)采集瓶内空气中O2含量和溶液中O2含量(DO)的数据。
实验现象:生成白色絮状沉淀,白色沉淀迅速变为灰绿色,一段时间后部分变为红褐色。
实验数据:

【解释与结论】
(1)搅拌的目的是________________________________________________________ 。
(2)生成白色沉淀的离子方程式是__________________________________________ 。
(3)红褐色沉淀是________________________ 。
(4)通过上述实验,可得到“在Fe(OH)2制备过程中,沉淀颜色改变与氧气有关”的结论,其实验证据是_____________________________________________________________________________ 。
①要收集较纯的干燥氨气,使用的收集方法是
②甲、乙两小组的学生用相同容积的圆底烧瓶各收集一瓶干燥氨气,进行实验,结果都产生了喷泉,说明氨气
(2)某兴趣小组为验证SO2和Cl2的漂白性,设计了如下方案,请你参与回答下列问题(尾气处理装置未画出)。

①如图甲所示,向品红溶液中通入SO2,同学们发现品红溶液褪色了,停止通气体,加热试管,发现溶液又变为红色,说明SO2的漂白是
②如图乙所示,将干燥的Cl2和SO2按其体积比1:1混合,通入石蕊溶液中,发现石蕊溶液变红,但不褪色,试用化学方程式解释之:
Ⅱ.某小组同学为了获取在Fe(OH)2制备过程中,沉淀颜色的改变与氧气有关的实验证据,用图1所示装置进行了如下实验(夹持装置已略去,气密性已检验)。

【进行实验】
实验步骤:(1)Ⅰ向瓶中加入饱和FeSO4溶液,按图1所示连接装置;
(2)打开磁力搅拌器,立即加入10% NaOH溶液;
(3)采集瓶内空气中O2含量和溶液中O2含量(DO)的数据。
实验现象:生成白色絮状沉淀,白色沉淀迅速变为灰绿色,一段时间后部分变为红褐色。
实验数据:

【解释与结论】
(1)搅拌的目的是
(2)生成白色沉淀的离子方程式是
(3)红褐色沉淀是
(4)通过上述实验,可得到“在Fe(OH)2制备过程中,沉淀颜色改变与氧气有关”的结论,其实验证据是
您最近一年使用:0次
名校
2 . 利用下列实验装置完成对应的实验,能达到实验目的的是
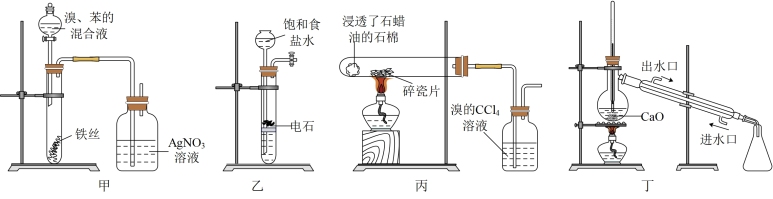

| A.装置甲验证苯与液溴发生取代反应 |
| B.装置乙进行实验室制乙炔 |
| C.装置丙检验石蜡油裂解产生的气体中含有不饱和烃 |
| D.装置丁进行分馏石油 |
您最近一年使用:0次
2022-05-20更新
|
281次组卷
|
4卷引用:福建省德化一中、永安一中、漳平一中三校协作2021-2022学年高二下学期5月联考化学试题
名校
解题方法
3 . 利用如图装置制取下表中的四种气体(图中夹持仪器已略去;a、b、c表示相应仪器中加入的试剂),能达到实验目的的是( )
| 选项 | 气体 | a | b | c |  |
| A | H2 | 稀硫酸 | Zn | 浓硫酸 | |
| B | CO2 | 盐酸 | CaCO3 | 饱和碳酸氢钠溶液 | |
| C | NH3 | 浓氨水 | CaO | 浓硫酸 | |
| D | Cl2 | 浓盐酸 | MnO2 | 饱和食盐水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-01-09更新
|
119次组卷
|
2卷引用:福建省厦门第六中学2021-2022学年高二上学期开学适应性练习化学试题
名校
4 . 设计学生实验要注意安全、无污染、现象明显。根据启普发生器原理,可用底部有小孔的试管制简易的气体发生器(如图)。若关闭K,不能使反应停止,可将试管从烧杯中取出(会有部分气体逸散)。下列气体的制取宜使用该装置的是( )
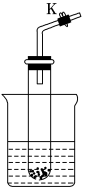

| A.用二氧化锰(粉末)与双氧水制氧气 | B.用大理石块与稀盐酸制CO2 |
| C.用硫化亚铁(块状)与盐酸制硫化氢 | D.铜片与浓硫酸制二氧化硫 |
您最近一年使用:0次
5 . 用如图所示装置能制备下列干燥的气体,且能控制反应的发生和停止的是(甲、乙、丙表示加入的试剂,部分夹持装置省略)
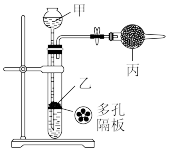

| 选项 | 气体 | 甲 | 乙 | 丙 |
| A | Cl2 | 浓盐酸 | 二氧化锰 | 氯化钙 |
| B | CO2 | 稀硫酸 | 石灰石 | 五氧化二磷 |
| C | C2H2 | 饱和食盐水 | 电石 | 碱石灰 |
| D | H2 | 稀硫酸 | 锌粒 | 碱石灰 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-03-07更新
|
472次组卷
|
3卷引用:福建省厦门外国语学校石狮分校2021-2022学年高二下学期3月月考化学试题
名校
解题方法
6 . 苯胺为无色油状液体,沸点184℃,易被氧化,有碱性,与酸反应生成盐。实验室以硝基苯为原料通过反应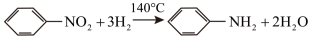 制备苯胺,反应结束后,关闭装置活塞K,加入生石灰。调整好温度计的位置,继续加热,收集182~186℃馏分,得到较纯苯胺。实验装置(夹持及加热装置略)如图。下列说法正确的是
制备苯胺,反应结束后,关闭装置活塞K,加入生石灰。调整好温度计的位置,继续加热,收集182~186℃馏分,得到较纯苯胺。实验装置(夹持及加热装置略)如图。下列说法正确的是

 制备苯胺,反应结束后,关闭装置活塞K,加入生石灰。调整好温度计的位置,继续加热,收集182~186℃馏分,得到较纯苯胺。实验装置(夹持及加热装置略)如图。下列说法正确的是
制备苯胺,反应结束后,关闭装置活塞K,加入生石灰。调整好温度计的位置,继续加热,收集182~186℃馏分,得到较纯苯胺。实验装置(夹持及加热装置略)如图。下列说法正确的是
| A.冷凝管也可采用球形冷凝管 |
| B.长颈漏斗内的酸最好选用盐酸 |
| C.反应时,应先通一段时间H2再加热 |
| D.为了加快氢气生成速率,可用锌粉代替锌粒 |
您最近一年使用:0次
2021-12-31更新
|
709次组卷
|
3卷引用:福建省福建师范大学附属中学2021-2022学年高二下学期期末考试化学试题
名校
解题方法
7 . 某研究性学习小组设计了一组实验来验证元素周期律.
用过氧化氢的水溶液和二氧化锰制备氧气,并将其通入到氢硫酸(H2S的水溶液)中.

(1)过氧化氢的电子式:_______________ ;
(2)从图1中选择氧气的制备装置______ ,反应前需要的操作是:________________ ;
(3)该实验如何证明O的非金属性强于S(用化学方程式表示)_____________ ;
(4)你认为能证明Cl的非金属性强于S的是___________
a.S在常温下为固体而Cl2为气体 b.H2S不如HCl稳定
c.H2SO3的酸性弱于HClO3 d.S与H2化合不如Cl2与H2化合剧烈
用过氧化氢的水溶液和二氧化锰制备氧气,并将其通入到氢硫酸(H2S的水溶液)中.

(1)过氧化氢的电子式:
(2)从图1中选择氧气的制备装置
(3)该实验如何证明O的非金属性强于S(用化学方程式表示)
(4)你认为能证明Cl的非金属性强于S的是
a.S在常温下为固体而Cl2为气体 b.H2S不如HCl稳定
c.H2SO3的酸性弱于HClO3 d.S与H2化合不如Cl2与H2化合剧烈
您最近一年使用:0次
2017-04-15更新
|
349次组卷
|
4卷引用:福建省莆田锦江中学2022-2023学年高二下学期期中考试化学试题



