1 . 水是清洁、可持续的氢能来源。利用太阳能从水中获取氢气符合可持续发展的理念。“太阳能直接热分解水制氢”通过集中阳光产生2000K以上高温,促使 分解为
分解为 和
和 ;若温度进一步升高至5000K,
;若温度进一步升高至5000K, 与
与 会分解为气态原子。
会分解为气态原子。
(1) 分解过程中断裂的化学键属于
分解过程中断裂的化学键属于___________ 。
A.离子键 B.极性共价键 C.非极性共价键
(2)在相同条件下,同时存在如下两个过程:
i.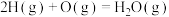 ii.
ii.
比较下列量的相对大小(均从选项中选择):①放出热量___________ ;②反应速率___________ 。
A.i>ii B.i=ii C.i<ii
“太阳能光催化分解水制氢”原理可以表示为: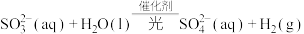 。
。
(3)已知 呈平面正三角形结构,推测
呈平面正三角形结构,推测 的立体构型为
的立体构型为___________ 。
A.平面正三角形 B.正四面体型 C.三角锥型
(4)能说明氯的非金属性比硫强的事实是___________。
(5) 与
与 结构相似,但
结构相似,但 的沸点高于
的沸点高于 ,原因是
,原因是___________ 。
(6)反应开始一段时间后,取出一定量溶液,写出检验溶液中 的操作方法:
的操作方法:________ 。
“太阳能热化学循环制氢”是将太阳能转化成化学能,通过多个化学过程产生 。如常见的铁氧化物循环制氢过程如图所示。
。如常见的铁氧化物循环制氢过程如图所示。
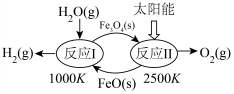
(7)写出反应I的化学方程式:___________ ;若该反应生成标准状况下 氢气,转移电子数目为
氢气,转移电子数目为___________ 。
(8)科学家想要用组成相似的钴氧化物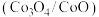 代替铁氧化物进行循环制氢。查阅资料发现,使用钴氧化物后反应I和反应II的
代替铁氧化物进行循环制氢。查阅资料发现,使用钴氧化物后反应I和反应II的 值随温度
值随温度 变化如图所示。
变化如图所示。
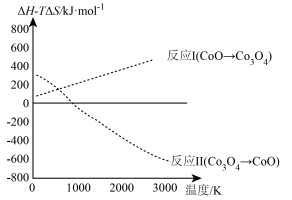
结合图像判断能否用钴氧化物代替铁氧化物进行热化学循环制氢?若可行,举出采用钴氧化物的一个优势;若不可行,说明理由___________ 。
(9)除了上述“直接热分解”、“光催化分解”和“热化学循环”外,请再设计一种利用太阳能从水中获取氢气的方法:___________ (简述即可,不必展开)。
 分解为
分解为 和
和 ;若温度进一步升高至5000K,
;若温度进一步升高至5000K, 与
与 会分解为气态原子。
会分解为气态原子。(1)
 分解过程中断裂的化学键属于
分解过程中断裂的化学键属于A.离子键 B.极性共价键 C.非极性共价键
(2)在相同条件下,同时存在如下两个过程:
i.
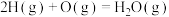 ii.
ii.
比较下列量的相对大小(均从选项中选择):①放出热量
A.i>ii B.i=ii C.i<ii
“太阳能光催化分解水制氢”原理可以表示为:
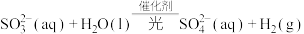 。
。(3)已知
 呈平面正三角形结构,推测
呈平面正三角形结构,推测 的立体构型为
的立体构型为A.平面正三角形 B.正四面体型 C.三角锥型
(4)能说明氯的非金属性比硫强的事实是___________。
A.溶解性: | B.氧化性: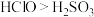 |
C.热稳定性: | D.酸性: |
(5)
 与
与 结构相似,但
结构相似,但 的沸点高于
的沸点高于 ,原因是
,原因是(6)反应开始一段时间后,取出一定量溶液,写出检验溶液中
 的操作方法:
的操作方法:“太阳能热化学循环制氢”是将太阳能转化成化学能,通过多个化学过程产生
 。如常见的铁氧化物循环制氢过程如图所示。
。如常见的铁氧化物循环制氢过程如图所示。
(7)写出反应I的化学方程式:
 氢气,转移电子数目为
氢气,转移电子数目为(8)科学家想要用组成相似的钴氧化物
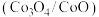 代替铁氧化物进行循环制氢。查阅资料发现,使用钴氧化物后反应I和反应II的
代替铁氧化物进行循环制氢。查阅资料发现,使用钴氧化物后反应I和反应II的 值随温度
值随温度 变化如图所示。
变化如图所示。
结合图像判断能否用钴氧化物代替铁氧化物进行热化学循环制氢?若可行,举出采用钴氧化物的一个优势;若不可行,说明理由
(9)除了上述“直接热分解”、“光催化分解”和“热化学循环”外,请再设计一种利用太阳能从水中获取氢气的方法:
您最近一年使用:0次
2 . 下列关于某无色溶液中离子检验的操作、现象与结论对应正确的是( )
| 检验操作 | 现象 | 结论 | |
| A | 加入盐酸酸化的氯化钡 | 产生白色沉淀 | 一定有SO |
| B | 加入氯水与四氯化碳 | 有机层呈紫色 | 一定有I- |
| C | 加入足量稀盐酸 | 产生无色气体 | 一定有CO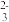 |
| D | 加入硝酸银溶液 | 产生白色沉淀 | 一定有Cl- |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
3 . 某溶液中只可能含有K+、Mg2+、Al3+、Br-、OH-、CO32-、SO32-中的一种或几种。取样,滴加足量氯水,有气泡产生,溶液变为橙色;向橙色溶液中加BaCl2溶液无明显现象。为确定该溶液的组成,还需进行的实验是( )
| A.取样,进行焰色反应 |
| B.取样,滴加酚酞溶液 |
| C.取样,加入足量稀HNO3,再滴加AgNO3溶液 |
| D.取样,加入足量BaCl2溶液,再滴加紫色石蕊溶 |
您最近一年使用:0次
2018-08-24更新
|
591次组卷
|
3卷引用:上海市虹口区2016年高考二模化学试题
名校
4 . 某实验小组用两种不同的方法测定已部分变质的亚硫酸钠样品的纯度。
方案一:实验流程如下
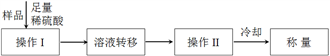
(1)简述检验亚硫酸钠样品已经变质的方法________________________________ 。
(2)操作Ⅱ的名称是________ ,整个实验过程中需要用到的仪器主要有烧杯、玻璃棒、干燥器、酒精灯、石棉网、_________ 、________ (固定、夹持仪器除外)。
(3)能证明冷却后称量的质量已达恒重的依据是_______________________________ 。
方案二:下图,Y管左侧装亚硫酸钠样品,右侧装较浓硫酸,相互接触即可反应产生SO2,通过测定SO2体积来测定样品中Na2SO3含量。
(4)如图,加入试剂之前须进行的操作是________ ;反应不用稀硫酸原因_________ ,为减小实验误差,量气管中液体M可用_________ 。
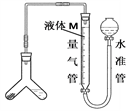
(5)若样品的质量为ag,加入10mL较浓硫酸充分反应后,测得排出液体的体积为VL(标准状况下),则样品中Na2SO3的质量分数的计算式为_________________________ 。
(6)若实验结果测得该样品中Na2SO3含量偏低,原因可能是_________ (选填编号)
a.硫酸不足量
b.测定气体体积时未冷却至室温
c.Y形管中留有反应生成的气体
d.测定气体体积时水准管的液面高于量气管的液面
方案一:实验流程如下

(1)简述检验亚硫酸钠样品已经变质的方法
(2)操作Ⅱ的名称是
(3)能证明冷却后称量的质量已达恒重的依据是
方案二:下图,Y管左侧装亚硫酸钠样品,右侧装较浓硫酸,相互接触即可反应产生SO2,通过测定SO2体积来测定样品中Na2SO3含量。
(4)如图,加入试剂之前须进行的操作是

(5)若样品的质量为ag,加入10mL较浓硫酸充分反应后,测得排出液体的体积为VL(标准状况下),则样品中Na2SO3的质量分数的计算式为
(6)若实验结果测得该样品中Na2SO3含量偏低,原因可能是
a.硫酸不足量
b.测定气体体积时未冷却至室温
c.Y形管中留有反应生成的气体
d.测定气体体积时水准管的液面高于量气管的液面
您最近一年使用:0次
2018-01-11更新
|
168次组卷
|
3卷引用:上海市复兴高级中学2022-2023学年高二上学期10月质量检测练习化学试卷
上海市复兴高级中学2022-2023学年高二上学期10月质量检测练习化学试卷上海市闵行区2018届高三上学期质量调研化学试题(已下线)【中等生百日捷进提升系列-技能方法】专题25 产物检验型实验探究评价题



