解题方法
1 . 现有四瓶失去标签的溶液,分别为 溶液、
溶液、 溶液、
溶液、 溶液、
溶液、 溶液。若不用其他试剂进行区别,请设计实验方案。
溶液。若不用其他试剂进行区别,请设计实验方案。______
 溶液、
溶液、 溶液、
溶液、 溶液、
溶液、 溶液。若不用其他试剂进行区别,请设计实验方案。
溶液。若不用其他试剂进行区别,请设计实验方案。
您最近一年使用:0次
2021高三·全国·专题练习
解题方法
2 . NO2与溴蒸气的鉴别可用NaOH溶液,溶于NaOH溶液得无色溶液的是NO2,得橙色溶液的为溴蒸气。(_______)
您最近一年使用:0次
2021高三·全国·专题练习
解题方法
3 . 用酚酞溶液可鉴别饱和食盐水和饱和碳酸钠溶液。( )
您最近一年使用:0次
名校
4 . 选用一种试剂,通过一步操作(必要时可以加热)即可鉴别Na2CO3、NH4Cl、(NH4)2SO4、KNO3 四种溶液,该试剂是
| A.AgNO3 溶液 | B.NaOH溶液 | C.Ba(OH)2溶液 | D.盐酸 |
您最近一年使用:0次
2022-03-14更新
|
202次组卷
|
5卷引用:福建省福州高级中学2021–2022学年高一上学期半期考试化学试题
5 . 请用化学方法鉴别苯、乙醇、乙酸、甲酸溶液和苯酚溶液。
(1)写出鉴别方法和使用化学试剂的先后顺序_______ 。
(2)写出有关反应的化学方程式_______ 。
(1)写出鉴别方法和使用化学试剂的先后顺序
(2)写出有关反应的化学方程式
您最近一年使用:0次
2021-12-04更新
|
535次组卷
|
2卷引用:人教2019版选择性必修三第三章 烃的衍生物 复习与提高
6 . 为进一步研究过氧化钠与水的反应,某活动小组进行了如下探究。
(1)把一定量水滴入盛有少量过氧化钠固体的试管中,反应的化学方程式为___ 。
(2)向反应后的溶液中滴入酚酞,一段时间后,发现溶液颜色逐渐变浅,最后颜色消失。为探究原因,进行实验1(环境温度为30℃)结果如下:
结合表中数据,判断下列说法正确的是___ 。(填字母)
a.其他条件相同时,NaOH溶液浓度越大褪色越快
b.溶液褪色可能是NaOH溶液浓度过大导致的
c.当NaOH溶液浓度大于或等于1.0mol/L时,对溶液颜色变化有明显影响
(3)中间产物H2O2也可能会对溶液颜色的变化产生影响。
①假设1:受H2O2自身氧化性的影响。
为验证假设,设计实验方案:___ 。实验表明,随H2O2浓度的增大,溶液颜色变化更快。
②假设2:___ 。
为验证假设,设计了实验2,请补全实验装置___ 。

实验2结果如下:
对比实验1,表中数据说明___ 。
(4)若准确称取Na2O2的质量为1.56g,加入一定体积的水后得到20mL溶液,则所得NaOH溶液的物质的量浓度为___ 。
(5)实验过程中,需待Na2O2固体完全溶解后再加入酚酞,原因是___ 。
综上所述,Na2O2与水反应过程复杂,滴入酚酞时溶液颜色变化受多因素影响。
(1)把一定量水滴入盛有少量过氧化钠固体的试管中,反应的化学方程式为
(2)向反应后的溶液中滴入酚酞,一段时间后,发现溶液颜色逐渐变浅,最后颜色消失。为探究原因,进行实验1(环境温度为30℃)结果如下:
NaOH溶液浓度/(mol/L) | 10.0 | 2.0 | 1.0 | 0.10 | 0.010 |
滴入酚酞时现象 | 深紫红色 | 深红色 | 深红色 | 深红色 | 深红色 |
溶液变为浅红色时间 | 2~3s | 26~30s | 54~60s | 6~7min | 45min内稳定不变 |
溶液完全褪色时间 | 7~8s | 50~54s 几乎无色 | 100~110s 几乎无色 | 20min后仍为浅红色 | 2h后略变浅 |
最终溶液是否褪色 | 褪色 | 褪色 | 褪色 | 不褪色 | 不褪色 |
a.其他条件相同时,NaOH溶液浓度越大褪色越快
b.溶液褪色可能是NaOH溶液浓度过大导致的
c.当NaOH溶液浓度大于或等于1.0mol/L时,对溶液颜色变化有明显影响
(3)中间产物H2O2也可能会对溶液颜色的变化产生影响。
①假设1:受H2O2自身氧化性的影响。
为验证假设,设计实验方案:
②假设2:
为验证假设,设计了实验2,请补全实验装置

实验2结果如下:
NaOH溶液浓度(mol/L) | 滴入酚酞时现象 | 溶液完全褪色时间 |
2.0 | 深红色 | 约50s |
1.0 | 深红色 | 约1min50s |
(4)若准确称取Na2O2的质量为1.56g,加入一定体积的水后得到20mL溶液,则所得NaOH溶液的物质的量浓度为
(5)实验过程中,需待Na2O2固体完全溶解后再加入酚酞,原因是
综上所述,Na2O2与水反应过程复杂,滴入酚酞时溶液颜色变化受多因素影响。
您最近一年使用:0次
名校
7 . 有4 瓶常用溶液∶①BaCl2溶液,②NaCl 溶液,③Na2SO4溶液,④CuSO4溶液。不用其他试剂,即可通过实验方法将它们一一鉴别出来,鉴别出来的先后顺序可能是
| A.①④③② | B.①④②③ | C.①③④② | D.④①②③ |
您最近一年使用:0次
2021-01-11更新
|
135次组卷
|
6卷引用:专题2 第一单元 第2课时 物质的检验 物质性质和变化的探究-高中化学苏教2019版必修第一册
名校
解题方法
8 . 用括号里的试剂鉴别下列各组气体或溶液,其中不合理的是
| A.二氧化碳、氮气、一氧化碳(澄清石灰水) |
| B.氯化钠、硝酸银、碳酸钠(稀盐酸) |
| C.酒精、醋酸、氨水(石蕊试液) |
| D.硫酸、硝酸钡、氯化钾(碳酸钠溶液) |
您最近一年使用:0次
2020-11-29更新
|
141次组卷
|
5卷引用:河北省沧州市第一中学2021-2022学年高一上学期第二次月考(期中)化学试题
9 . 已知HNO2是一种弱酸,向NaNO2中加入强酸可生成HNO2,HNO2不稳定,易分解成NO和NO2气体;HNO2是一种还原剂,能被常见的强氧化剂氧化,但在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+。AgNO2是一种难溶于水、易溶于酸的化合物。试回答下列问题:
(1)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐如NaNO2,则导致血红蛋白中的Fe2+转化为Fe3+而中毒,可以服用维生素C解毒,维生素C在解毒的过程中表现出___ (填“氧化”或“还原”)性。
(2)下列方法中,不能用来区分NaNO2和NaCl的是___ (填字母代号)。
A.加入盐酸,观察是否有气泡产生
B.加入AgNO3溶液观察是否有沉淀生成
C.分别在它们的酸性溶液中加FeCl2溶液,观察溶液颜色变化
(3) 可以与Fe2+反应制备Fe2O3纳米颗粒。
可以与Fe2+反应制备Fe2O3纳米颗粒。
①若 与Fe2+的系数之比为1:2,配平该反应的离子方程式:
与Fe2+的系数之比为1:2,配平该反应的离子方程式:
__ Fe2++__  +
+__ H2O2+__ OH-=__ Fe2O3+__ 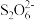 +
+__ H2O
②下列关于该反应的说法正确的是__ (填字母代号)。
A.反应中 表现了氧化性
表现了氧化性
B.已知生成的Fe2O3纳米颗粒直径为10纳米,则该分散系为胶体
C.该反应中H2O2做氧化剂
(1)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐如NaNO2,则导致血红蛋白中的Fe2+转化为Fe3+而中毒,可以服用维生素C解毒,维生素C在解毒的过程中表现出
(2)下列方法中,不能用来区分NaNO2和NaCl的是
A.加入盐酸,观察是否有气泡产生
B.加入AgNO3溶液观察是否有沉淀生成
C.分别在它们的酸性溶液中加FeCl2溶液,观察溶液颜色变化
(3)
 可以与Fe2+反应制备Fe2O3纳米颗粒。
可以与Fe2+反应制备Fe2O3纳米颗粒。①若
 与Fe2+的系数之比为1:2,配平该反应的离子方程式:
与Fe2+的系数之比为1:2,配平该反应的离子方程式: +
+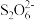 +
+②下列关于该反应的说法正确的是
A.反应中
 表现了氧化性
表现了氧化性B.已知生成的Fe2O3纳米颗粒直径为10纳米,则该分散系为胶体
C.该反应中H2O2做氧化剂
您最近一年使用:0次
2020-11-21更新
|
1028次组卷
|
5卷引用:专题4 第二单元 综合拔高练-高中化学苏教2019版必修第一册
20-21高一上·广西钦州·阶段练习
解题方法
10 . 有5瓶白色固体试剂,分别是氯化钡、氢氧化钠、无水硫酸铜、碳酸钠、硫酸钠。现只提供蒸馏水,通过下面的实验步骤即可鉴别它们。请填写下列空白:
(1)各取适量固体试剂分别加入5支试管中,加入适量蒸馏水,振荡试管,观察到的现象是___________ 。被检出的物质的化学式(分子式)是____________________ 。
(2)分别取未检出的溶液,往其中加入上述已检出的溶液,根据观察到的现象写出相应的方程式: 1 支试管中有白色沉淀生成:__________________ 。2支试管中有蓝色沉淀生成:____________ 。被检出物质的化学式是_____________ 。
(3)鉴别余下未检出物质的方法和观察到的现象是___________________ 。
(1)各取适量固体试剂分别加入5支试管中,加入适量蒸馏水,振荡试管,观察到的现象是
(2)分别取未检出的溶液,往其中加入上述已检出的溶液,根据观察到的现象写出相应的方程式: 1 支试管中有白色沉淀生成:
(3)鉴别余下未检出物质的方法和观察到的现象是
您最近一年使用:0次



