名校
1 . 二氧化氯(ClO2)具有强氧化性,是优良的饮用水消毒剂。ClO2常温下为黄绿色气体,熔点-59℃,沸点11℃,极易溶于水且不与水反应,浓的ClO2受热时易爆炸。我国广泛使用的方法是用干燥的Cl2与NaClO2固体反应制取ClO2,实验室模拟制备ClO2装置如图所示:
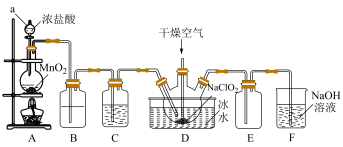
(1)仪器a的名称是:___________ ,装置A中反应的离子方程式为:___________ 。
(2)装置B中盛装的试剂是___________ ,装置C中试剂的作用是:___________ 。
(3)为防止ClO2制备装置发生爆炸,实验中采取的措施:①将装置置于冰水浴中降温,②___________ 。
(4)装置E为ClO2的收集装置,应将其置于___________ 水浴中(填“热”或“冰”)。
(5)装置F为氯气的尾气吸收装置,小组同学用胶头滴管将新制的饱和氯水慢慢滴入含有酚酞的NaOH溶液中,当滴到一定量时,红色突然褪去,小组同学对褪色原因提出假设:
假设1:___________ 。
假设2:可能是氯水中存在HClO具有强氧化性,漂白褪色。
该小组同学设计实验证明假设1是否成立。实验方案为:取少许褪色后的溶液于试管中,滴加足量的NaOH溶液,若___________ (填“实验现象”),则假设1成立。

(1)仪器a的名称是:
(2)装置B中盛装的试剂是
(3)为防止ClO2制备装置发生爆炸,实验中采取的措施:①将装置置于冰水浴中降温,②
(4)装置E为ClO2的收集装置,应将其置于
(5)装置F为氯气的尾气吸收装置,小组同学用胶头滴管将新制的饱和氯水慢慢滴入含有酚酞的NaOH溶液中,当滴到一定量时,红色突然褪去,小组同学对褪色原因提出假设:
假设1:
假设2:可能是氯水中存在HClO具有强氧化性,漂白褪色。
该小组同学设计实验证明假设1是否成立。实验方案为:取少许褪色后的溶液于试管中,滴加足量的NaOH溶液,若
您最近一年使用:0次
2023-11-06更新
|
632次组卷
|
2卷引用:宁夏银川市第二中学2023-2024学年高一上学期期中考试化学试题
2 . 实验室用如图装置制备无水FeCl3。

已知:FeCl3固体易升华,易吸收水分而潮解变质。请回答下列问题:
(1)连接好仪器后首先应进行的操作是_______ ;A装置中连接分液漏斗与烧瓶之间的导管的作用是_______ 。
(2)请写出A装置中反应的离子方程式_______ 。
(3)实验室还可用KMnO4和浓盐酸反应制取氯气:2KMnO4+l6HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,在上述反应中,生成56LCl2(标准状况下),转移电子的个数为_______ 。
(4)写出工业制取漂白粉的化学方程式_______ 。
(5)装置B中长颈漏斗可以检验后续装置是否堵塞,其中饱和食盐水的作用是_______ ,D装置与E装置之间用弧形粗弯管连接而不是普通的直角玻璃导管,其目的是_______ 。
(6)F中所装试剂为_______ ,有学生提出:装置F和G二者可以简约用一个球形干燥管来代替,为了达到相同的作用,球形干燥管内盛放的试剂是_______ 。

已知:FeCl3固体易升华,易吸收水分而潮解变质。请回答下列问题:
(1)连接好仪器后首先应进行的操作是
(2)请写出A装置中反应的离子方程式
(3)实验室还可用KMnO4和浓盐酸反应制取氯气:2KMnO4+l6HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,在上述反应中,生成56LCl2(标准状况下),转移电子的个数为
(4)写出工业制取漂白粉的化学方程式
(5)装置B中长颈漏斗可以检验后续装置是否堵塞,其中饱和食盐水的作用是
(6)F中所装试剂为
您最近一年使用:0次
名校
解题方法
3 . 焦亚硫酸钠(Na2S2O5)是一种常用的食品抗氧化剂(易被氧化)。实验室利用如图所示装置制取少量焦亚硫酸钠并探究SO2的性质(夹持装置已略去)。
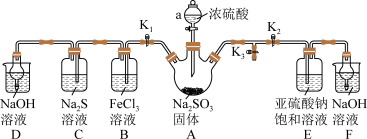
请回答下列问题:(实验前已除去装置中的空气)
(1)仪器a的名称是________ 。
(2)关闭K2、K3,打开K1,装置B中发生反应的离子方程式为_____ ,观察到装置C中发生的现象是_______ 。
(3)装置D和F的作用是_______ 。
(4)实验前,装置E中所用蒸馏水需经煮沸后迅速冷却,目的是____ ,关闭K1、K3,打开K2,一段时间后装置E中有Na2S2O5晶体析出,装置E中发生反应的化学方程式为_______
(5)Na2S2O5可用作食品的抗氧化剂。在测定某葡萄酒中Na2S2O5残留量时,取50.00mL葡萄酒样品,用0.01000 mol·L-1的碘标准液滴定至终点,消耗20.00 mL(S2O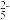 被氧化为SO
被氧化为SO )。滴定反应的离子方程式为
)。滴定反应的离子方程式为_____ ,该样品中Na2S2O5的残留量为_____ g·L-1

请回答下列问题:(实验前已除去装置中的空气)
(1)仪器a的名称是
(2)关闭K2、K3,打开K1,装置B中发生反应的离子方程式为
(3)装置D和F的作用是
(4)实验前,装置E中所用蒸馏水需经煮沸后迅速冷却,目的是
(5)Na2S2O5可用作食品的抗氧化剂。在测定某葡萄酒中Na2S2O5残留量时,取50.00mL葡萄酒样品,用0.01000 mol·L-1的碘标准液滴定至终点,消耗20.00 mL(S2O
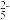 被氧化为SO
被氧化为SO )。滴定反应的离子方程式为
)。滴定反应的离子方程式为
您最近一年使用:0次



