1 . 某学生应用如下图所示的方法研究物质的性质,其中气体A的主要成分是氯气,杂质是空气和水蒸气。回答下列问题:
(1)该项研究(实验)的主要目的是__________________________________ 。
(2)浓H2SO4的作用是_______________________ ,与研究目的直接相关的实验现象是___________________ 。
(3)从物质性质的方面来看,这样的实验设计还存在不妥之处,有隐患,隐患表现为__________________ 。请在D处以图的形式表明克服隐患的措施__________ 。

(1)该项研究(实验)的主要目的是
(2)浓H2SO4的作用是
(3)从物质性质的方面来看,这样的实验设计还存在不妥之处,有隐患,隐患表现为
您最近一年使用:0次
2018-09-23更新
|
60次组卷
|
8卷引用:人教版高一化学必修1第四章《非金属及其化合物》测试卷
人教版高一化学必修1第四章《非金属及其化合物》测试卷鲁科版高中化学必修1第一章《认识化学科学》测试卷(已下线)2011-2012学年甘肃武威六中高一上学期期末考试化学试卷(已下线)2012年人教版高中化学必修一4.2 富集在海水中的元素-氯练习卷(已下线)2012-2013学年山东省高二暑假作业(八)化学试卷陕西省渭南中学2018-2019学年高一上学期教学质量检测月考(一)化学试题(已下线)【走进新高考】(人教版必修一)4.2.1富集在海水中的元素——氯 (氯气) 同步练习01(已下线)衔接点15 氯气的性质-2021年初升高化学无忧衔接
2 . 氯气能使湿润的红色布条褪色。对于使红色布条褪色的物质,同学们的看法不一致,认为氯水中存在的几种粒子都有可能。请设计实验,得出正确结论。
(1)提出问题:
氯水中何种物质能使湿润的红色布条褪色?
(2)收集资料:
①氯气有强氧化性
②氯气与水反应生成盐酸和次氯酸
③次氯酸有强氧化性
(3)提出假设:
①__ ;
②__ ;
③___ ;
④水使红色布条褪色
(4)验证假设:
实验①:把红色干布条放入充满氯气的集气瓶中,布条不褪色;
实验②:__ ;
实验③:把红色布条放在水里,布条不褪色。
(5)得出的实验结论__ 。
(1)提出问题:
氯水中何种物质能使湿润的红色布条褪色?
(2)收集资料:
①氯气有强氧化性
②氯气与水反应生成盐酸和次氯酸
③次氯酸有强氧化性
(3)提出假设:
①
②
③
④水使红色布条褪色
(4)验证假设:
实验①:把红色干布条放入充满氯气的集气瓶中,布条不褪色;
实验②:
实验③:把红色布条放在水里,布条不褪色。
(5)得出的实验结论
您最近一年使用:0次
解题方法
3 . 某同学设计实验验证非金属元素的非金属性越强,其最高价氧化物对应的水化物的酸性就越强。他设计了如图所示装置以验证氮、碳、硅元素的非金属性强弱。

该同学设计的实验可直接证明三种酸的酸性强弱,已知A是强酸,常温下可与铜反应;B是块状固体;打开分液漏斗的活塞后,C中可观察到有白色沉淀生成。
(1)写出所选用物质的化学式:A.___ B.____ C.___
(2)写出烧杯中发生反应的离子方程式:___ 。

该同学设计的实验可直接证明三种酸的酸性强弱,已知A是强酸,常温下可与铜反应;B是块状固体;打开分液漏斗的活塞后,C中可观察到有白色沉淀生成。
(1)写出所选用物质的化学式:A.
(2)写出烧杯中发生反应的离子方程式:
您最近一年使用:0次
9-10高一·全国·单元测试
4 . 某校高一化学研究性学习小组对日常生活中的氯气用途进行了调查,了解到氯气可广泛地应用于衣物的漂白、水体的杀菌和消毒等。
(1)氯气可以用于漂白、消毒的原因是因为能与水作用形成具有______ 性的次氯酸,相关反应的化学方程式为____________________________ 。

(2)在调查某室外游泳池夏季池水消毒情况时,小组成员了解到,该游泳池每周一上午8:00换水,然后通入氯气消毒,通常游泳池中水的含氯量控制在0.5 mg·L-1至1.0 mg·L-1之间时,效果最好。右图是该小组测定的每天19:00时游泳池中水的含氯量,哪几天使用游泳池不安全?______ 。
(3)你认为哪几天的天气炎热、阳光强烈______ ,说出一种理由是
__________________________ (必要的方程式和文字)。
(4)在对游泳池水中通入氯气消毒时,当发生氯气泄漏时,应立即关闭氯气罐,还应采取下列自救方法______ 。
(5)小型游泳池通常使用漂白液(NaClO溶液)而非氯气来消毒池水,试举出使用漂白液消毒而非氯气的一项理由__________________ ;用化学方程式说明工业上如何生产漂白液?________________________________________________________________________ 。
(1)氯气可以用于漂白、消毒的原因是因为能与水作用形成具有

(2)在调查某室外游泳池夏季池水消毒情况时,小组成员了解到,该游泳池每周一上午8:00换水,然后通入氯气消毒,通常游泳池中水的含氯量控制在0.5 mg·L-1至1.0 mg·L-1之间时,效果最好。右图是该小组测定的每天19:00时游泳池中水的含氯量,哪几天使用游泳池不安全?
(3)你认为哪几天的天气炎热、阳光强烈
(4)在对游泳池水中通入氯气消毒时,当发生氯气泄漏时,应立即关闭氯气罐,还应采取下列自救方法
| A.用湿润的毛巾捂住口鼻跑向低处 |
| B.用浸湿小苏打或肥皂水的毛巾捂住口鼻跑向高处 |
| C.用浸湿浓氨水的毛巾捂住口鼻匍匐跑至安全处 |
| D.用浸湿食盐水的毛巾捂住口鼻顺风跑至安全处 |
(5)小型游泳池通常使用漂白液(NaClO溶液)而非氯气来消毒池水,试举出使用漂白液消毒而非氯气的一项理由
您最近一年使用:0次
解题方法
5 . 某化学兴趣小组用如图所示的装置做有关CO2气体的实验:
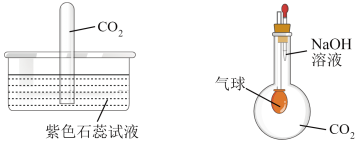
⑴甲同学将收集满CO2气体的试管倒插入紫色石蕊试液中(左图),并轻轻振荡试管。
①描述产生的现象:____________________________________________ 。
②写出反应的化学方程式:____________________________________________ 。
⑵乙同学挤压图装置中滴管的胶头,使其中的NaOH溶液滴入烧瓶,并轻轻振荡,系在导气管一端的气球慢慢胀大。产生这一现象的原因是________________________ (请用离子方程式结合必要的文字说明)。

⑴甲同学将收集满CO2气体的试管倒插入紫色石蕊试液中(左图),并轻轻振荡试管。
①描述产生的现象:
②写出反应的化学方程式:
⑵乙同学挤压图装置中滴管的胶头,使其中的NaOH溶液滴入烧瓶,并轻轻振荡,系在导气管一端的气球慢慢胀大。产生这一现象的原因是
您最近一年使用:0次
10-11高三上·全国·单元测试
6 . 为了探究乙醇和金属钠反应的原理,做了如下四个实验,回答以下问题:
实验一:向小烧杯中加入无水乙醇,再放入一小块金属钠,观察现象,并收集产生的气体。
实验二:设法检验实验一收集到的气体。
实验三:向试管中加入3 mL水,并加入一小块金属钠,观察现象。
实验四:向试管中加入3 mL乙醚,并加入一小块金属钠,观察现象。
(1)简述实验二中检验气体的实验方法及作出判断的依据_______
(2)从结构上分析,该实验选取水和乙醚做参照物的原因是_______
(3)实验三的目的是欲证明_______ ;实验四的目的是欲证明_______ ;根据实验三和实验四的结果,可以证明乙醇和金属钠反应的化学方程式应为_______
实验一:向小烧杯中加入无水乙醇,再放入一小块金属钠,观察现象,并收集产生的气体。
实验二:设法检验实验一收集到的气体。
实验三:向试管中加入3 mL水,并加入一小块金属钠,观察现象。
实验四:向试管中加入3 mL乙醚,并加入一小块金属钠,观察现象。
(1)简述实验二中检验气体的实验方法及作出判断的依据
(2)从结构上分析,该实验选取水和乙醚做参照物的原因是
(3)实验三的目的是欲证明
您最近一年使用:0次
7 . 为探究Na2SO3溶液的性质,在白色点滴板的a、b、c、d四个凹槽中滴入Na2SO3溶液,再分别滴加下图所示的试剂:
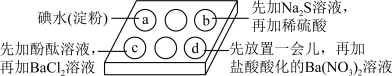
对实验现象的“解释或结论”错误的是( )

对实验现象的“解释或结论”错误的是( )
| 选项 | 实验现象 | 解释或结论 |
| A | a中溶液褪色 | 还原性: |
| B | b中加硫酸后产生淡黄色沉淀 | 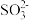 和 和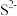 在酸性条件下发生反应 在酸性条件下发生反应 |
| C | c中滴入酚酞溶液变红,再加BaCl2溶液后产生白色沉淀且红色褪色 |  ,所以滴入酚酞变红; ,所以滴入酚酞变红; ,使水解平衡左移,红色褪去 ,使水解平衡左移,红色褪去 |
| D | d中产生白色沉淀 | Na2SO3溶液已变质 |
| A.A |
| B.B |
| C.C |
| D.D |
您最近一年使用:0次
解题方法
8 . 某化学兴趣小组为探究Cl2、Br2、Fe3+的氧化性强弱,设计了如下实验:
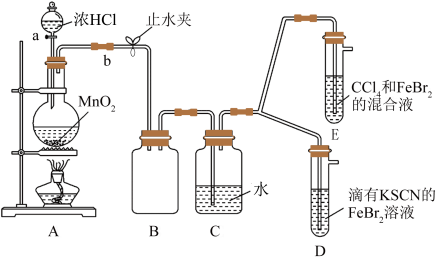
(1)①装置A中发生反应的离子方程式是______________ 。
②整套实验装置存在一处明显的不足,请指出_______________________ 。
(2)因忙于观察和记录,没有及时停止反应,D、E中均发生了新的变化。D装置中:红色慢慢褪去。E装置中:CCl4层先由无色变为橙色,后颜色逐渐加深,直至变成红色。
为探究上述实验现象的本质,小组同学查得资料如下:
①用平衡移动原理(结合上述资料)解释Cl2过量时D中溶液红色褪去的原因___________ ,现设计简单实验证明上述解释:取少量褪色后的溶液,滴加____________ 溶液,若溶液颜色________ ,则上述解释是合理的。
②探究E中颜色变化的原因,设计实验如下:用分液漏斗分离出E的下层溶液,蒸馏、收集红色物质,取少量,加入AgNO3溶液,结果观察到仅有白色沉淀产生。请结合上述资料用两步方程式(离子或化学方程式不限定)解释仅产生白色沉淀原因_________________________ 。

(1)①装置A中发生反应的离子方程式是
②整套实验装置存在一处明显的不足,请指出
(2)因忙于观察和记录,没有及时停止反应,D、E中均发生了新的变化。D装置中:红色慢慢褪去。E装置中:CCl4层先由无色变为橙色,后颜色逐渐加深,直至变成红色。
为探究上述实验现象的本质,小组同学查得资料如下:
Ⅰ.Fe3++3SCN- Fe(SCN)3是一个可逆反应。 Fe(SCN)3是一个可逆反应。Ⅱ.(SCN)2性质与卤素单质类似。氧化性:Cl2  (SCN)2。 (SCN)2。Ⅲ.Cl2和Br2反应生成BrCl,BrCl呈红色(略带黄色),沸点 约5 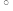 C,它与水能发生水解反应,且该反应为非氧化还原反应。 C,它与水能发生水解反应,且该反应为非氧化还原反应。Ⅳ.AgClO、AgBrO均可溶于水。 |
①用平衡移动原理(结合上述资料)解释Cl2过量时D中溶液红色褪去的原因
②探究E中颜色变化的原因,设计实验如下:用分液漏斗分离出E的下层溶液,蒸馏、收集红色物质,取少量,加入AgNO3溶液,结果观察到仅有白色沉淀产生。请结合上述资料用两步方程式(离子或化学方程式不限定)解释仅产生白色沉淀原因
您最近一年使用:0次
9 . Ⅰ.将刮去氧化膜的镁片投入沸水中,反应的化学方程式为_________ 。
Ⅱ.若用灼热的镁粉与水蒸气反应,则在生成H2的同时还可能得到氧化镁粉未。为实现这一反应并收集一瓶H2,某课外活动小组设计了如图所示的装置。
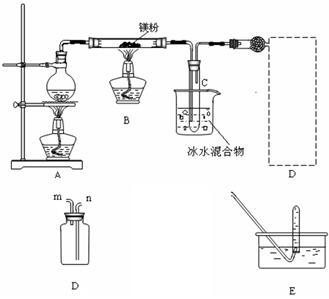
(1)实验开始时,应先点燃__ (填“A”或“B”)处的酒精灯,等观察到___ ,再点燃另一酒精灯。这样做的目的是______ 。
(2)若将装置D与干燥管相连,则所连导管口应为___ (填“m”或“n”),这种方法叫___ (填“向上”、“向下”)排气法
(3)小试管C的作用是________ 。
(4)装置E的作用是检验集气瓶中是否收集满了H2,则检验的操作和需要观察的现象是________ 。
(5)反应一段时间后,B装置玻璃管中可能残留的固体物质除MgO外,还可能Mg和Mg(OH)2 任选其中一种,设计实验证明它的存在,简要写出主要操作.所用试剂.现象及结论________ 。
Ⅱ.若用灼热的镁粉与水蒸气反应,则在生成H2的同时还可能得到氧化镁粉未。为实现这一反应并收集一瓶H2,某课外活动小组设计了如图所示的装置。

(1)实验开始时,应先点燃
(2)若将装置D与干燥管相连,则所连导管口应为
(3)小试管C的作用是
(4)装置E的作用是检验集气瓶中是否收集满了H2,则检验的操作和需要观察的现象是
(5)反应一段时间后,B装置玻璃管中可能残留的固体物质除MgO外,还可能Mg和Mg(OH)2 任选其中一种,设计实验证明它的存在,简要写出主要操作.所用试剂.现象及结论
您最近一年使用:0次



