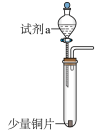
1 . 下述实验中均有红棕色气体产生,对比分析所得结论下正确的是
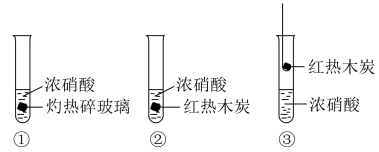
A.由①中的红棕色气体,不能推断产生的气体只含 |
| B.红棕色气体不能表明②中木炭与浓硝酸发生了反应 |
| C.由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物 |
D.③的气体产物中检测出 ,由此说明木炭一定与浓硝酸发生了反应 ,由此说明木炭一定与浓硝酸发生了反应 |
您最近一年使用:0次
2 . 某中学趣味化学实验小组的同学想通过“ 被浓
被浓 氧化”的实验,验证
氧化”的实验,验证 的还原性.
的还原性.
实验一:验证 的还原性
的还原性
(1)红棕色气体是____________ 。(写化学式)
(2)实验现象与预期不符,继续进行实验。
取深棕色溶液于试管中,滴加KSCN溶液,溶液变为红色,该现象说明___________________ 。
实验二:探究溶液变为深棕色的原因
【资料与猜想】
查阅资料后猜想,可能是生成的 或NO与溶液中的
或NO与溶液中的 或
或 反应,而使溶液变为深棕色。
反应,而使溶液变为深棕色。
【实验与探究】
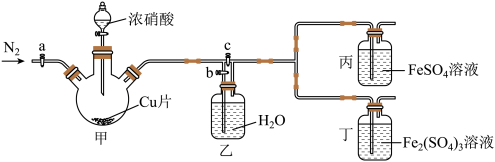
用如图所示装置进行实验(气密性已检验,尾气处理已略去)
ⅱ.向甲中加入适量浓 ,一段时间后丙中溶液变为深棕色,丁中溶液无明显变化;
,一段时间后丙中溶液变为深棕色,丁中溶液无明显变化;
ⅲ.关闭b、打开c,更换丙、丁中的溶液(试剂不变);
ⅳ.继续向甲中加入浓 ,一段时间后观察到了与ⅱ相同的实验现象。
,一段时间后观察到了与ⅱ相同的实验现象。
(3)通入 的目的是
的目的是________________________ 。
(4)铜与浓硝酸反应的离子方程式是__________________________ 。
(5)装置乙的作用是_____________________ 。
(6)实验结论:溶液的深棕色可能是因为 。
【反思与改进】
实验三:验证 的还原性
的还原性
(7)该小组同学依据实验二的结论改进了实验一,观察到了预期现象,其实验操作是向盛有____________ 的试管中滴入几滴____________ ,振荡。
 被浓
被浓 氧化”的实验,验证
氧化”的实验,验证 的还原性.
的还原性.实验一:验证
 的还原性
的还原性实验操作 | 预期现象 | 实验现象 |
向盛有2mL  溶液的试管中,滴入几滴浓硝酸,振荡。 溶液的试管中,滴入几滴浓硝酸,振荡。 | 试管中产生红棕色气体,溶液变为黄色。 | 试管中产生红棕色气体,溶液变为深棕色。 |
(1)红棕色气体是
(2)实验现象与预期不符,继续进行实验。
取深棕色溶液于试管中,滴加KSCN溶液,溶液变为红色,该现象说明
实验二:探究溶液变为深棕色的原因
【资料与猜想】
查阅资料后猜想,可能是生成的
 或NO与溶液中的
或NO与溶液中的 或
或 反应,而使溶液变为深棕色。
反应,而使溶液变为深棕色。【实验与探究】
用如图所示装置进行实验(气密性已检验,尾气处理已略去)
ⅱ.向甲中加入适量浓
 ,一段时间后丙中溶液变为深棕色,丁中溶液无明显变化;
,一段时间后丙中溶液变为深棕色,丁中溶液无明显变化;ⅲ.关闭b、打开c,更换丙、丁中的溶液(试剂不变);
ⅳ.继续向甲中加入浓
 ,一段时间后观察到了与ⅱ相同的实验现象。
,一段时间后观察到了与ⅱ相同的实验现象。(3)通入
 的目的是
的目的是(4)铜与浓硝酸反应的离子方程式是
(5)装置乙的作用是
(6)实验结论:溶液的深棕色可能是因为 。
A. 与NO发生了反应 与NO发生了反应 | B. 与 与 发生了反应 发生了反应 |
C. 与NO发生了反应 与NO发生了反应 | D. 与 与 发生了反应 发生了反应 |
【反思与改进】
实验三:验证
 的还原性
的还原性(7)该小组同学依据实验二的结论改进了实验一,观察到了预期现象,其实验操作是向盛有
您最近一年使用:0次
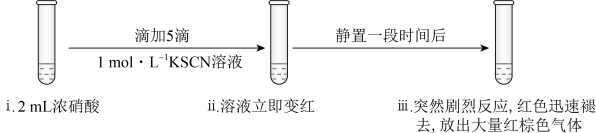
3 . 某同学研究浓硝酸的氧化性,做了如下实验:
资料:
i. 中
中 、
、 、
、 元素的化合价依次为:
元素的化合价依次为: 价、
价、 价、
价、 价。
价。
ii. 的性质类似卤素离子,能被氧化为黄色的
的性质类似卤素离子,能被氧化为黄色的 ,
, 可聚合为红色的
可聚合为红色的 。
。
(1)写出实验Ⅰ中铜和浓硝酸反应的离子方程式______ 。
(2)甲同学对实验Ⅱ中红色褪去的原因提出猜想,浓硝酸氧化了 ,其理论依据是
,其理论依据是______ 。
甲同学为证明猜想,做了如下实验Ⅲ
实验Ⅲ: 溶液,溶液立即变红是因为生成了
溶液,溶液立即变红是因为生成了______ (填化学式)。推测红棕色气体是______ (填化学式)。
(4)研究 的转化产物:
的转化产物:
实验Ⅳ:
a.将实验Ⅲ 中的气体通入
中的气体通入 和
和 的混合溶液中,有白色沉淀生成。
的混合溶液中,有白色沉淀生成。
b.过滤、洗涤白色沉淀,取少量于试管中,加入过量的稀硝酸,沉淀完全溶解,再滴加少量 溶液,不褪色。
溶液,不褪色。
c.另取少量实验Ⅲ中反应后的溶液,加入 溶液,产生大量白色沉淀。
溶液,产生大量白色沉淀。
①通过 证实了红棕色气体中不含
证实了红棕色气体中不含 ,证据是
,证据是______ 。
② 中,
中, 溶液中加入
溶液中加入 溶液以增大
溶液以增大 浓度的目的是
浓度的目的是______ 。
③由上述实验现象可知: 转化的最终产物中一定有
转化的最终产物中一定有______ 。
序号 | 实验Ⅰ | 实验Ⅱ |
操作 | 1:2 | 1:2 |
实验现象 | 铜片迅速溶解,产生大量红棕色气体,溶液变成绿色 | 滴入硝酸后,溶液变为红色,一段时间后,溶液褪为无色。 |
i.
 中
中 、
、 、
、 元素的化合价依次为:
元素的化合价依次为: 价、
价、 价、
价、 价。
价。ii.
 的性质类似卤素离子,能被氧化为黄色的
的性质类似卤素离子,能被氧化为黄色的 ,
, 可聚合为红色的
可聚合为红色的 。
。(1)写出实验Ⅰ中铜和浓硝酸反应的离子方程式
(2)甲同学对实验Ⅱ中红色褪去的原因提出猜想,浓硝酸氧化了
 ,其理论依据是
,其理论依据是甲同学为证明猜想,做了如下实验Ⅲ
实验Ⅲ:
 溶液,溶液立即变红是因为生成了
溶液,溶液立即变红是因为生成了(4)研究
 的转化产物:
的转化产物:实验Ⅳ:
a.将实验Ⅲ
 中的气体通入
中的气体通入 和
和 的混合溶液中,有白色沉淀生成。
的混合溶液中,有白色沉淀生成。b.过滤、洗涤白色沉淀,取少量于试管中,加入过量的稀硝酸,沉淀完全溶解,再滴加少量
 溶液,不褪色。
溶液,不褪色。c.另取少量实验Ⅲ中反应后的溶液,加入
 溶液,产生大量白色沉淀。
溶液,产生大量白色沉淀。①通过
 证实了红棕色气体中不含
证实了红棕色气体中不含 ,证据是
,证据是②
 中,
中, 溶液中加入
溶液中加入 溶液以增大
溶液以增大 浓度的目的是
浓度的目的是③由上述实验现象可知:
 转化的最终产物中一定有
转化的最终产物中一定有
您最近一年使用:0次
名校
4 . 实验室用下图装置(夹持装置已略去)制备 ,并研究其性质。其中,a、b为湿润的红色石蕊试纸。
,并研究其性质。其中,a、b为湿润的红色石蕊试纸。
 ,并研究其性质。其中,a、b为湿润的红色石蕊试纸。
,并研究其性质。其中,a、b为湿润的红色石蕊试纸。 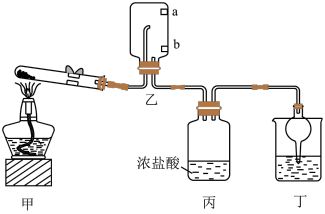
| A.装置乙中,a比b先变蓝 | B.装置丙中,产生大量白烟 |
| C.装置丁中,试剂只能是水 | D.装置丁具有防止倒吸的作用 |
您最近一年使用:0次
名校
解题方法
5 . 小组同学为探究 与可溶性钡的强酸盐能否反应生成
与可溶性钡的强酸盐能否反应生成 沉淀,用下图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验)。
沉淀,用下图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验)。
(1)A中反应的化学方程式是___________ 。
(2)C中白色沉淀是___________ ,该沉淀的生成表明 具有
具有___________ 性。
(3)分析B中不溶于稀盐酸的沉淀产生的原因,甲同学认为是空气参与反应,乙同学认为是白雾参与反应。
①为证实各自的观点,在原实验基础上:甲在原有操作之前增加一步操作,该操作是___________ ;乙在A、B间增加洗气瓶D,D中盛放的试剂是足量饱和 溶液,其目的是除去
溶液,其目的是除去___________ (写化学式)。
②进行实验,B中现象:
检验白色沉淀,发现均不溶于稀盐酸。分别用离子方程式解释白色沉淀产生的原因:___________ 。
(4)合并(3)中两同学的方案进行实验。B中无沉淀生成,而C中产生白色沉淀,由此得出的结论是___________ 。
 与可溶性钡的强酸盐能否反应生成
与可溶性钡的强酸盐能否反应生成 沉淀,用下图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验)。
沉淀,用下图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验)。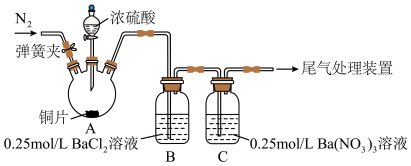
| 操作 | 现象 |
| 关闭弹簧夹,滴加一定量浓硫酸,加热 | A中有白雾生成,铜片表面产生气泡 B中有气泡冒出,产生大量白色沉淀 C中产生白色沉淀,液面上方略显浅红棕色并逐渐消失 |
打开弹簧夹,通入 ,停止加热,一段时间后关闭 ,停止加热,一段时间后关闭 | —— |
| 从B、C中分别取少量白色沉淀,加稀盐酸 | 均未发现白色沉淀溶解 |
(1)A中反应的化学方程式是
(2)C中白色沉淀是
 具有
具有(3)分析B中不溶于稀盐酸的沉淀产生的原因,甲同学认为是空气参与反应,乙同学认为是白雾参与反应。
①为证实各自的观点,在原实验基础上:甲在原有操作之前增加一步操作,该操作是
 溶液,其目的是除去
溶液,其目的是除去②进行实验,B中现象:
| 甲 | 大量白色沉淀 | 乙 | 少量白色沉淀 |
(4)合并(3)中两同学的方案进行实验。B中无沉淀生成,而C中产生白色沉淀,由此得出的结论是
您最近一年使用:0次
名校
解题方法
6 . 研究铜与硝酸的反应,实验如下(加持装置和尾气处理装置略)。
(1)实验Ⅰ产生红棕色气体的离子方程式是___________ 。实验Ⅱ产生红棕色气体的化学方程式是___________ 。
(2)对实验Ⅰ所得溶液呈绿色,而实验Ⅱ所得溶液呈蓝色的原因提出猜想。
查阅资料:i. 溶于浓硝酸后呈黄色;
溶于浓硝酸后呈黄色;
ii. 。
。 是弱酸,不稳定。
是弱酸,不稳定。
猜想一: 溶于浓硝酸,与蓝色
溶于浓硝酸,与蓝色 溶液混合而呈现绿色。
溶液混合而呈现绿色。
猜想二: 电离出的
电离出的 与
与 结合为
结合为 (绿色)。
(绿色)。
①向浓硝酸中通入 ,现象是
,现象是___________ ,滴加少量蓝色 溶液后呈绿色,证实猜想一合理。
溶液后呈绿色,证实猜想一合理。
②研究猜想二是否为实验Ⅰ所得溶液呈绿色的主要原因,实验如下。 的证据是
的证据是___________ 。
Ⅱ.向溶液B中滴加少量硝酸,溶液由绿色变为蓝色。结果表明,猜想二不是实验Ⅰ所得溶液呈绿色的主要原因,说明理由:___________ 。
| 装置 | 编号 | 试剂a | 现象 |
| Ⅰ | 4mL浓硝酸(过量) | 铜片完全溶解,溶液变绿,出现大量红棕色气体。 |
| Ⅱ | 4mL稀硝酸(过量) | 铜片完全溶解,溶液变蓝,液面上方气体呈浅红棕色。 |
(1)实验Ⅰ产生红棕色气体的离子方程式是
(2)对实验Ⅰ所得溶液呈绿色,而实验Ⅱ所得溶液呈蓝色的原因提出猜想。
查阅资料:i.
 溶于浓硝酸后呈黄色;
溶于浓硝酸后呈黄色;ii.
 。
。 是弱酸,不稳定。
是弱酸,不稳定。猜想一:
 溶于浓硝酸,与蓝色
溶于浓硝酸,与蓝色 溶液混合而呈现绿色。
溶液混合而呈现绿色。猜想二:
 电离出的
电离出的 与
与 结合为
结合为 (绿色)。
(绿色)。①向浓硝酸中通入
 ,现象是
,现象是 溶液后呈绿色,证实猜想一合理。
溶液后呈绿色,证实猜想一合理。②研究猜想二是否为实验Ⅰ所得溶液呈绿色的主要原因,实验如下。

 的证据是
的证据是Ⅱ.向溶液B中滴加少量硝酸,溶液由绿色变为蓝色。结果表明,猜想二不是实验Ⅰ所得溶液呈绿色的主要原因,说明理由:
您最近一年使用:0次
名校
解题方法
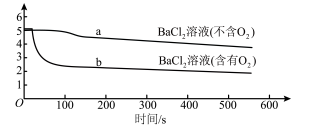
7 . 分别向等体积的不含O2、含有O2的0.1mol/L BaCl2溶液中通入SO2,探究体系中物质间的相互作用,实验记录如下。(已知:pH越小,溶液酸性越强)
下列说法不正确的是
下列说法不正确的是
pH变化 |
|
溶液中是否产生沉淀 | 不含O2的BaCl2溶液中没有白色沉淀, 含有O2的BaCl2溶液中产生白色沉淀。 |
| A.a所示溶液的pH降低的原因:SO2与H2O反应生成H2SO3,溶液的c(H+)增大 |
B.b所示溶液中发生反应: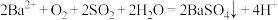 |
| C. SO2通入不含O2的BaCl2溶液后,再加入NaOH溶液,产生BaSO3沉淀 |
D.b比a所示溶液的pH小的原因: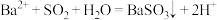 |
您最近一年使用:0次
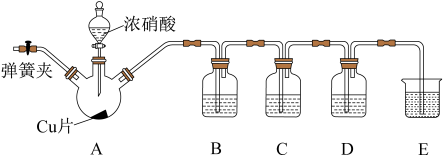
8 . 某小组通过实验探究NO的某些性质,实验装置图如下:___________ 。
(2)判断NO既有氧化性又有还原性的理论依据是___________ 。
资料:i.NO与 溶液会发生氧化还原反应,NO被还原为
溶液会发生氧化还原反应,NO被还原为 。
。
ii.醋酸银易溶于水,硫酸银微溶于水, 是不溶于水的黄色固体。
是不溶于水的黄色固体。
iii.浓硝酸能将NO氧化成 ,而稀硝酸不能氧化NO。
,而稀硝酸不能氧化NO。
iv.NaOH溶液不与NO反应,能与 反应:
反应: 。
。
可选药品: 溶液、浓
溶液、浓 、3mo/L稀
、3mo/L稀 、蒸馏水、浓
、蒸馏水、浓 、NaOH溶液及
、NaOH溶液及 。
。
(3)滴加浓硝酸之前的操作是检验装置的气密性,加入药品,打开弹簧夹后,通入一段时间 ,关闭弹簧夹,其目的是
,关闭弹簧夹,其目的是___________ 。
(4)装置B的作用是___________ (用化学方程式表示)。
(5)装置C中装有 溶液,实验探究NO的氧化性。
溶液,实验探究NO的氧化性。
①甲同学检验 的转化产物。取少量反应后装置C中的溶液,
的转化产物。取少量反应后装置C中的溶液,___________ (填操作和实验现象)。
②乙同学认为即使甲同学检验出有 ,也不能说明NO具有氧化性,理由是
,也不能说明NO具有氧化性,理由是___________ (用离子方程式说明)。
③丙同学认为,需通过进一步实验验证NO的氧化性,补充以下实验:
实验I:取饱和 溶液,加入少量醋酸,再滴加5滴0.1mol/L的
溶液,加入少量醋酸,再滴加5滴0.1mol/L的 溶液,无明显变化。
溶液,无明显变化。
实验Ⅱ:取少量装置C中反应后的溶液,加入少量醋酸,再滴加5滴0.1mol/L的 溶液,
溶液,___________ (填实验现象)。
实验I的目的是___________ 。
上述实验证明NO有氧化性。
(6)实验探究NO的还原性。
装置D中,实验得出NO具有还原性的实验现象是___________ 。
(7)装置E的作用是___________ 。
(2)判断NO既有氧化性又有还原性的理论依据是
资料:i.NO与
 溶液会发生氧化还原反应,NO被还原为
溶液会发生氧化还原反应,NO被还原为 。
。ii.醋酸银易溶于水,硫酸银微溶于水,
 是不溶于水的黄色固体。
是不溶于水的黄色固体。iii.浓硝酸能将NO氧化成
 ,而稀硝酸不能氧化NO。
,而稀硝酸不能氧化NO。iv.NaOH溶液不与NO反应,能与
 反应:
反应: 。
。可选药品:
 溶液、浓
溶液、浓 、3mo/L稀
、3mo/L稀 、蒸馏水、浓
、蒸馏水、浓 、NaOH溶液及
、NaOH溶液及 。
。(3)滴加浓硝酸之前的操作是检验装置的气密性,加入药品,打开弹簧夹后,通入一段时间
 ,关闭弹簧夹,其目的是
,关闭弹簧夹,其目的是(4)装置B的作用是
(5)装置C中装有
 溶液,实验探究NO的氧化性。
溶液,实验探究NO的氧化性。①甲同学检验
 的转化产物。取少量反应后装置C中的溶液,
的转化产物。取少量反应后装置C中的溶液,②乙同学认为即使甲同学检验出有
 ,也不能说明NO具有氧化性,理由是
,也不能说明NO具有氧化性,理由是③丙同学认为,需通过进一步实验验证NO的氧化性,补充以下实验:
实验I:取饱和
 溶液,加入少量醋酸,再滴加5滴0.1mol/L的
溶液,加入少量醋酸,再滴加5滴0.1mol/L的 溶液,无明显变化。
溶液,无明显变化。实验Ⅱ:取少量装置C中反应后的溶液,加入少量醋酸,再滴加5滴0.1mol/L的
 溶液,
溶液,实验I的目的是
上述实验证明NO有氧化性。
(6)实验探究NO的还原性。
装置D中,实验得出NO具有还原性的实验现象是
(7)装置E的作用是
您最近一年使用:0次
名校
解题方法
9 . 某小组同学探究不同条件下氯气与二价锰化合物的反应
资料:i. 在一定条件下被
在一定条件下被 或
或 氧化成
氧化成 (棕黑色)、
(棕黑色)、 (绿色)、
(绿色)、 (紫色)。
(紫色)。
ii.浓碱条件下, 可被
可被 还原为
还原为 。
。
iii. 的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
实验装置如图(夹持装置略)
(1)B中试剂是___________ 。
(2)通入 前,II、III中沉淀由白色
前,II、III中沉淀由白色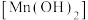 变为棕黑色,补全发生反应的化学方程式:
变为棕黑色,补全发生反应的化学方程式:___________ 。

(3)对比实验I、II通入 后的实验现象,对于二价锰化合物还原性的认识是:
后的实验现象,对于二价锰化合物还原性的认识是:
①___________ ;
②在碱性条件下二价锰可以被氧化到更高价态。
(4)根据资料ii,II中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入 导致溶液的碱性减弱。
导致溶液的碱性减弱。
原因二:可能是氧化剂过量,氧化剂将 氧化为
氧化为 。
。
①用化学方程式表示可能导致溶液碱性减弱的原因___________ ,但通过实验测定,溶液的碱性变化很小。
②针对原因二小组同学做如下探究:
IV中溶液紫色迅速变为绿色的离子方程式为___________ ,溶液绿色缓慢加深,原因是 被
被___________ (填“化学式”)氧化,可证明III的悬浊液中氧化剂过量。
③分析IV、V实验现象不同的原因是___________ 。
资料:i.
 在一定条件下被
在一定条件下被 或
或 氧化成
氧化成 (棕黑色)、
(棕黑色)、 (绿色)、
(绿色)、 (紫色)。
(紫色)。ii.浓碱条件下,
 可被
可被 还原为
还原为 。
。iii.
 的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。实验装置如图(夹持装置略)

| 序号 | I | II | III |
| 物质a | 水 | 5%NaOH溶液 | 40%NaOH溶液 |
通入 前C中实验现象 前C中实验现象 | 得到无色溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 |
通入 后C中实验现象 后C中实验现象 | 产生棕黑色沉淀,且放置后不发生变化 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
(1)B中试剂是
(2)通入
 前,II、III中沉淀由白色
前,II、III中沉淀由白色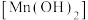 变为棕黑色,补全发生反应的化学方程式:
变为棕黑色,补全发生反应的化学方程式:
(3)对比实验I、II通入
 后的实验现象,对于二价锰化合物还原性的认识是:
后的实验现象,对于二价锰化合物还原性的认识是:①
②在碱性条件下二价锰可以被氧化到更高价态。
(4)根据资料ii,II中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入
 导致溶液的碱性减弱。
导致溶液的碱性减弱。原因二:可能是氧化剂过量,氧化剂将
 氧化为
氧化为 。
。①用化学方程式表示可能导致溶液碱性减弱的原因
②针对原因二小组同学做如下探究:
| 序号 | IV | V |
| 操作 | 取III中放置后的1mL悬浊液,加入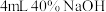 溶液 溶液 | 取III中放置后的1mL悬浊液,加入4mL水 |
| 现象 | 溶液紫色迅速变为绿色,且绿色缓慢加深 | 溶液紫色缓慢加深 |
 被
被③分析IV、V实验现象不同的原因是
您最近一年使用:0次
名校
解题方法
10 . 某同学进行如下实验:
下列说法不正确 的是。
实验步骤 | 实验现象 | |
Ⅰ | 将 固体加入试管中,并将湿润的pH试纸置于试管口,试管口略向下倾斜,对试管底部进行加热 固体加入试管中,并将湿润的pH试纸置于试管口,试管口略向下倾斜,对试管底部进行加热 | 试纸颜色变化:黄色→蓝色 →黄色→红色 →黄色→红色 ;试管中部有白色固体附着 ;试管中部有白色固体附着 |
Ⅱ | 将饱和 溶液滴在pH试纸上 溶液滴在pH试纸上 | 试纸颜色变化:黄色→橙黄色 |
A.根据Ⅰ中试纸变蓝,说明 发生了分解反应 发生了分解反应 |
| B.根据Ⅰ中试纸颜色变化,说明氨气比氯化氢气体扩散速率快 |
C.Ⅰ中试纸变成红色,是由 造成的 造成的 |
D.该实验现象说明可以用加热 的方法制备 的方法制备 |
您最近一年使用:0次