1 . 磺酰氯 是重要的有机合成试剂,实验室可利用
是重要的有机合成试剂,实验室可利用 与
与 在活性炭作用下反应制取少量
在活性炭作用下反应制取少量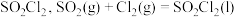 ,该反应放热,装置如图所示(部分夹持装置省略)。已知
,该反应放热,装置如图所示(部分夹持装置省略)。已知 的熔点为
的熔点为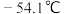 ,沸点为
,沸点为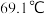 ,遇水能发生剧烈的水解反应,并产生白雾。
,遇水能发生剧烈的水解反应,并产生白雾。
回答下列问题。 ,则下列试剂组合中合适的是___________。
,则下列试剂组合中合适的是___________。
(2)导管a的作用是___________ ;仪器b中的试剂是___________ 。
(3)实验结束时,关闭分液漏斗活塞和止水夹k,此时装置戊的作用是___________ 。
(4) 遇水发生反应生成两种酸,该反应的化学方程式为
遇水发生反应生成两种酸,该反应的化学方程式为___________ 。
(5)若反应中消耗的氯气体积为 (标准状况下),最后经过分离提纯得到
(标准状况下),最后经过分离提纯得到 纯净的磺酰氯,则磺酰氯的产率为
纯净的磺酰氯,则磺酰氯的产率为___________ (产率:实际产量/理论产量 )。
)。
(6)已知酸性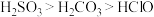 ,借助该酸性排序,使用以下装置设计实验证明
,借助该酸性排序,使用以下装置设计实验证明 的酸性强于
的酸性强于 ,其连接顺序应为
,其连接顺序应为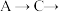
___________ 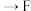 ;能证明
;能证明 的酸性强于
的酸性强于 的实验现象为
的实验现象为___________ 。
 是重要的有机合成试剂,实验室可利用
是重要的有机合成试剂,实验室可利用 与
与 在活性炭作用下反应制取少量
在活性炭作用下反应制取少量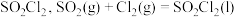 ,该反应放热,装置如图所示(部分夹持装置省略)。已知
,该反应放热,装置如图所示(部分夹持装置省略)。已知 的熔点为
的熔点为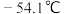 ,沸点为
,沸点为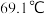 ,遇水能发生剧烈的水解反应,并产生白雾。
,遇水能发生剧烈的水解反应,并产生白雾。回答下列问题。

 ,则下列试剂组合中合适的是___________。
,则下列试剂组合中合适的是___________。A. 的硫酸和 的硫酸和 | B. 的硝酸和 的硝酸和 固体 固体 |
C. 的硫酸和 的硫酸和 固体 固体 | D. 的硫酸和 的硫酸和 固体 固体 |
(2)导管a的作用是
(3)实验结束时,关闭分液漏斗活塞和止水夹k,此时装置戊的作用是
(4)
 遇水发生反应生成两种酸,该反应的化学方程式为
遇水发生反应生成两种酸,该反应的化学方程式为(5)若反应中消耗的氯气体积为
 (标准状况下),最后经过分离提纯得到
(标准状况下),最后经过分离提纯得到 纯净的磺酰氯,则磺酰氯的产率为
纯净的磺酰氯,则磺酰氯的产率为 )。
)。(6)已知酸性
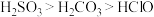 ,借助该酸性排序,使用以下装置设计实验证明
,借助该酸性排序,使用以下装置设计实验证明 的酸性强于
的酸性强于 ,其连接顺序应为
,其连接顺序应为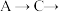
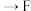 ;能证明
;能证明 的酸性强于
的酸性强于 的实验现象为
的实验现象为
您最近一年使用:0次
2024-02-23更新
|
160次组卷
|
2卷引用:广东省深圳实验学校高中部2023-2024学年高一上学期第三阶段考试化学试题
解题方法
2 . 某小组探究SO2的漂白原理及铜和浓硫酸反应的最低浓度,装置如图所示,部分装置省略。实验发现,装置B中溶液变红色,不褪色;装置C中溶液为红色,装置D中溶液褪色。向烧瓶中加入200mL18.4mol/L浓硫酸,充分反应直至装置A中反应停止。
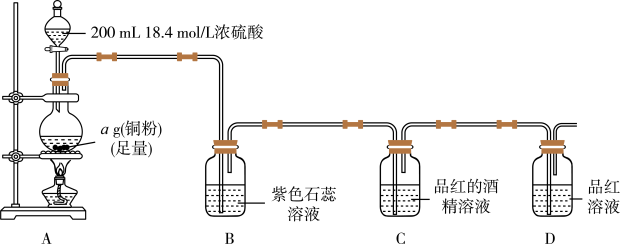
回答下列问题:
(1)装置A中发生反应的化学方程式为_______ 。
(2)根据装置C、D中出现的现象,对漂白品红的粒子提出如下猜想:
猜想1:H2SO3;猜想2:HSO ;猜想3:
;猜想3:_______ 。
针对猜想2设计简单实验探究漂白原理:_______ 。
(3)实验完毕后,甲同学设计如下实验测定剩余硫酸浓度(不考虑体积变化,假设锌与稀硫酸反应只产生氢气):

①实验部分操作:(a)调平量气管和烧杯的液面;(b)冷却至室温;(c)读数。
正确的先后操作顺序是_______ (填字母)。
②已知开始时量气管读数为V1mL,最终读数为V2mL(均折合成标准状况)。
则铜与浓硫酸发生反应的最低硫酸浓度为_______ mol/L。
(4)乙同学分析上述实验后,设计如下实验方案:
方案1:过滤、洗涤、低温干燥,称过量铜粉的质量(不考虑副产物)。
方案2:取25mL残留溶液,滴加甲基橙作指示剂,用标准NaOH溶液滴定H2SO4。
丙同学分析上述方案,认为方案_______ (填“1”或“2”)可行。请你帮丙同学分析不可行方案的理由:_______ 。
(5)丁同学采用滴定法测定硫酸最低浓度。取烧杯中剩余混合液20.00mL于锥形瓶中,滴加指示剂,用cmol/L标准EDTA(用Na4Y表示)溶液滴定至终点时消耗滴定液xmL。
已知:滴定反应为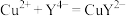 。
。
该浓硫酸的最低浓度为_______ mol/L。若滴定管没有用EDTA溶液润洗,测得结果_______ (填“偏高”“偏低”或“无影响”)。

回答下列问题:
(1)装置A中发生反应的化学方程式为
(2)根据装置C、D中出现的现象,对漂白品红的粒子提出如下猜想:
猜想1:H2SO3;猜想2:HSO
 ;猜想3:
;猜想3:针对猜想2设计简单实验探究漂白原理:
(3)实验完毕后,甲同学设计如下实验测定剩余硫酸浓度(不考虑体积变化,假设锌与稀硫酸反应只产生氢气):

①实验部分操作:(a)调平量气管和烧杯的液面;(b)冷却至室温;(c)读数。
正确的先后操作顺序是
②已知开始时量气管读数为V1mL,最终读数为V2mL(均折合成标准状况)。
则铜与浓硫酸发生反应的最低硫酸浓度为
(4)乙同学分析上述实验后,设计如下实验方案:
方案1:过滤、洗涤、低温干燥,称过量铜粉的质量(不考虑副产物)。
方案2:取25mL残留溶液,滴加甲基橙作指示剂,用标准NaOH溶液滴定H2SO4。
丙同学分析上述方案,认为方案
(5)丁同学采用滴定法测定硫酸最低浓度。取烧杯中剩余混合液20.00mL于锥形瓶中,滴加指示剂,用cmol/L标准EDTA(用Na4Y表示)溶液滴定至终点时消耗滴定液xmL。
已知:滴定反应为
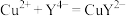 。
。该浓硫酸的最低浓度为
您最近一年使用:0次
2022-12-23更新
|
208次组卷
|
3卷引用: 河南省湘豫名校联考2022-2023学年高三上学期12月期末摸底考试化学试题
河南省湘豫名校联考2022-2023学年高三上学期12月期末摸底考试化学试题 (已下线)河南省湘豫名校联考2022-2023学年高三上学期12月期末摸底考试变式汇编(17-21)河南省郑州市等3地2022-2023学年高三上学期12月月考化学试题
名校
解题方法
3 . 某兴趣小组同学们对SO2的性质进行探究。
实验一:探究SO2的漂白原理,装置如图所示,部分装置省略。实验发现,装置B中溶液变红色,不褪色;装置C中溶液为红色,装置D中溶液褪色。向烧瓶中加入200mL18.4mol/L浓硫酸,充分反应直至装置A中反应停止。
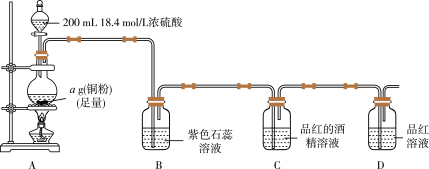
回答下列问题:
(1)装置A中发生反应的化学方程式为_______ 。
(2)根据装置C、D中出现的现象,对漂白品红的粒子提出如下猜想:
猜想1:H2SO3;
猜想2:HSO ;
;
猜想3:_______ 。
针对猜想2设计简单实验探究漂白原理:_______ 。
(3)实验完毕后,甲同学设计如下实验测定剩余硫酸浓度(不考虑体积变化,假设锌与稀硫酸反应只产生氢气):

①实验部分操作:(a)调平量气管和烧杯的液面;(b)冷却至室温;(c)读数正确的先后操作顺序是_______ (填字母)。
②已知开始时量气管读数为V1mL,最终读数为V2mL(均折合成标准状况,且V2>V1)。则铜与浓硫酸发生反应的最低硫酸浓度为_______ mol/L。
实验二:结合实验一的装置,乙同学添加一些装置(如图),利用SO2和Cl2在活性炭催化作用下制取亚硫酰氯SOCl2。亚硫酰氯是重要的化工试剂,沸点较低,易水解。
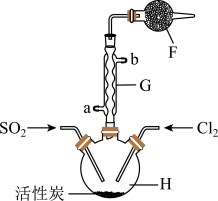
(4)①G仪器的进水口是_______ (填“a”或“b”),其作用是_______ 。
②F仪器的作用是_______ 。
(5)已知SOCl2具有还原性,其氧化产物为SO 。丙同学为了验证SOCl2和FeCl3·6H2O能发生氧化还原反应,做以下实验:取少量SOCl2和FeCl3·6H2O反应后的混合物于试管中,加水充分溶解后……接下来的实验操作和现象都正确的是_______(填字母序号)。
。丙同学为了验证SOCl2和FeCl3·6H2O能发生氧化还原反应,做以下实验:取少量SOCl2和FeCl3·6H2O反应后的混合物于试管中,加水充分溶解后……接下来的实验操作和现象都正确的是_______(填字母序号)。
实验一:探究SO2的漂白原理,装置如图所示,部分装置省略。实验发现,装置B中溶液变红色,不褪色;装置C中溶液为红色,装置D中溶液褪色。向烧瓶中加入200mL18.4mol/L浓硫酸,充分反应直至装置A中反应停止。

回答下列问题:
(1)装置A中发生反应的化学方程式为
(2)根据装置C、D中出现的现象,对漂白品红的粒子提出如下猜想:
猜想1:H2SO3;
猜想2:HSO
 ;
;猜想3:
针对猜想2设计简单实验探究漂白原理:
(3)实验完毕后,甲同学设计如下实验测定剩余硫酸浓度(不考虑体积变化,假设锌与稀硫酸反应只产生氢气):

①实验部分操作:(a)调平量气管和烧杯的液面;(b)冷却至室温;(c)读数正确的先后操作顺序是
②已知开始时量气管读数为V1mL,最终读数为V2mL(均折合成标准状况,且V2>V1)。则铜与浓硫酸发生反应的最低硫酸浓度为
实验二:结合实验一的装置,乙同学添加一些装置(如图),利用SO2和Cl2在活性炭催化作用下制取亚硫酰氯SOCl2。亚硫酰氯是重要的化工试剂,沸点较低,易水解。

(4)①G仪器的进水口是
②F仪器的作用是
(5)已知SOCl2具有还原性,其氧化产物为SO
 。丙同学为了验证SOCl2和FeCl3·6H2O能发生氧化还原反应,做以下实验:取少量SOCl2和FeCl3·6H2O反应后的混合物于试管中,加水充分溶解后……接下来的实验操作和现象都正确的是_______(填字母序号)。
。丙同学为了验证SOCl2和FeCl3·6H2O能发生氧化还原反应,做以下实验:取少量SOCl2和FeCl3·6H2O反应后的混合物于试管中,加水充分溶解后……接下来的实验操作和现象都正确的是_______(填字母序号)。| A.滴加几滴KSCN溶液,溶液变为红色 |
| B.滴加几滴BaCl2溶液,有白色沉淀生成 |
| C.加入少量稀硝酸,再滴加几滴BaCl2溶液,有白色沉淀生成 |
| D.滴加几滴酸性KMnO4溶液,紫红色消失 |
您最近一年使用:0次
4 . 制备乙酸乙酯是中学有机化学中的一个重要实验。某化学学习小组的同学查阅资料发现,某些无机盐类也可以催化乙酸乙酯的合成,为了探究不同盐的催化效果,设计了如下实验:
实验步骤:向大试管中加入一定量的无机盐催化剂,再加入3 mL无水乙醇和2 mL冰醋酸,按图连接装置。用酒精灯小心均匀地加热试管5 min,产生的蒸气经导管通到饱和碳酸钠溶液上方。
实验记录:使用不同的催化剂,实验得到的酯层高度如下表。

(1)实验时,需要加入几粒沸石,目的是________________ 。
(2)催化剂用量为3 mmol(以阳离子计),选用的催化剂A可能是_____ (填标号)。
a. 氯化铜晶体 b. 硫酸钙晶体 c. 碳酸钠晶体 d. 硝酸钾晶体
实验所用四种催化剂中,制备乙酸乙酯最好选用________ 。
(3)若用18O标记乙醇中的O,用氯化铝作催化剂时,产生乙酸乙酯的化学方程式为________ 。
(4)实验中用饱和碳酸钠溶液的作用是__________ 。得到的混合液经_________ ,蒸馏,最终得到较纯净的乙酸乙酯。
实验步骤:向大试管中加入一定量的无机盐催化剂,再加入3 mL无水乙醇和2 mL冰醋酸,按图连接装置。用酒精灯小心均匀地加热试管5 min,产生的蒸气经导管通到饱和碳酸钠溶液上方。
实验记录:使用不同的催化剂,实验得到的酯层高度如下表。

| 催化剂 | 酯层高度/cm | 催化剂 | 酯层高度/cm |
| 氯化铁晶体 | 2.7 | 氯化铝 | 3.2 |
| A | 2.2 | 氯化钠 | 0.0 |
(2)催化剂用量为3 mmol(以阳离子计),选用的催化剂A可能是
a. 氯化铜晶体 b. 硫酸钙晶体 c. 碳酸钠晶体 d. 硝酸钾晶体
实验所用四种催化剂中,制备乙酸乙酯最好选用
(3)若用18O标记乙醇中的O,用氯化铝作催化剂时,产生乙酸乙酯的化学方程式为
(4)实验中用饱和碳酸钠溶液的作用是
您最近一年使用:0次
5 . 某研究性学习小组在做Cu 和浓HNO3、稀HNO3反应时,发现生成溶液的颜色有差别。Cu和浓HNO3反应后的溶液为鲜艳草绿色,而Cu和稀HNO3反应溶液为蓝色。
(1)写出Cu和浓HNO3反应的化学方程式:______ 。
(2)该研究性小组成员对反应后生成的溶液颜色差别进行了实验探究。
甲同学认为:绿色是硝酸铜溶液浓度较大引起的,即Cu(NO3)2浓溶液显绿色,Cu(NO3)2稀溶液显蓝色。
乙同学认为:绿色是NO2溶于Cu2+溶液引起的。
①甲同学用Cu(NO3)2晶体配制成稀溶液,溶液为浅蓝色,随着Cu(NO3)2固体的加入,最终配成饱和溶液,颜色逐渐变深,但始终是蓝色。该现象可证明甲同学推测______ (填“合理”或“不合理”)。
②乙同学将Cu与浓HNO3反应后的绿色溶液稍微加热,放出大量红棕色气体,溶液变为______ 色,证明乙同学推测可能成立。
③乙同学设计实验进一步探究,向不同浓度的铜盐溶液中通入NO2气体,实验数据和实验现象如下表:
不同浓度铜盐溶液中通入NO2气体的现象
对比实验1和2,或对比实验3和4,可以得到结论______ 。对比铜与浓硝酸的反应,生成的部分NO2 也会溶入溶液,使溶液呈现绿色。说明“反应混合液”呈绿色确实与NO2气体溶解有关。
(3)丙同学查阅文献:浓硝酸和铜的反应因为有亚硝酸(HNO2)生成,进而可以和Cu2+ 结合成亚硝酸化合物,而铜的亚硝酸化合物是绿色的。
①丙同学设计实验验证生成了亚硝酸(HNO2),取一支试管加入浓硝酸1 mL,插入铜丝后,快速反应,有红棕色气体放出,溶液为绿色;然后加入3滴30%的H2O2溶液,振荡后溶液变为蓝色。分析原因是H2O2和反应过程中生成的HNO2发生了氧化还原反应,写出H2O2和HNO2反应的化学方程式:______ 。
②丙同学继续设计实验验证。取1 mol/LCu(NO3)2溶液2 mL,加入1 mol/L的NaNO2溶液3滴,观察溶液变为绿色,再加入3滴30%H2O2和1滴浓硝酸。溶液很快由绿色变为蓝色。由此可以得到Cu和浓HNO3反应后的溶液为绿色的原因是:______ 。
(1)写出Cu和浓HNO3反应的化学方程式:
(2)该研究性小组成员对反应后生成的溶液颜色差别进行了实验探究。
甲同学认为:绿色是硝酸铜溶液浓度较大引起的,即Cu(NO3)2浓溶液显绿色,Cu(NO3)2稀溶液显蓝色。
乙同学认为:绿色是NO2溶于Cu2+溶液引起的。
①甲同学用Cu(NO3)2晶体配制成稀溶液,溶液为浅蓝色,随着Cu(NO3)2固体的加入,最终配成饱和溶液,颜色逐渐变深,但始终是蓝色。该现象可证明甲同学推测
②乙同学将Cu与浓HNO3反应后的绿色溶液稍微加热,放出大量红棕色气体,溶液变为
③乙同学设计实验进一步探究,向不同浓度的铜盐溶液中通入NO2气体,实验数据和实验现象如下表:
不同浓度铜盐溶液中通入NO2气体的现象
| 实验编号 | ① | ② | ③ | ④ |
| 饱和Cu(NO3)2溶液体积/mL | 2 | 1 | 0 | 0 |
| 蒸馏水体积/mL | 0 | 1 | 0 | 1 |
| 饱和CuSO4溶液体积/mL | 0 | 0 | 2 | 1 |
| 现象 | 蓝绿色 | 蓝绿色 | 绿色 | 绿色 |
(3)丙同学查阅文献:浓硝酸和铜的反应因为有亚硝酸(HNO2)生成,进而可以和Cu2+ 结合成亚硝酸化合物,而铜的亚硝酸化合物是绿色的。
①丙同学设计实验验证生成了亚硝酸(HNO2),取一支试管加入浓硝酸1 mL,插入铜丝后,快速反应,有红棕色气体放出,溶液为绿色;然后加入3滴30%的H2O2溶液,振荡后溶液变为蓝色。分析原因是H2O2和反应过程中生成的HNO2发生了氧化还原反应,写出H2O2和HNO2反应的化学方程式:
②丙同学继续设计实验验证。取1 mol/LCu(NO3)2溶液2 mL,加入1 mol/L的NaNO2溶液3滴,观察溶液变为绿色,再加入3滴30%H2O2和1滴浓硝酸。溶液很快由绿色变为蓝色。由此可以得到Cu和浓HNO3反应后的溶液为绿色的原因是:
您最近一年使用:0次
2021-02-27更新
|
590次组卷
|
2卷引用:北京市房山区2020-2021学年高一上学期期末考试化学试题
6 . 某化学活动小组进行如下实验探究活动。
Ⅰ.甲组同学用如图所示装置制备氨气
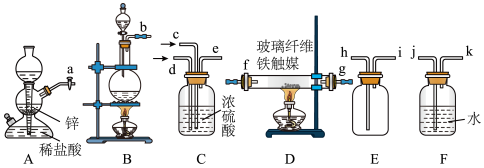
已知:加热NH4Cl和NaNO2饱和溶液可以制取N2,缓慢通入原料气有利于D中合成氨气。
(1)图示装置从左到右正确的连接顺序(填接口字母)
 →e→f→g→
→e→f→g→____ →____ →____ →____ 。
(2)写出B中制取N2的反应的离子方程式__________
(3)装置C的作用:干燥气体、_______________ 、_____________ 。
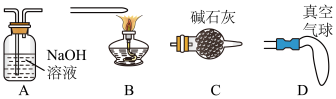
(4)小组经过讨论认为尾气逸出存在安全隐患,可以采用下列哪种方法处理____ (填选项字母)。
Ⅱ.乙组同学查阅资料:制取氮气用的亚硝酸钠外观与食盐相似,毒性较强。可以用如下装置(略去部分夹持仪器)制备。
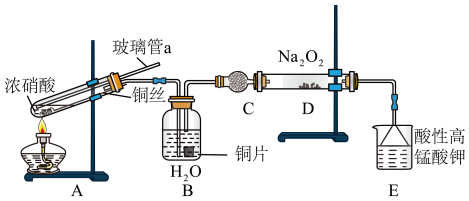
已知:①2NO+Na2O2=2NaNO2;
②酸性条件下,NO和NO2都能与MnO 反应生成NO
反应生成NO 和Mn2+。
和Mn2+。
(5)仪器C的名称为______ ,A中与碎铜片比较使用铜丝的优点_______________ 。
(6)实验结束后还可以通入空气把残存气体排入后面装置吸收,防止污染大气。NO在E中发生反应的离子方程式为_____________ 。
Ⅰ.甲组同学用如图所示装置制备氨气

已知:加热NH4Cl和NaNO2饱和溶液可以制取N2,缓慢通入原料气有利于D中合成氨气。
(1)图示装置从左到右正确的连接顺序(填接口字母)
 →e→f→g→
→e→f→g→(2)写出B中制取N2的反应的离子方程式
(3)装置C的作用:干燥气体、
(4)小组经过讨论认为尾气逸出存在安全隐患,可以采用下列哪种方法处理

Ⅱ.乙组同学查阅资料:制取氮气用的亚硝酸钠外观与食盐相似,毒性较强。可以用如下装置(略去部分夹持仪器)制备。

已知:①2NO+Na2O2=2NaNO2;
②酸性条件下,NO和NO2都能与MnO
 反应生成NO
反应生成NO 和Mn2+。
和Mn2+。(5)仪器C的名称为
(6)实验结束后还可以通入空气把残存气体排入后面装置吸收,防止污染大气。NO在E中发生反应的离子方程式为
您最近一年使用:0次
2020-11-30更新
|
297次组卷
|
2卷引用:河北省石家庄市辛集市2022-2023学年高一下学期7月期末考试化学试题
7 . 某实验小组对KSCN的性质进行探究,设计如下实验:
(1)SCN-存在两种结构式,分别为N≡C—S-和S=C=N-,SCN-是二者的互变异构的混合物,请写出N≡C—S-的电子式__________ 。
(2)用离子方程式表示FeSO4溶液显酸性的原因__________ 。
(3)①用离子方程式表示实验Ⅰ溶液变红的原因____________________________ 。
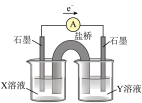
②针对实验Ⅰ中红色褪去的原因,小组同学认为是SCN-被酸性KMnO4氧化为SO42-,并设计如如图实验装置证实了猜想是成立的。其中X溶液是_______ ,Y溶液是_______ ,检验产物SO42-的操作及现象是_____________ 。
(4)针对实验Ⅱ“红色明显变浅”的现象,实验小组进行探究。
甲同学查资料得知:当加入强电解质后,增大了离子间相互作用,离子之间牵制作用增强,即“盐效应”。“盐效应”使Fe3++SCN- [Fe(SCN)]2+平衡体系中的Fe3+跟SCN-结合成[Fe(SCN)]2+的机会减少,溶液红色变浅。
[Fe(SCN)]2+平衡体系中的Fe3+跟SCN-结合成[Fe(SCN)]2+的机会减少,溶液红色变浅。
乙同学认为SCN-可以与Fe2+反应生成无色络合离子,进一步使Fe3++SCN-⇌[Fe(SCN)]2+平衡左移,红色明显变浅,而Mg2+与SCN-难络合,于是乙设计了如下实验:
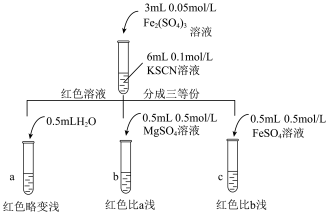
由此推测,实验Ⅱ“红色明显变浅”的原因是___________________ 。
(5)工业上测定钛铁合金中钛含量的其中一步反应原理是:以KSCN为指示剂,用NH4Fe(SO4)2标准溶液滴定Ti(Ⅲ),反应的化学方程式为:Ti2(SO4)3+2NH4Fe(SO4)2===2Ti(SO4)2+(NH4)2SO4+2FeSO4,则达到滴定终点的实验现象是______ 。
| 试管中试剂 | 实验 | 滴加试剂 | 现象 |
 | Ⅰ | ⅰ.先加1mL 0.1 mol/L FeSO4溶液 ⅱ.再加硫酸酸化的KMnO4溶液 | ⅰ.无明显现象 ⅱ.先变红,后褪色 |
| Ⅱ | ⅲ.先加1mL 0.05 mol/L Fe2(SO4)3溶液 ⅳ.再滴加0.5 mL 0.5 mol/L FeSO4溶液 | ⅲ.溶液变红 ⅳ.红色明显变浅 |
(1)SCN-存在两种结构式,分别为N≡C—S-和S=C=N-,SCN-是二者的互变异构的混合物,请写出N≡C—S-的电子式
(2)用离子方程式表示FeSO4溶液显酸性的原因
(3)①用离子方程式表示实验Ⅰ溶液变红的原因

②针对实验Ⅰ中红色褪去的原因,小组同学认为是SCN-被酸性KMnO4氧化为SO42-,并设计如如图实验装置证实了猜想是成立的。其中X溶液是
(4)针对实验Ⅱ“红色明显变浅”的现象,实验小组进行探究。
甲同学查资料得知:当加入强电解质后,增大了离子间相互作用,离子之间牵制作用增强,即“盐效应”。“盐效应”使Fe3++SCN-
 [Fe(SCN)]2+平衡体系中的Fe3+跟SCN-结合成[Fe(SCN)]2+的机会减少,溶液红色变浅。
[Fe(SCN)]2+平衡体系中的Fe3+跟SCN-结合成[Fe(SCN)]2+的机会减少,溶液红色变浅。乙同学认为SCN-可以与Fe2+反应生成无色络合离子,进一步使Fe3++SCN-⇌[Fe(SCN)]2+平衡左移,红色明显变浅,而Mg2+与SCN-难络合,于是乙设计了如下实验:

由此推测,实验Ⅱ“红色明显变浅”的原因是
(5)工业上测定钛铁合金中钛含量的其中一步反应原理是:以KSCN为指示剂,用NH4Fe(SO4)2标准溶液滴定Ti(Ⅲ),反应的化学方程式为:Ti2(SO4)3+2NH4Fe(SO4)2===2Ti(SO4)2+(NH4)2SO4+2FeSO4,则达到滴定终点的实验现象是
您最近一年使用:0次
2019-04-03更新
|
647次组卷
|
2卷引用:北京市北京交通大学附属中学2020-2021学年高二上学期期末练习化学试题
名校
解题方法
8 . 工业上可以用废铁屑制备活性Fe3O4,流程如下图:
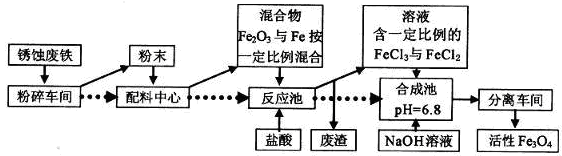
(1)在制备过程中,要将块状固体原料粉碎、磨成粉末,作用是________________________
(2)在合成池里生成Fe3O4的离子方程式为__________________________
(3)假如在反应池中几乎没有气体产生,根据流程可知,配料中心很可能使混合物中的Fe2O3与Fe物质的量之比接近________
(4)某同学利用废铁屑(含Fe和Fe2O3)来制取FeCl3·6H2O晶体,同时测定混合物中铁的质量分数,装置如图(夹持装置略,气密性已检验):

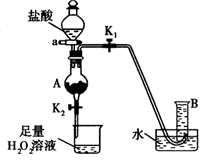
操作步骤如下:
I.打开弹簧夹K1、关闭弹簧夹K2,并打开活塞a,缓慢滴加盐酸。
Ⅱ.当……时,关闭弹簧夹K1打开弹簧夹K2,当A中溶液完全进入烧杯后关闭活塞a。
Ⅲ.将烧杯中溶液蒸发浓缩、冷却结晶、过滤后得到FeC13·6H2O晶体。
请回答:
①操作Ⅱ中“……”的内容是______________ ,烧杯中的现象是________________ ,相应的方程式是________________ 、________________ 。(是离子反应的写离子方程式)
②若混合物质量为m g,实验结束后测得B中所得的气体是V mL(标准状况时),该同学由此计算出此废铁屑中铁的质量分数是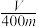 ,该数值比实际数值偏低,若实验过程操作无误,偏低的原因是
,该数值比实际数值偏低,若实验过程操作无误,偏低的原因是______________________ 。

(1)在制备过程中,要将块状固体原料粉碎、磨成粉末,作用是
(2)在合成池里生成Fe3O4的离子方程式为
(3)假如在反应池中几乎没有气体产生,根据流程可知,配料中心很可能使混合物中的Fe2O3与Fe物质的量之比接近
(4)某同学利用废铁屑(含Fe和Fe2O3)来制取FeCl3·6H2O晶体,同时测定混合物中铁的质量分数,装置如图(夹持装置略,气密性已检验):


操作步骤如下:
I.打开弹簧夹K1、关闭弹簧夹K2,并打开活塞a,缓慢滴加盐酸。
Ⅱ.当……时,关闭弹簧夹K1打开弹簧夹K2,当A中溶液完全进入烧杯后关闭活塞a。
Ⅲ.将烧杯中溶液蒸发浓缩、冷却结晶、过滤后得到FeC13·6H2O晶体。
请回答:
①操作Ⅱ中“……”的内容是
②若混合物质量为m g,实验结束后测得B中所得的气体是V mL(标准状况时),该同学由此计算出此废铁屑中铁的质量分数是
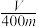 ,该数值比实际数值偏低,若实验过程操作无误,偏低的原因是
,该数值比实际数值偏低,若实验过程操作无误,偏低的原因是
您最近一年使用:0次
2017-07-14更新
|
461次组卷
|
3卷引用:福建省福州市闽侯县2016-2017学年高二下学期期末考试化学试题
福建省福州市闽侯县2016-2017学年高二下学期期末考试化学试题(已下线)2019年8月10日 《每日一题》2020年高考一轮复习—— 周末培优山西大学附中2020届高三上学期第二次模块诊断化学试题



