名校
解题方法
1 . 阅读下面一段材料并回答问题。
(1) 中铁元素的化合价为
中铁元素的化合价为_______ 。
(2)制备 需要在
需要在_______  填“酸性”、“碱性”或“中性”
填“酸性”、“碱性”或“中性” 环境中进行。
环境中进行。
(3)下列关于 的说法中,不正确的是
的说法中,不正确的是_______ 。
 是强氧化性的盐
是强氧化性的盐
 固体保存需要防潮
固体保存需要防潮
 其消毒和净化水的原理相同
其消毒和净化水的原理相同
 其净水优点有:作用快、安全性好、无异味
其净水优点有:作用快、安全性好、无异味
(4)将 与水反应的化学方程式补充完整:
与水反应的化学方程式补充完整:_______
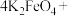 _______
_______ _______
_______ 胶体
胶体 _______
_______ _______
_______
该反应消耗1个 时,转移的电子数为
时,转移的电子数为_______ 个
(5)消毒净化 水,至少需要
水,至少需要 的质量为
的质量为_______  。
。
| 高铁酸钾使用说明书 【化学式】K2FeO4 【性状】暗紫色具有金属光泽的粉末,无臭无味 【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气K2FeO4通过强烈 的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。K2FeO4与水反应还能产生具有强吸附 性的Fe(OH)3胶体,可除去水中细微的悬浮物,有净水作用 【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理 【用量】消毒净化1L水投放5 mg K2FeO4即可达到卫生标准 ... ... |
 中铁元素的化合价为
中铁元素的化合价为(2)制备
 需要在
需要在 填“酸性”、“碱性”或“中性”
填“酸性”、“碱性”或“中性” 环境中进行。
环境中进行。(3)下列关于
 的说法中,不正确的是
的说法中,不正确的是 是强氧化性的盐
是强氧化性的盐 固体保存需要防潮
固体保存需要防潮 其消毒和净化水的原理相同
其消毒和净化水的原理相同 其净水优点有:作用快、安全性好、无异味
其净水优点有:作用快、安全性好、无异味(4)将
 与水反应的化学方程式补充完整:
与水反应的化学方程式补充完整: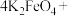 _______
_______ _______
_______ 胶体
胶体 _______
_______ _______
_______
该反应消耗1个
 时,转移的电子数为
时,转移的电子数为(5)消毒净化
 水,至少需要
水,至少需要 的质量为
的质量为 。
。
您最近一年使用:0次
2 . 绿钒(FeSO4•xH2O)是含有一定量结晶水的硫酸亚铁,在工农业生产中具有 重要的用途。某化学兴趣小组对绿钒的一些性质进行探究。回答下列问题:
(1)在试管中加入少量绿钒样品,加水溶解,滴加KSCN溶液,溶液颜色无明显变化,结论是_______ ,再向试管中通入空气,溶液逐渐变红,原因是_______ 。
(2)为测定绿钒中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重, 记为m1g。将样品装入石英玻璃管中,再次将装置A称重,记为m2g。按如图连接好装置

①仪器B的名称是_______ 。
②将下列实验操作步骤正确排序_______ (填序号),重复上述操作步骤,直至A恒重,记为m3g。
a.点燃酒精灯,加热 b.打开K1和K2,缓缓通入N2 c.关闭K1和K2 d.熄灭酒精灯 e.称量A f.冷却到室温
(3)根据实验记录,计算绿钒化学式中结晶水数目x为_______ (列式表示)。若实验时按a、b次序操作,则得出的x_______ (填“偏大”、“偏小”或“无影响”)。
(4)为探究硫酸亚铁的分解产物,将(2)中已恒重的装置A改用酒精喷灯加热。实验后反应管中残留固体为红色粉末,并将分解产生的气体依次通入右侧C、D装置。

①C中的溶液为BaCl2其作用是_______ ,D中的溶液为_______ ,可观察到的现象是_______ 。
②写出硫酸亚铁高温分解反应的化学方程式_______ 。
(1)在试管中加入少量绿钒样品,加水溶解,滴加KSCN溶液,溶液颜色无明显变化,结论是
(2)为测定绿钒中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重, 记为m1g。将样品装入石英玻璃管中,再次将装置A称重,记为m2g。按如图连接好装置

①仪器B的名称是
②将下列实验操作步骤正确排序
a.点燃酒精灯,加热 b.打开K1和K2,缓缓通入N2 c.关闭K1和K2 d.熄灭酒精灯 e.称量A f.冷却到室温
(3)根据实验记录,计算绿钒化学式中结晶水数目x为
(4)为探究硫酸亚铁的分解产物,将(2)中已恒重的装置A改用酒精喷灯加热。实验后反应管中残留固体为红色粉末,并将分解产生的气体依次通入右侧C、D装置。

①C中的溶液为BaCl2其作用是
②写出硫酸亚铁高温分解反应的化学方程式
您最近一年使用:0次
3 . 氨是重要的化工原料,回答下列问题:
I.氨气的制备

(1)制取并收集一瓶干燥氨气,上述装置的连接顺序为A→_____→_____→C→____,____ ,制气时的化学方程式为___________ ,收集时气体从___________ 口进入
II.氨气的性质
(2)装置如图所示,打开止水夹,用热毛巾将烧瓶捂热,水上喷形成红色喷泉,说明氨气___________ 。

III.氨气的用途
利用下图装置由氨制硝酸,实验时戊中溶液呈淡黄色时关闭分液漏斗活塞。

(3)Na2O2的作用___________ ,证明有硝酸生成的实验是___________ ,发生反应的离子方程式___________ 。
(4)实验中的氮氧化物(NOx)尾气折算成标准状况下的体积为aL,完全吸收时,烧杯中c(NaOH)至少是___________ mol/L(忽略溶液体积变化)。
I.氨气的制备

(1)制取并收集一瓶干燥氨气,上述装置的连接顺序为A→_____→_____→C→____,
II.氨气的性质
(2)装置如图所示,打开止水夹,用热毛巾将烧瓶捂热,水上喷形成红色喷泉,说明氨气

III.氨气的用途
利用下图装置由氨制硝酸,实验时戊中溶液呈淡黄色时关闭分液漏斗活塞。

(3)Na2O2的作用
(4)实验中的氮氧化物(NOx)尾气折算成标准状况下的体积为aL,完全吸收时,烧杯中c(NaOH)至少是
您最近一年使用:0次
2021-12-11更新
|
1081次组卷
|
3卷引用:四川省达州市普通高中2022届高三第一次诊断性测试理综化学试题
四川省达州市普通高中2022届高三第一次诊断性测试理综化学试题四川省达州市2021-2022学年高三上学期第一次诊断考试理科综合化学试题(已下线)微专题24 氯气、氨气、二氧化硫的实验室制备与应用-备战2023年高考化学一轮复习考点微专题



