名校
解题方法
1 . 部分含氮物质的“价—类”二维图如下:
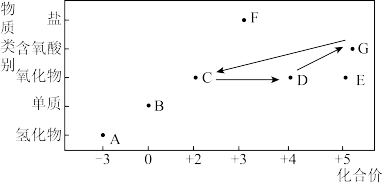
根据图示信息,回答下列问题:
(1)E的化学式为_______ 。写出B的用途:_______ (列举一种)。
(2)在常温条件下实现 的循环转化,其中有颜色变化且属于化合反应的化学方程式为
的循环转化,其中有颜色变化且属于化合反应的化学方程式为_______ 。
(3)实验室可选择甲、乙装置制备A,利用收集的A用丙装置探究A的性质。
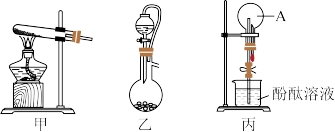
①若选择乙制备A,则反应物是_______ (填名称)。
②若选择甲装置制备A,则化学方程式为_______ 。
③若顺利完成丙装置实验,可观察到_______ 色喷泉。
(4)若F是一种钠盐,取少量F溶于蒸馏水,将溶液分成两份,进行实验,测得结果如下:
已知 水溶液呈无色,由此推断,F具有_______(填字母)。
水溶液呈无色,由此推断,F具有_______(填字母)。

根据图示信息,回答下列问题:
(1)E的化学式为
(2)在常温条件下实现
 的循环转化,其中有颜色变化且属于化合反应的化学方程式为
的循环转化,其中有颜色变化且属于化合反应的化学方程式为(3)实验室可选择甲、乙装置制备A,利用收集的A用丙装置探究A的性质。

①若选择乙制备A,则反应物是
②若选择甲装置制备A,则化学方程式为
③若顺利完成丙装置实验,可观察到
(4)若F是一种钠盐,取少量F溶于蒸馏水,将溶液分成两份,进行实验,测得结果如下:
| 实验 | 操作 | 现象 |
| Ⅰ | 向一份溶液中滴加稀硫酸酸化的 溶液,再滴加淀粉溶液,振荡 溶液,再滴加淀粉溶液,振荡 | 溶液由无色变为蓝色 |
| Ⅱ | 向另一份溶液中滴加少量的稀硫酸酸化的 溶液,振荡 溶液,振荡 | 溶液由紫红色变为无色 |
 水溶液呈无色,由此推断,F具有_______(填字母)。
水溶液呈无色,由此推断,F具有_______(填字母)。| A.氧化性 | B.还原性 | C.既有氧化性,又有还原性 | D.既无氧化性,又无还原性 |
您最近一年使用:0次
名校
2 . 氨气是重要的化工原料,在工农业生产中有重要用途。
(1)工业上合成氨的反应原理为_______ 。
(2)氨气极易溶于水,这个性质可以利用如图装置进喷泉实验。
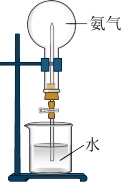
①完成喷泉实验的具体操作为_______ 。
②若该条件为标准状况,且水充满整个圆底烧瓶,则最终所得溶液的物质的量浓度为_______ 。
某小组的同学欲探究NH3经一系列反应得到HNO3和NH4NO3的过程。NH3的转化过程如图1所示。
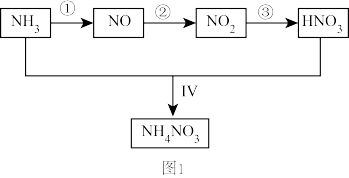
甲、乙两同学分别按图2所示装置进行实验。用于A、B装置中的可选药品:浓氨水、30% H2O2溶液、蒸馏水、NaOH固体、MnO2。
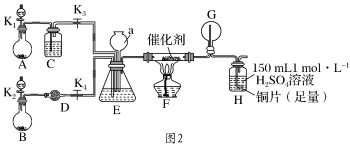
(3)装置A的圆底烧瓶中发生反应的化学方程式为_______ 。装置E有多种作用,下列关于装置E的作用或其中所盛液体的说法中,不正确的是_______ (填字母)。
a.使氨气和氧气充分混合
b.控制通入氨气和氧气的体积比
c.平衡装置内的压强
d.锥形瓶内液体是饱和食盐水
(4)甲同学先点燃酒精灯,再打开K1、K2、K3、K4,反应一段时间后,成功模拟了反应过程,并将实验中产生的气体持续通入装置H一段时间后,装置H中的溶液变成蓝色,则其中铜片所参与反应的离子方程式为_______ ,若制得的氨气仅按①→②→③的顺序完全转化为硝酸,欲使装置H中所得溶液为纯净的CuSO4溶液,理论上所需氨气在标准状况下的体积为_______ L(假设硝酸与铜反应产生的还原产物全部排出反应装置)。
(5)乙同学为模拟过程Ⅳ的反应,在甲同学操作的基础上对该装置进行了下列各项中的一项操作,使G处圆底烧瓶中产生大量白烟,你认为这项操作是_______ (填字母)。
a.关闭K3并熄灭酒精灯
b.关闭K4并熄灭酒精灯
c.关闭K3、K4并熄灭酒精灯
(6)丙同学认为该系列实验装置存在一处明显的设计缺陷,你认为该设计缺陷_______ 。
(1)工业上合成氨的反应原理为
(2)氨气极易溶于水,这个性质可以利用如图装置进喷泉实验。

①完成喷泉实验的具体操作为
②若该条件为标准状况,且水充满整个圆底烧瓶,则最终所得溶液的物质的量浓度为
某小组的同学欲探究NH3经一系列反应得到HNO3和NH4NO3的过程。NH3的转化过程如图1所示。

甲、乙两同学分别按图2所示装置进行实验。用于A、B装置中的可选药品:浓氨水、30% H2O2溶液、蒸馏水、NaOH固体、MnO2。

(3)装置A的圆底烧瓶中发生反应的化学方程式为
a.使氨气和氧气充分混合
b.控制通入氨气和氧气的体积比
c.平衡装置内的压强
d.锥形瓶内液体是饱和食盐水
(4)甲同学先点燃酒精灯,再打开K1、K2、K3、K4,反应一段时间后,成功模拟了反应过程,并将实验中产生的气体持续通入装置H一段时间后,装置H中的溶液变成蓝色,则其中铜片所参与反应的离子方程式为
(5)乙同学为模拟过程Ⅳ的反应,在甲同学操作的基础上对该装置进行了下列各项中的一项操作,使G处圆底烧瓶中产生大量白烟,你认为这项操作是
a.关闭K3并熄灭酒精灯
b.关闭K4并熄灭酒精灯
c.关闭K3、K4并熄灭酒精灯
(6)丙同学认为该系列实验装置存在一处明显的设计缺陷,你认为该设计缺陷
您最近一年使用:0次
2022-04-14更新
|
114次组卷
|
2卷引用:江西省宜春市上高二中2021-2022学年高一下学期第七次月考化学试题
名校
3 .  在生产和生活中有着广泛用途,某化学小组在实验室制备
在生产和生活中有着广泛用途,某化学小组在实验室制备 并探究其性质。请回答:
并探究其性质。请回答:
(一) 的制备,分步骤Ⅰ、Ⅱ两步进行。
的制备,分步骤Ⅰ、Ⅱ两步进行。
步骤Ⅰ.先利用下图所示装置制备
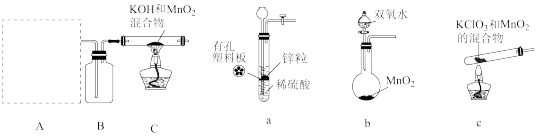
(1)装置A应选用___________ (填a、b或c)。
(2)装置B中所盛试剂的名称为___________ 。
(3)装置C处反应生成 的化学方程式为
的化学方程式为___________ 。
步骤Ⅱ.由 制备
制备 。已知:
。已知: 易溶于水,水溶液呈墨绿色。主要过程如下:
易溶于水,水溶液呈墨绿色。主要过程如下:
①充分反应后,将装置C处所得固体加水溶解,过滤;
②向滤液中通入足量CO2,过滤出生成的 ;
;
⑧将滤液蒸发浓缩、降温结晶、过滤、洗涤、干燥,得 晶体。
晶体。
(4)过程②向滤液中通入足量 ,可观察到的现象为
,可观察到的现象为___________ ;该步反应中氧化剂与还原剂的物质的量之比为___________ 。
(二)KMnO4的性质
已知:KMnO4具有强氧化性,可与草酸 反应。
反应。
(5)写出 酸性溶液与草酸反应的离子方程式
酸性溶液与草酸反应的离子方程式___________ 。
(6)基于(5)的反应原理,选择适当试剂探究浓度对化学反应速率的影响。
可供选择的试剂有:①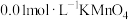 酸性溶液;②
酸性溶液;②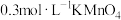 酸性溶液;③
酸性溶液;③ 溶液;④
溶液;④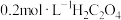 溶液,为了更好的观察现象,应选择的试剂为
溶液,为了更好的观察现象,应选择的试剂为___________ (填序号)。
 在生产和生活中有着广泛用途,某化学小组在实验室制备
在生产和生活中有着广泛用途,某化学小组在实验室制备 并探究其性质。请回答:
并探究其性质。请回答:(一)
 的制备,分步骤Ⅰ、Ⅱ两步进行。
的制备,分步骤Ⅰ、Ⅱ两步进行。步骤Ⅰ.先利用下图所示装置制备


(1)装置A应选用
(2)装置B中所盛试剂的名称为
(3)装置C处反应生成
 的化学方程式为
的化学方程式为步骤Ⅱ.由
 制备
制备 。已知:
。已知: 易溶于水,水溶液呈墨绿色。主要过程如下:
易溶于水,水溶液呈墨绿色。主要过程如下:①充分反应后,将装置C处所得固体加水溶解,过滤;
②向滤液中通入足量CO2,过滤出生成的
 ;
;⑧将滤液蒸发浓缩、降温结晶、过滤、洗涤、干燥,得
 晶体。
晶体。(4)过程②向滤液中通入足量
 ,可观察到的现象为
,可观察到的现象为(二)KMnO4的性质
已知:KMnO4具有强氧化性,可与草酸
 反应。
反应。(5)写出
 酸性溶液与草酸反应的离子方程式
酸性溶液与草酸反应的离子方程式(6)基于(5)的反应原理,选择适当试剂探究浓度对化学反应速率的影响。
可供选择的试剂有:①
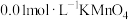 酸性溶液;②
酸性溶液;②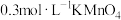 酸性溶液;③
酸性溶液;③ 溶液;④
溶液;④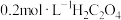 溶液,为了更好的观察现象,应选择的试剂为
溶液,为了更好的观察现象,应选择的试剂为
您最近一年使用:0次
2021-12-07更新
|
646次组卷
|
7卷引用:江西省临川一中暨临川一中实验学校2021-2022学年高二下学期第二次月考化学试题
江西省临川一中暨临川一中实验学校2021-2022学年高二下学期第二次月考化学试题(已下线)解密11 化学实验(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题11 物质制备类综合实验-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)(已下线)回归教材重难点10 综合实验方案的设计与评价-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)回归教材重难点10 实验方案的设计与评价-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)河北省邢台市四校联盟2021-2022学年高三12月联考化学试题湖南省隆回县第二中学2021-2022学年高三上学期第四次月考化学试题



