名校
解题方法
1 . 某小组通过分析镁与酸反应时pH的变化,探究镁与醋酸溶液反应的实质。
【实验】在常温水浴条件下,进行实验Ⅰ~Ⅲ,记录生成气体体积和溶液pH的变化:
Ⅰ.取0.1g光亮的镁屑(过量)放入10mL 0.10mol/L HCl溶液中;
Ⅱ.取0.1g光亮的镁屑放入10mL 0.10
 溶液
溶液 中;
中;
Ⅲ.取0.1g光亮的镁屑放入10mL pH=2.9 HCl溶液中。
【数据】
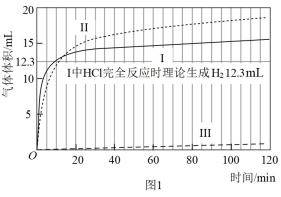
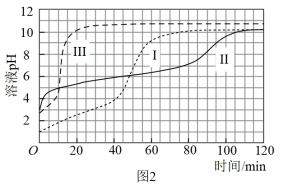
(1)起始阶段,Ⅰ中主要反应的离子方程式是___________ 。
(2)Ⅱ起始溶液中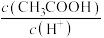 约为
约为___________ 。(选填“1”、“10”或“102”)
(3)起始阶段,导致Ⅱ、Ⅲ气体产生速率差异的主要因素不是 ,实验证据是
,实验证据是___________ 。
(4)探究Ⅱ的反应速率大于Ⅲ的原因。
提出假设: 能直接与Mg反应。
能直接与Mg反应。
进行实验Ⅳ:___________ 。
实验现象:___________ 。
得出结论:该假设成立。
(5)探究醋酸溶液中与Mg反应的主要微粒,进行实验Ⅴ。
与Ⅱ相同的条件和试剂用量,将溶液换成含0.10 的
的 与0.10
与0.10
 的混合溶液pH=4.8,气体产生速率与Ⅱ对比如下。
的混合溶液pH=4.8,气体产生速率与Ⅱ对比如下。
对比a~c中的微粒浓度,解释其a与b、a与c气体产生速率差异的原因:___________ 。
(6)综合以上实验得出2个结论:镁与醋酸溶液反应时, 、
、 、
、 均能与镁反应产生氢气:
均能与镁反应产生氢气:___________ 。
【实验】在常温水浴条件下,进行实验Ⅰ~Ⅲ,记录生成气体体积和溶液pH的变化:
Ⅰ.取0.1g光亮的镁屑(过量)放入10mL 0.10mol/L HCl溶液中;
Ⅱ.取0.1g光亮的镁屑放入10mL 0.10

 溶液
溶液 中;
中;Ⅲ.取0.1g光亮的镁屑放入10mL pH=2.9 HCl溶液中。
【数据】


(1)起始阶段,Ⅰ中主要反应的离子方程式是
(2)Ⅱ起始溶液中
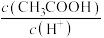 约为
约为(3)起始阶段,导致Ⅱ、Ⅲ气体产生速率差异的主要因素不是
 ,实验证据是
,实验证据是(4)探究Ⅱ的反应速率大于Ⅲ的原因。
提出假设:
 能直接与Mg反应。
能直接与Mg反应。进行实验Ⅳ:
实验现象:
得出结论:该假设成立。
(5)探究醋酸溶液中与Mg反应的主要微粒,进行实验Ⅴ。
与Ⅱ相同的条件和试剂用量,将溶液换成含0.10
 的
的 与0.10
与0.10
 的混合溶液pH=4.8,气体产生速率与Ⅱ对比如下。
的混合溶液pH=4.8,气体产生速率与Ⅱ对比如下。| a.实验Ⅴ起始速率 | b.实验Ⅱ起始速率 | c.实验ⅡpH=4.8时速率 |
2.1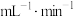 | 2.3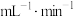 | 0.8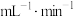 |
(6)综合以上实验得出2个结论:镁与醋酸溶液反应时,
 、
、 、
、 均能与镁反应产生氢气:
均能与镁反应产生氢气:
您最近一年使用:0次
名校
解题方法
2 . 探究一定条件下反应物浓度对硫代硫酸钠(Na2S2O3)与硫酸反应速率的影响。
【查阅资料】a.Na2S2O3易溶于水,能与硫酸发生反应;
b.浊度计用于测量浑浊度的变化。产生的沉淀越多,浑浊度(单位为NTU)值越大。
【实验过程】

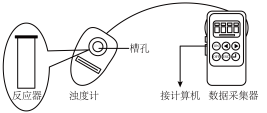
用如图所示装置进行如表所示的 5 个实验,分别测量混合后溶液达到相同浑浊度的过程中, 浑浊度随时间的变化。实验①~⑤所得数据如图曲线①~⑤所示及分组实验数据:
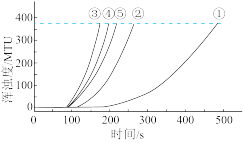
【分析与解释】
(1)实验序号①中,Na2S2O3写出与硫酸的化学反应方程式_______ ;溶液混合后Na2S2O3溶液的初始浓度_______ mol/L。
(2)实验③中,x =_______ 。
(3)实验①、②、③的目的是_______ 。
(4)通过比较①、②、③与③、④、⑤两组实验,可推断:反应物浓度的改变对Na2S2O3与硫酸反应的化学反应速率的影响,Na2S2O3溶液浓度的改变影响更大。该推断的证据是_______ 。
实验二:以Fe3+与I-反应生成Fe2+和I2为例,探究该反应是否为可逆反应。
实验方法:在KI溶液中滴加少量FeCl3溶液,将混合溶液均匀分到甲、乙、丙三支试管中;往试管甲中滴加淀粉溶液,往试管乙中滴加某溶液,丙试管中加入蒸馏水,如图所示:
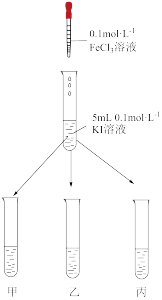
(5)若已知反应为可逆反应,则试管甲中的现象为_______ ,试管乙中加入的试剂为_______ ,现象为_______ 。
【查阅资料】a.Na2S2O3易溶于水,能与硫酸发生反应;
b.浊度计用于测量浑浊度的变化。产生的沉淀越多,浑浊度(单位为NTU)值越大。
【实验过程】


用如图所示装置进行如表所示的 5 个实验,分别测量混合后溶液达到相同浑浊度的过程中, 浑浊度随时间的变化。实验①~⑤所得数据如图曲线①~⑤所示及分组实验数据:

| 实验编号 | Na2S2O3溶液 | H2SO4溶液 | 蒸馏水 | ||
| c / (mol·L-1) | V / mL | c / (mol·L-1) | V / mL | V / mL | |
| ① | 0.1 | 1.5 | 0.1 | 3.5 | 10 |
| ② | 0.1 | 2.5 | 0.1 | 3.5 | 9 |
| ③ | 0.1 | 3.5 | 0.1 | 3.5 | x |
| ④ | 0.1 | 3.5 | 0.1 | 2.5 | 9 |
| ⑤ | 0.1 | 3.5 | 0.1 | 1.5 | 10 |
(1)实验序号①中,Na2S2O3写出与硫酸的化学反应方程式
(2)实验③中,x =
(3)实验①、②、③的目的是
(4)通过比较①、②、③与③、④、⑤两组实验,可推断:反应物浓度的改变对Na2S2O3与硫酸反应的化学反应速率的影响,Na2S2O3溶液浓度的改变影响更大。该推断的证据是
实验二:以Fe3+与I-反应生成Fe2+和I2为例,探究该反应是否为可逆反应。
实验方法:在KI溶液中滴加少量FeCl3溶液,将混合溶液均匀分到甲、乙、丙三支试管中;往试管甲中滴加淀粉溶液,往试管乙中滴加某溶液,丙试管中加入蒸馏水,如图所示:

(5)若已知反应为可逆反应,则试管甲中的现象为
您最近一年使用:0次
解题方法
3 . K2Cr2O7是一种有致癌性的强氧化剂,含Cr2O72—的酸性工业废水必须经过处理才能排放。工业上通常采用Fe电极电解法处理,调节pH值使之以Cr(OH)3沉淀形式除去。某化学兴趣小组在实验室里探究了该处理工艺,具体实验日志如下:

I.原理探查
查阅文献发现,电解时阳极产生Fe2+,在阴极附近(如图),Cr2O72—被Fe2+还原成Cr3+,而Fe3+则在阴极表面还原为Fe2+,如此循环。
(1)用离子方程式表示Cr2O72—与Fe2+的反应:______________________________ 。
II.实验探究
实验一:探究不同电压对Cr2O72-降解效率的影响
各取6份100 mL 1 mol/L 酸性K2Cr2O7溶液,均以Fe为电极,分别用不同电压电解5 min。取电解后溶液10 mL,测定Cr2O72-的含量,所测溶液中Cr2O72-物质的量与电解电压关系如下图所示。(假设电解前后溶液体积不变)
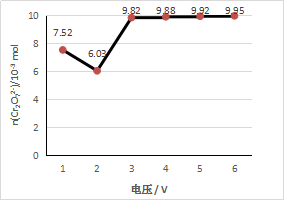
(2)实验结果显示,最佳电解电压应选择_______ V。
(3)电压为6 V时,用Cr2O72-表示5 min内平均反应速率为_________ mol·L—1·min—1。
(4)当电压高于3 V时,阴阳两极在电解过程中不断有气泡产生,且测得体积比约等于2:1。因此,阳极产生气泡的电极反应式为:__________________________________ 。
实验二:探究其他影响Cr2O72-降解效率的因素
以1A电流电解500mL K2Cr2O7稀溶液,通电时间30min,考察影响Cr2O72-降解效率的其他因素。具体方法和数据如下表所示。
(5)以上实验中,Cr2O72-降解效率最高的是实验组_____ (填编号),该实验组阳极电极反应式为:__________________________________ 。
(6)对比②和③,Cr2O72-降解效率③>②的原因是:__________________________ 。
(7)由实验组①和②,可认为Cr2O72-能直接在阴极放电还原,电极反应式为:__________________________________ 。
(8)法拉第提出了电解定律,为电化学的发展作出了巨大贡献。根据法拉第电解定律: Q=It=n(e-)F,[I为电流强度单位为A,t为时间单位为s,n(e-)为通过电路的电子的物质的量,F为法拉第常数(每摩电子电量,F=96500 C·mol-1)],则实验组②中的电流效率 =
=______________ 。(保留三位有效数字;假设电解前后溶液体积不变,且没有副反应发生。)

I.原理探查
查阅文献发现,电解时阳极产生Fe2+,在阴极附近(如图),Cr2O72—被Fe2+还原成Cr3+,而Fe3+则在阴极表面还原为Fe2+,如此循环。
(1)用离子方程式表示Cr2O72—与Fe2+的反应:
II.实验探究
实验一:探究不同电压对Cr2O72-降解效率的影响
各取6份100 mL 1 mol/L 酸性K2Cr2O7溶液,均以Fe为电极,分别用不同电压电解5 min。取电解后溶液10 mL,测定Cr2O72-的含量,所测溶液中Cr2O72-物质的量与电解电压关系如下图所示。(假设电解前后溶液体积不变)

(2)实验结果显示,最佳电解电压应选择
(3)电压为6 V时,用Cr2O72-表示5 min内平均反应速率为
(4)当电压高于3 V时,阴阳两极在电解过程中不断有气泡产生,且测得体积比约等于2:1。因此,阳极产生气泡的电极反应式为:
实验二:探究其他影响Cr2O72-降解效率的因素
以1A电流电解500mL K2Cr2O7稀溶液,通电时间30min,考察影响Cr2O72-降解效率的其他因素。具体方法和数据如下表所示。
| 实验组 | ① | ② | ③ | ④ | |
| 加入硫酸铁 /g | 0 | 0 | 5.0 | 0 | |
| 加入浓硫酸 /mL | 0 | 1.0 | 1.0 | 1.0 | |
| 电极材料 | 阴极 | 石墨 | 石墨 | 石墨 | 石墨 |
| 阳极 | 石墨 | 石墨 | 石墨 | 铁 | |
| Cr2O72-浓度 / mol·L-1 | 初始 | 0.00651 | 0.00651 | 0.00651 | 0.00651 |
| 结束 | 0.00645 | 0.00568 | 0.00516 | 0.00278 | |
(6)对比②和③,Cr2O72-降解效率③>②的原因是:
(7)由实验组①和②,可认为Cr2O72-能直接在阴极放电还原,电极反应式为:
(8)法拉第提出了电解定律,为电化学的发展作出了巨大贡献。根据法拉第电解定律: Q=It=n(e-)F,[I为电流强度单位为A,t为时间单位为s,n(e-)为通过电路的电子的物质的量,F为法拉第常数(每摩电子电量,F=96500 C·mol-1)],则实验组②中的电流效率
 =
=
您最近一年使用:0次



