解题方法
1 . 焦炭是工业生产中的重要还原剂和燃料,活性炭用于生活和实验室中通过吸附作用除去有害气体或有毒物质。它们的化学成分都可以看成是碳单质。
(1)红热的焦炭投入浓硝酸中,写出反应的化学方程式________________ ;
(2)将一定条件下的高锰酸钾溶液与活性炭混合,可发生如下反应(未配平)
_______MnO +_______C+_______H2O——_______MnO2+_______① +CO
+_______C+_______H2O——_______MnO2+_______① +CO
则 ① 处应该填入的微粒化学式为_________ ;
(3)PbO俗称密陀僧或铅黄,将黄色粉末状PbO和足量活性炭充分混合,平铺在反应管a中,在b瓶中盛足量澄清石灰水,按图连接仪器。实验开始时缓缓通入氮气,过一段时间后,加热反应管a,观察到管内发生剧烈反应,并有熔融物生成。同时,b瓶的溶液中出现白色浑浊。待反应完全后,停止加热,仍继续通氮气,直至反应管冷却。此时,管中的熔融物凝固成银白色金属。

写出反应管a中发生的所有反应的化学方程式__________ 。
(1)红热的焦炭投入浓硝酸中,写出反应的化学方程式
(2)将一定条件下的高锰酸钾溶液与活性炭混合,可发生如下反应(未配平)
_______MnO
 +_______C+_______H2O——_______MnO2+_______① +CO
+_______C+_______H2O——_______MnO2+_______① +CO
则 ① 处应该填入的微粒化学式为
(3)PbO俗称密陀僧或铅黄,将黄色粉末状PbO和足量活性炭充分混合,平铺在反应管a中,在b瓶中盛足量澄清石灰水,按图连接仪器。实验开始时缓缓通入氮气,过一段时间后,加热反应管a,观察到管内发生剧烈反应,并有熔融物生成。同时,b瓶的溶液中出现白色浑浊。待反应完全后,停止加热,仍继续通氮气,直至反应管冷却。此时,管中的熔融物凝固成银白色金属。

写出反应管a中发生的所有反应的化学方程式
您最近一年使用:0次
2 . 微生物对人类有着各种各样的用途,现在生物工程学家利用微生物从矿石中提取金属。铜是一种很有价值的金属,可以从铜矿中提取。微生物法是采用某些细菌能用空气中的氧气氧化硫化铜矿石,把不溶性的硫化铜转化成可溶的硫酸铜。利用细菌提取铜的生产过程:在已有细菌存在的岩石。矿石堆中,喷洒酸水以促进细菌生长;在它们的生长过程中,氧化而成的硫酸铜形成低浓度的溶液流到矿石堆的底部,再从这种溶液中提取金属铜。水循环使用,再回到矿石堆中。在美国,10%的铜是用这种方法生产的。
试回答下列问题:
(1)细菌把硫化铜氧化为硫酸铜的过程中起了什么作用:_______ 。
(2)从硫酸铜溶液中提取铜,简便而经济的方法是_______ ;相应的化学方程式为: _______ 。
(3)普通生产铜的方法是在空气中燃烧硫化铜(产物中有一种气态氧化物)。试比较两种方法的优缺点_______ 。
(4)用一定量的铁与足量的稀H2SO4及足量的CuO制成单质铜,有人设计以下两种方案:
①Fe H2
H2 Cu
Cu
②CuO CuSO4
CuSO4 Cu
Cu
若按实验原则进行操作,则两者制得单质铜的量的比较中,正确的是_______
(5)工业上可用Cu2S和O2反应制取粗铜,该反应中氧化剂为_______ 。电解粗铜制取精铜,电解时,阳极材料是_______ ,电解液中必须含有的阳离子是_______ 。
(6)工业上制备氯化铜时,是将浓盐酸用蒸气加热至80℃左右,慢慢加入粗制氧化铜粉末(含杂质氧化亚铁),充分搅拌,使之溶解,反应如下:
CuO+2HCl=CuCl2+H2O
FeO+2HCl=FeCl2+H2O
已知:pH≥9.6时,Fe2+以Fe(OH)2形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH在3~4时,Fe3+以Fe(OH)3的形式完全沉淀。除去溶液中的Fe2+,可以采用的方法是_______ 。
试回答下列问题:
(1)细菌把硫化铜氧化为硫酸铜的过程中起了什么作用:
(2)从硫酸铜溶液中提取铜,简便而经济的方法是
(3)普通生产铜的方法是在空气中燃烧硫化铜(产物中有一种气态氧化物)。试比较两种方法的优缺点
(4)用一定量的铁与足量的稀H2SO4及足量的CuO制成单质铜,有人设计以下两种方案:
①Fe
 H2
H2 Cu
Cu②CuO
 CuSO4
CuSO4 Cu
Cu若按实验原则进行操作,则两者制得单质铜的量的比较中,正确的是_______
| A.①多 | B.②多 | C.相等 | D.无法判断 |
(6)工业上制备氯化铜时,是将浓盐酸用蒸气加热至80℃左右,慢慢加入粗制氧化铜粉末(含杂质氧化亚铁),充分搅拌,使之溶解,反应如下:
CuO+2HCl=CuCl2+H2O
FeO+2HCl=FeCl2+H2O
已知:pH≥9.6时,Fe2+以Fe(OH)2形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH在3~4时,Fe3+以Fe(OH)3的形式完全沉淀。除去溶液中的Fe2+,可以采用的方法是
您最近一年使用:0次
3 . 合理、高效利用金属矿物,将其中的金属从其化合物中还原出来用于生产和制造各种金属材料,这一过程在工业上称为金属的冶炼。
(1)以HgO为原料冶炼Hg,冶炼方法是_______ 。
(2)铝热法是冶炼金属的方法之一,写出铝热法炼铁(Fe2O3)的化学方程式:_______ 。引发铝热反应的实验操作是:_______ 。
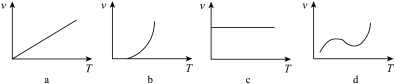
(3)某些金属氧化物粉末和铝粉在一定条件下可以发生铝热反应。下列反应速率(υ)和温度(T)的关系示意图中与铝热反应最接近的是:_______ (填字母)。
(1)以HgO为原料冶炼Hg,冶炼方法是
(2)铝热法是冶炼金属的方法之一,写出铝热法炼铁(Fe2O3)的化学方程式:
(3)某些金属氧化物粉末和铝粉在一定条件下可以发生铝热反应。下列反应速率(υ)和温度(T)的关系示意图中与铝热反应最接近的是:

您最近一年使用:0次
4 . (1)铜器表面有时会生成铜绿[Cu2(OH)2CO3],这层铜绿可用化学方法除去。试写出除去铜绿而不损伤器物的化学方程式 _________________________ 。
(2)工业上常用铝热反应产生的“铁水”来焊接铁轨,请写出铝热反应的化学方程式_________ 。
(3)冶金工业中,常用焦炭来冶炼铁。写出赤铁矿(Fe2O3)被CO还原成铁的化学方程式_____ 。
(2)工业上常用铝热反应产生的“铁水”来焊接铁轨,请写出铝热反应的化学方程式
(3)冶金工业中,常用焦炭来冶炼铁。写出赤铁矿(Fe2O3)被CO还原成铁的化学方程式
您最近一年使用:0次
9-10高一·全国·单元测试
5 . 古代的药金外观与金相似,常被误认为是金子,冶炼的方法如下:将碳酸锌、赤铜(Cu2O)、木炭混合加热到800℃,得到金光闪闪的“药金”.
(1)药金的主要成分是______________________________________________________ .
(2)冶炼时发生反应的化学方程式为___________________________________________ .
(1)药金的主要成分是
(2)冶炼时发生反应的化学方程式为
您最近一年使用:0次
2010-03-23更新
|
1163次组卷
|
6卷引用:2010~2011学年辽宁省瓦房店市高级中学高一下学期期末考试
(已下线)2010~2011学年辽宁省瓦房店市高级中学高一下学期期末考试(已下线)新课标高一化学第三节 用途广泛的金属材料练习人教版2017-2018学年高一化学必修1:3.3 用途广泛的金属材料 同步测试2(已下线)【走进新高考】(人教版必修一)3.3用途广泛的金属材料 同步练习01(已下线)5.1.2 金属的性质(第二课时)-【帮课堂】2021-2022学年高一化学同步精品讲义(沪科版2020必修第二册)【定心卷】1.3.2 氧化剂和还原剂随堂练习-人教版2023-2024学年必修第一册



