1 . 美国计划2028年再次登陆月球,并在月球上建立永久性基地,为人类登陆新的行星做好前期准备。为了解决基地人员的供氧问题,科学家设想利用月球富氧岩石制取氧气。其提氧原理是:用氢气还原富氧岩石获取水,再利用太阳能电池电解水得到氢气和氧气。
玄武岩(含钛铁矿)是月球的主要岩石之一,其质地坚硬,钛铁矿的主要成分为钛酸亚铁(FeTiO3)。用上述提氧原理,理论上,从1kgFeTiO3中可获取约105.3gO2。
(1)写出FeTiO3与H2反应的化学方程式:___ 。
(2)研究表明,月球上平均直径为40微米的小圆珠形成的堆积物(富含Fe2TiO4)是最适合提氧的矿物。这种堆积物作为提氧原料的优点是___ 。
(3)研究人员查阅文献后,得知钛铁矿在高温下还能被炭粉还原:2FeTiO3+C 2Fe+2TiO2+CO2↑,通过植物的光合作用可吸收CO2获得O2。他们设计了两套实验装置来测定钛铁矿中可提取氧的质量分数。
2Fe+2TiO2+CO2↑,通过植物的光合作用可吸收CO2获得O2。他们设计了两套实验装置来测定钛铁矿中可提取氧的质量分数。
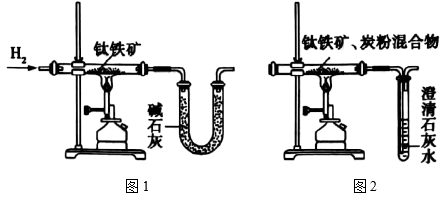
研究人员用图1装置从钛铁矿中提取氧,实验中得出的可提取氧的质量分数大于理论值,产生这种情况的原因可能是___ ;用图2装置进行实验的过程中,称得反应前钛铁矿的质量为m1g,炭粉的质量为m2g,钛铁矿完全反应后,测得生成CaCO3的质量为m3g,则钛铁矿中可提取氧的质量分数表达式为___ 。
(4)在钛铁矿提氧过程中科学家们常选用H2而不用其他还原剂,其主要原因是__ 。
玄武岩(含钛铁矿)是月球的主要岩石之一,其质地坚硬,钛铁矿的主要成分为钛酸亚铁(FeTiO3)。用上述提氧原理,理论上,从1kgFeTiO3中可获取约105.3gO2。
(1)写出FeTiO3与H2反应的化学方程式:
(2)研究表明,月球上平均直径为40微米的小圆珠形成的堆积物(富含Fe2TiO4)是最适合提氧的矿物。这种堆积物作为提氧原料的优点是
(3)研究人员查阅文献后,得知钛铁矿在高温下还能被炭粉还原:2FeTiO3+C
 2Fe+2TiO2+CO2↑,通过植物的光合作用可吸收CO2获得O2。他们设计了两套实验装置来测定钛铁矿中可提取氧的质量分数。
2Fe+2TiO2+CO2↑,通过植物的光合作用可吸收CO2获得O2。他们设计了两套实验装置来测定钛铁矿中可提取氧的质量分数。
研究人员用图1装置从钛铁矿中提取氧,实验中得出的可提取氧的质量分数大于理论值,产生这种情况的原因可能是
(4)在钛铁矿提氧过程中科学家们常选用H2而不用其他还原剂,其主要原因是
您最近半年使用:0次
解题方法
2 . 2020年地球日的主题为“珍爱地球,人与自然和谐共生”。研究和开发清洁能源与治理环境污染是未来发展的重要任务。
(1)氢气是清洁能源,高温下用天然气和水蒸气制取氢气和一氧化碳的化学方程式为_______ 。
(2)铁酸锰(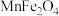 )可以用于热化学循环分解水制氢,
)可以用于热化学循环分解水制氢,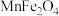 的制备流程如下:
的制备流程如下:
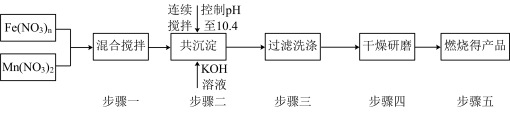
已知:整个过程中未发生氧化还原反应。
①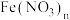 中
中
_______ 。
②“共沉淀”时,参与反应的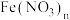 和
和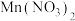 的物质的量之比为
的物质的量之比为_______ 。
③步骤三中沉淀洗涤干净的标准是_______ 。
④ 热化学循环制氢的反应为
热化学循环制氢的反应为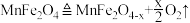 ,
,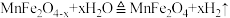 。该热化学循环制氢的优点为
。该热化学循环制氢的优点为_______ (答一点即可)。
(3)高铁酸钾常用于工业废水与城市生活污水的处理,工业上通过电解 浓溶液制备
浓溶液制备 。
。
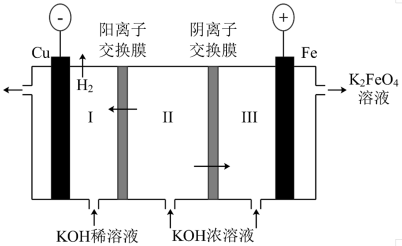
①阳极生成 的电极反应式为
的电极反应式为_______ 。
②Ⅰ室左侧出口流出的是_______ ,形成原因为_______ 。
(1)氢气是清洁能源,高温下用天然气和水蒸气制取氢气和一氧化碳的化学方程式为
(2)铁酸锰(
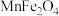 )可以用于热化学循环分解水制氢,
)可以用于热化学循环分解水制氢,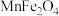 的制备流程如下:
的制备流程如下:
已知:整个过程中未发生氧化还原反应。
①
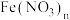 中
中
②“共沉淀”时,参与反应的
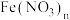 和
和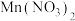 的物质的量之比为
的物质的量之比为③步骤三中沉淀洗涤干净的标准是
④
 热化学循环制氢的反应为
热化学循环制氢的反应为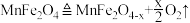 ,
,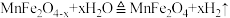 。该热化学循环制氢的优点为
。该热化学循环制氢的优点为(3)高铁酸钾常用于工业废水与城市生活污水的处理,工业上通过电解
 浓溶液制备
浓溶液制备 。
。
①阳极生成
 的电极反应式为
的电极反应式为②Ⅰ室左侧出口流出的是
您最近半年使用:0次
2020-12-19更新
|
215次组卷
|
2卷引用:山东省百所名校2021届高三12月联考化学试题
名校
解题方法
3 . 氢能是一种公认的高热值清洁能源,目前世界各国正致力于将高污染高排放的碳能源过渡成清洁高效低排放的氢能源。氢能开发包括以下三个环节:
一、氢燃料的制备
(1)我国氢气的主要来源是焦炉气制氢,所制得的氢气含有较多的CO和H2S,中温干法脱硫是用氧化铁将硫元素转化为硫化铁。干法脱硫的反应方程式为________ 。
(2)我国科研人员用木屑水蒸气气化制取氢燃料,在一定条件下,反应器中存在如下反应:
i.CO2 (g) +C(s)=2CO (g) △H1
ii.C(s) + H2O(g)=CO ( g) + H2 (g) △H2
iii.C(s) + 2H2 (g)=CH4( g) △H3
iv.CO(g) + H2O(g)=CO2 ( g) + H2 (g) △H4
v. CH4(g)+ 2 H2O(g)= CO2 ( g) + 4H2 (g) △H5
①△H5=_________________ 。
②研究中 CaO 的添加量按照CaO 中所含的Ca 和松木屑所含碳的物质的量比确定,在750℃,控制水蒸气流量为 0.lg/(min•g)下,探究催化剂加入量对产气组分和气化性能的影响,结果如表所示:
由表中数据,n(Ca) / n(C) =___ 时最为合理。 n(Ca) / n(C) 由0到0.5时,H2的体积分数显著增加的原因_____ 。体系的气化温度不仅对木屑的热解气化反应有影响 ,而且对 CaO 吸收 CO2的能力以及 CaCO3的分解反应也有很大影响。实验过程中,控制 n(Ca) / n(C) 为 1.0,水蒸气流量为0.1 g/(min• g), 将气化反应温度从700℃升到850℃,气化温度对产氢率、产气率的影响如表:
③从产氢率的角度考虑,最佳操作温度是________________ 。
④随着反应的进行,发现 CaO 的吸收能力逐渐降低,原因是___________ 。
二、氢燃料的存储
(3)将氢气储存于液体燃料中,可以解决氢气的安全高效存储和运输问题。由于甲醇具有单位体积储氢量高、活化温度低等优点,是理想的液体储氢平台分子。我国学者构建一种双功能结构的催化剂,反应过程中,在催化剂的表面同时活化水和甲醇。如图是甲醇脱氢转化的反应历程( TS 表示过渡态)。

根据图象判断甲醇脱氢反应中断裂的化学键是______ ,该反应的△H___ 0( 填“大于”、“等于”或“小于”)
三、氢燃料的应用。一种氢能电池的原理如图:
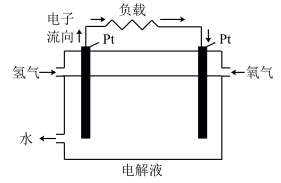
(4)正极的电极反应式为________ 。在 Pt 电极表面镜一层细小的铅粉,原因是______ 。
一、氢燃料的制备
(1)我国氢气的主要来源是焦炉气制氢,所制得的氢气含有较多的CO和H2S,中温干法脱硫是用氧化铁将硫元素转化为硫化铁。干法脱硫的反应方程式为
(2)我国科研人员用木屑水蒸气气化制取氢燃料,在一定条件下,反应器中存在如下反应:
i.CO2 (g) +C(s)=2CO (g) △H1
ii.C(s) + H2O(g)=CO ( g) + H2 (g) △H2
iii.C(s) + 2H2 (g)=CH4( g) △H3
iv.CO(g) + H2O(g)=CO2 ( g) + H2 (g) △H4
v. CH4(g)+ 2 H2O(g)= CO2 ( g) + 4H2 (g) △H5
①△H5=
②研究中 CaO 的添加量按照CaO 中所含的Ca 和松木屑所含碳的物质的量比确定,在750℃,控制水蒸气流量为 0.lg/(min•g)下,探究催化剂加入量对产气组分和气化性能的影响,结果如表所示:
| n(Ca)/n(C) | 气体体积分数 | 碳转化率/% | |||
| H2 | CO | CO2 | CH4 | ||
| 0 | 45.58 | 22.70 | 22.37 | 7.54 | 61.22 |
| 0.5 | 52.95 | 21.74 | 19.11 | 5.14 | 56.59 |
| 1.0 | 58.62 | 22.37 | 12.60 | 5.31 | 61.42 |
| 温度/℃ | 气体体积分数 | 碳转化率/% | ||
| H2 | CO | CO2 | ||
| 700 | 51.78 | 20.75 | 19.89 | 54.37 |
| 750 | 58.62 | 22.37 | 12.60 | 61.42 |
| 800 | 55.63 | 26.05 | 12.71 | 73.43 |
| 850 | 54.16 | 26.94 | 13.82 | 83.34 |
③从产氢率的角度考虑,最佳操作温度是
④随着反应的进行,发现 CaO 的吸收能力逐渐降低,原因是
二、氢燃料的存储
(3)将氢气储存于液体燃料中,可以解决氢气的安全高效存储和运输问题。由于甲醇具有单位体积储氢量高、活化温度低等优点,是理想的液体储氢平台分子。我国学者构建一种双功能结构的催化剂,反应过程中,在催化剂的表面同时活化水和甲醇。如图是甲醇脱氢转化的反应历程( TS 表示过渡态)。

根据图象判断甲醇脱氢反应中断裂的化学键是
三、氢燃料的应用。一种氢能电池的原理如图:

(4)正极的电极反应式为
您最近半年使用:0次
2020-05-15更新
|
163次组卷
|
4卷引用:河南省郑州市2020届高三第二次质检理综试卷
4 . 能源、资源、环境日益成为人们关注的主题。
(1)近日习近平向2019世界新能源汽车大会致贺信,为发展氢能源,必须制得廉价氢气。下列可供开发又较经济的一种制氢方法是_______ (填写编号)
①电解水 ②锌和稀硫酸反应 ③利用太阳能,光解海水
(2)某同学用铜和硫酸做原料,设计了两种制取硫酸铜的方案:
方案①:铜与浓硫酸加热直接反应,即Cu→CuSO4
方案②:铜在空气中加热再与稀硫酸反应,即Cu→CuO→CuSO4
这两种方案,你认为哪一种方案更合理并简述理由_______ 。
(3)海带中含有丰富的碘元素.从海带中提取碘单质的工业生产流程如图所示.
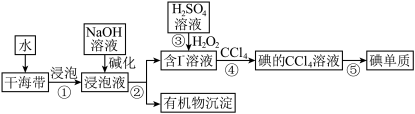
步骤③中双氧水在酸性条件下氧化碘离子的离子方程式是_______ ,步骤④除了CCl4 还可以选用的萃取剂是_______ (填序号)。
a.苯 b.乙醇 c.乙酸 d.乙烷
(1)近日习近平向2019世界新能源汽车大会致贺信,为发展氢能源,必须制得廉价氢气。下列可供开发又较经济的一种制氢方法是
①电解水 ②锌和稀硫酸反应 ③利用太阳能,光解海水
(2)某同学用铜和硫酸做原料,设计了两种制取硫酸铜的方案:
方案①:铜与浓硫酸加热直接反应,即Cu→CuSO4
方案②:铜在空气中加热再与稀硫酸反应,即Cu→CuO→CuSO4
这两种方案,你认为哪一种方案更合理并简述理由
(3)海带中含有丰富的碘元素.从海带中提取碘单质的工业生产流程如图所示.

步骤③中双氧水在酸性条件下氧化碘离子的离子方程式是
a.苯 b.乙醇 c.乙酸 d.乙烷
您最近半年使用:0次
5 . 随着能源问题的进一步突出,利用热化学循环制氢的研究受到许多发达国家的青睐。最近的研究发现,复合氧化物铁酸锰(MnFe2O4)也可以用于热化学循环分解水制氢,MnFe2O4的制备流程如下:
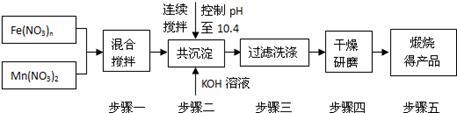
(1)原料Fe(NO3)n中n=____ ,投入原料Fe(NO3)n和Mn(NO3)2的物质的量之比应为______ 。
(2)步骤二中“连续搅拌”的目的是______ ;步骤三中洗涤干净的标准是__________ 。
(3)利用MnFe2O4热化学循环制氢的反应可表示为:
MnFe2O4 MnFe2O4-x+
MnFe2O4-x+ O2↑
O2↑
MnFe2O4-x+xH2O=MnFe2O4+xH2↑
请认真分析上述两个反应并回答下列问题:
①若MnFe2O4-x中x=0.8,则MnFe2O4-x中Fe2+占全部铁元素的百分比为_______ 。
②该热化学循环法制氢的优点有(答两点即可)_________________ 。
③该热化学循环法制氢尚有不足之处,进一步改进的研究方向是_____________________ 。

(1)原料Fe(NO3)n中n=
(2)步骤二中“连续搅拌”的目的是
(3)利用MnFe2O4热化学循环制氢的反应可表示为:
MnFe2O4
 MnFe2O4-x+
MnFe2O4-x+ O2↑
O2↑MnFe2O4-x+xH2O=MnFe2O4+xH2↑
请认真分析上述两个反应并回答下列问题:
①若MnFe2O4-x中x=0.8,则MnFe2O4-x中Fe2+占全部铁元素的百分比为
②该热化学循环法制氢的优点有(答两点即可)
③该热化学循环法制氢尚有不足之处,进一步改进的研究方向是
您最近半年使用:0次
2015-06-15更新
|
253次组卷
|
5卷引用:2011届吉林省高考复习质量监测(理综)化学部分
(已下线)2011届吉林省高考复习质量监测(理综)化学部分(已下线)2011届陕西省西安中学高三第十三次模拟考试(理综)化学试题(已下线)2014届高考化学二轮冲刺非选择题增分专练 化学工艺流程练习卷2015届东北三省三校高三第二次高考模拟考试 理综化学试卷河南省许昌市第三高级中学2019-2020学年高一下学期期末考试化学试题



