名校
解题方法
1 . 食盐是日常生活的必需品,也是重要的化工原料。试剂级NaCl可用海盐(含泥沙、海藻、K+、Ca2+、Mg2+、Fe3+、SO 等杂质)为原料制备。实验室提纯NaCl的流程如图:
等杂质)为原料制备。实验室提纯NaCl的流程如图:
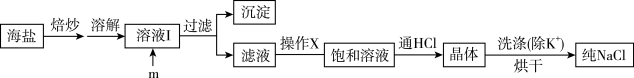
提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、75%乙醇、四氯化碳
(1)欲除去溶液I中的Ca2+、Mg2+、Fe3+、 ,在提供的试剂中,选出m所代表的试剂,按滴加顺序依次为
,在提供的试剂中,选出m所代表的试剂,按滴加顺序依次为_______ 、NaOH、_______ (只填化学式);洗涤除去NaCl晶体表面附带的少量KCl,在提供的试剂中,选用的试剂为_______ 。
(2)操作X为用提纯的NaCl配制500mL 4.00mol/L NaCl溶液,所用的玻璃仪器除烧杯、玻璃棒外还有_______ (填仪器名称)
(3)用如图所示装置,以焙炒后的海盐为原料制备HCl气体,并通入NaCl饱和溶液中使NaCl结晶析出。
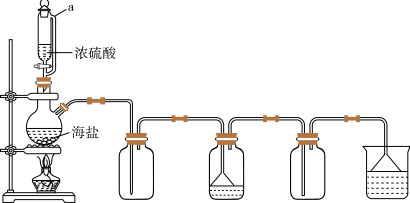
①用浓硫酸和海盐混合加热制取氯化氢利用了浓硫酸的性质是_______ (填编号),相比分液漏斗,选用仪器a的优点是_______ 。
a.高沸点 b.强酸性 c.强氧化性
②对比实验发现,将烧瓶中的海盐磨细可加快NaCl晶体的析出,其原因是_______ 。
(4)设计实验测定NaCl产品中SO 的含量,填写表格。
的含量,填写表格。
 等杂质)为原料制备。实验室提纯NaCl的流程如图:
等杂质)为原料制备。实验室提纯NaCl的流程如图:
提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、75%乙醇、四氯化碳
(1)欲除去溶液I中的Ca2+、Mg2+、Fe3+、
 ,在提供的试剂中,选出m所代表的试剂,按滴加顺序依次为
,在提供的试剂中,选出m所代表的试剂,按滴加顺序依次为(2)操作X为用提纯的NaCl配制500mL 4.00mol/L NaCl溶液,所用的玻璃仪器除烧杯、玻璃棒外还有
(3)用如图所示装置,以焙炒后的海盐为原料制备HCl气体,并通入NaCl饱和溶液中使NaCl结晶析出。

①用浓硫酸和海盐混合加热制取氯化氢利用了浓硫酸的性质是
a.高沸点 b.强酸性 c.强氧化性
②对比实验发现,将烧瓶中的海盐磨细可加快NaCl晶体的析出,其原因是
(4)设计实验测定NaCl产品中SO
 的含量,填写表格。
的含量,填写表格。| 操作 | 目的/结论 | |
| ① | 称取样品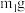 ,加水溶解,加盐酸调至弱酸性,滴加过量c1mol/LBaCl2溶液V1mL ,加水溶解,加盐酸调至弱酸性,滴加过量c1mol/LBaCl2溶液V1mL | 目的: |
| ② | 过滤洗涤,干燥后称得沉淀为m2g | 结论:样品中SO 的质量分数为 的质量分数为 |
您最近一年使用:0次
2021-04-11更新
|
275次组卷
|
3卷引用:上海市青浦区2021届高三等级考二模化学试题
解题方法
2 . 海水中化学资源的综合开发利用,已受到各国的高度重视。Br2和Mg等两种单质都可以从海水中提取,如图为提取它们的主要步骤:

请回答:
Ⅰ.从海水中提取的溴占世界溴年产量的三分之一,主要方法就是上述流程中的空气吹出法。
(1)吸收塔中反应的离子方程式是______ ,工业生产1mol高浓度Br2,理论上需要Cl2的物质的量为______ 。
(2)10L海水经过提纯浓缩,向吸收塔吸收后的溶液中加入0.100mol/LAgNO3溶液8.0mL恰好完全反应,则海水中含溴的含量为______ mg/L(不考虑提纯过程中溴的损失)。
Ⅱ.镁及其合金是用途很广的金属材料,而目前世界上60%的镁就是从海水中按上述流程提取的。
(1)上述流程中为了使MgSO4完全转化为Mg(OH)2,试剂①可以选用______ (写化学式)。
(2)步骤①包括______ 、______ 、过滤、洗涤、干燥。
(3)通电时无水MgCl2在熔融状态下反应的化学方程式是______ 。

请回答:
Ⅰ.从海水中提取的溴占世界溴年产量的三分之一,主要方法就是上述流程中的空气吹出法。
(1)吸收塔中反应的离子方程式是
(2)10L海水经过提纯浓缩,向吸收塔吸收后的溶液中加入0.100mol/LAgNO3溶液8.0mL恰好完全反应,则海水中含溴的含量为
Ⅱ.镁及其合金是用途很广的金属材料,而目前世界上60%的镁就是从海水中按上述流程提取的。
(1)上述流程中为了使MgSO4完全转化为Mg(OH)2,试剂①可以选用
(2)步骤①包括
(3)通电时无水MgCl2在熔融状态下反应的化学方程式是
您最近一年使用:0次
3 . 海洋是资源的宝库,海水中含量最高的金属元素是
| A.Na | B.Ca | C.Mg | D.Cu |
您最近一年使用:0次
2014·河北唐山·二模
解题方法
4 . 海水是巨大的资源宝库,下列说法正确的是
| A.碘元素又称“海洋元素” |
| B.镁是海水中含量最多的金属元素 |
| C.从海水中提取食盐和碘的过程都是物理变化 |
| D.氯碱工业和纯碱工业的原料都有食盐 |
您最近一年使用:0次



