在工农业生产生活中都有重要的用途。某化学研究小组设计如下过程,请你参与探究,回答相关问题。
在工农业生产生活中都有重要的用途。某化学研究小组设计如下过程,请你参与探究,回答相关问题。I.
 的性质探究
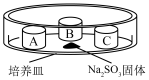
的性质探究装置如下表(图)所示,培养皿中A、B、C三个塑料瓶盖内盛有不同物质。向
 固体上滴加
固体上滴加 硫酸,迅速用玻璃片将培养皿盖严,实验现象记录如下。
硫酸,迅速用玻璃片将培养皿盖严,实验现象记录如下。实验装置 | 㼛盖 | 物质 | 实验现象 |
| A | 蒸馏水 | 无明显变化 |
B |
| 溶液褪色 | |
C | 蘸有品红溶液的棉花 | 品红溶液褪色 |
(1)70%浓硫酸溶液和
 固体反应制备
固体反应制备 的化学方程式为
的化学方程式为(2)瓶盖A中发生反应的化学方程式为
(3)瓶盖A中无明显变化,若要证明A中发生了化学反应,可先在蒸馏水中滴入少量试剂X,X是
a.
 溶液 b.
溶液 b. 溶液 c.石蕊溶液
溶液 c.石蕊溶液(4)瓶盖
 具有还原性,反应的离子方程式为
具有还原性,反应的离子方程式为(5)综合上述实验信息可证明
 具有还原性、
具有还原性、(6)增加瓶盖D可验证
 具有氧化性,则D中盛装的试剂及现象是
具有氧化性,则D中盛装的试剂及现象是II.化石燃料燃烧会产生大量的
 ,造成环境污染,某化学研究小组设计如下表列出的3种燃煤烟气脱硫方法的原理。
,造成环境污染,某化学研究小组设计如下表列出的3种燃煤烟气脱硫方法的原理。方法1 | 用氨水将 转化为 转化为 ,再氧化成 ,再氧化成 |
方法2 | 用生物质热解气(主要成分 、 、 、 、 )将 )将 在高温下还原成单质硫,其他生成物均可直接排放 在高温下还原成单质硫,其他生成物均可直接排放 |
方法3 | 用 溶液吸收 溶液吸收 ,再经电解转化为 ,再经电解转化为 |
(7)如果不对燃煤烟气脱硫,易形成硫酸型酸雨,酸雨一般指的是
 小于
小于(8)方法I中氨水吸收燃煤烟气中
 的化学反应为:
的化学反应为: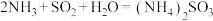 、
、(9)方法II中用
 将
将 还原为S时,
还原为S时, 转化为
转化为(10)对方法III吸收
 后的溶液加热可使吸收液再生,其反应属于基本反应类型中的
后的溶液加热可使吸收液再生,其反应属于基本反应类型中的
更新时间:2024-01-17 09:04:47
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】门捷列夫在研究周期表时预言了“类硅”元素锗和“类铝”元素镓等11种元素。锗及其化合物应用于航空航天测控、光纤通讯等领域。一种提纯二氧化锗粗品(主要含GeO2、As2O3)的工艺如图:

已知:ⅰ.GeO2与碱反应生成Na2GeO3.
ⅱ.GeCl4极易水解,GeCl4沸点86.6℃。
ⅲ.As位于同主族P的下一周期,As2O3+2NaOH =2NaAsO2+H2O。
(1)Ge位于同主族Si的下一周期,则Ge核外电子排布式为_______ 。
(2)Ge为共价晶体,其晶胞与金刚石晶胞相似,则一个晶胞中含有_______ 个Ge原子。
(3)“氧化”过程是将NaAsO2氧化为Na3AsO4,其离子方程式为_______ 。
(4)AsH3的中心原子轨道杂化为_______ 。AsH3的沸点比NH3低的原因_______ 。
(5)盐酸蒸馏生成GeCl4,反应的化学方程式为_______ 。
(6)高纯二氧化锗的含量采用碘酸钾滴定法进行测定。称取ag高纯二氧化锗样品,加入氢氧化钠在电炉溶解,用次亚磷酸钠还原为Ge2+,以淀粉为指示剂,用bmol/L的碘酸钾标准溶液滴定,消耗碘酸钾的体积为V mL。(20℃以下,次亚磷酸钠不会被碘酸钾和碘氧化)
资料:3Ge2++IO +6H+ = 3Ge4++I-+3H2O,IO
+6H+ = 3Ge4++I-+3H2O,IO +5I-+6H+ = 3I2+3H2O。
+5I-+6H+ = 3I2+3H2O。
此样品中二氧化锗的质量分数是_______ (用表达式表示)。

已知:ⅰ.GeO2与碱反应生成Na2GeO3.
ⅱ.GeCl4极易水解,GeCl4沸点86.6℃。
ⅲ.As位于同主族P的下一周期,As2O3+2NaOH =2NaAsO2+H2O。
(1)Ge位于同主族Si的下一周期,则Ge核外电子排布式为
(2)Ge为共价晶体,其晶胞与金刚石晶胞相似,则一个晶胞中含有
(3)“氧化”过程是将NaAsO2氧化为Na3AsO4,其离子方程式为
(4)AsH3的中心原子轨道杂化为
(5)盐酸蒸馏生成GeCl4,反应的化学方程式为
(6)高纯二氧化锗的含量采用碘酸钾滴定法进行测定。称取ag高纯二氧化锗样品,加入氢氧化钠在电炉溶解,用次亚磷酸钠还原为Ge2+,以淀粉为指示剂,用bmol/L的碘酸钾标准溶液滴定,消耗碘酸钾的体积为V mL。(20℃以下,次亚磷酸钠不会被碘酸钾和碘氧化)
资料:3Ge2++IO
 +6H+ = 3Ge4++I-+3H2O,IO
+6H+ = 3Ge4++I-+3H2O,IO +5I-+6H+ = 3I2+3H2O。
+5I-+6H+ = 3I2+3H2O。此样品中二氧化锗的质量分数是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】纳米氧化镁是在磁性、催化方面有许多特异功能的新材料,具有重要价值。工业以菱镁矿(主要成分为MgCO3,少量FeCO3和SiO2杂质)为原料制备纳米氧化镁工艺流程如图:

试回答下列问题:
(1)“焙烧”时生成的主要气体有___ ;滤渣I的主要成分为___ 。
(2)氧化剂常用空气或H2O2而不选用酸性KMnO4,解释其原因__ 。
已知在该条件下金属离子开始沉淀和完全沉淀的pH如表:
上述流程中“氧化”是否可省掉及理由是___ 。
(3)试剂a可能是__ 。
(4)资料显示煅烧MgCO3比煅烧Mg(OH)2更容易生成MgO纳米材料。“沉淀”时若将NH4HCO3更换成Na2CO3,则产生的后果是__ 。
(5)该流程中可以循环利用的物质是__ 。

试回答下列问题:
(1)“焙烧”时生成的主要气体有
(2)氧化剂常用空气或H2O2而不选用酸性KMnO4,解释其原因
已知在该条件下金属离子开始沉淀和完全沉淀的pH如表:
| 金属离子 | Fe2+ | Fe3+ | Mg2+ |
| 开始沉淀pH | 6.3 | 1.5 | 8.9 |
| 完全沉淀pH | 9.0 | 2.8 | 10.9 |
(3)试剂a可能是
(4)资料显示煅烧MgCO3比煅烧Mg(OH)2更容易生成MgO纳米材料。“沉淀”时若将NH4HCO3更换成Na2CO3,则产生的后果是
(5)该流程中可以循环利用的物质是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】根据文字信息书写相应的方程式。
(1)PH3有剧毒,用硫酸铜溶液吸收,生成物含Cu3P沉淀、磷酸,反应的离子方程式为____ 。
(2)二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的消毒剂。工业上用潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得,反应过程中还有CO2等生成,且n(CO2):n(ClO2)=1:2。该反应的化学方程式是____ 。
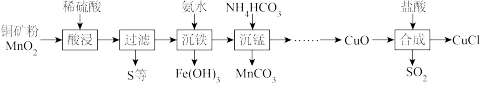
(3)CuCl难溶于水,常用作有机合成催化剂,实验室以铜矿粉(主要含Cu2S及少量Fe2O3、FeCO3等)为原料制备CuCl的流程如图:
①“酸浸”时,Cu2S所发生反应的离子方程式为____ 。
②“沉锰”时有CO2气体放出,该反应的化学方程式为____ 。
③“合成”反应的化学方程式为____ 。
(1)PH3有剧毒,用硫酸铜溶液吸收,生成物含Cu3P沉淀、磷酸,反应的离子方程式为
(2)二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒的消毒剂。工业上用潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得,反应过程中还有CO2等生成,且n(CO2):n(ClO2)=1:2。该反应的化学方程式是
(3)CuCl难溶于水,常用作有机合成催化剂,实验室以铜矿粉(主要含Cu2S及少量Fe2O3、FeCO3等)为原料制备CuCl的流程如图:

①“酸浸”时,Cu2S所发生反应的离子方程式为
②“沉锰”时有CO2气体放出,该反应的化学方程式为
③“合成”反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某化学小组拟探究 能否与可溶性钡的强酸盐反应生成
能否与可溶性钡的强酸盐反应生成 沉淀,用下图所示装置进行实验(夹持、加热装置已略,气密性已检验)。
沉淀,用下图所示装置进行实验(夹持、加热装置已略,气密性已检验)。
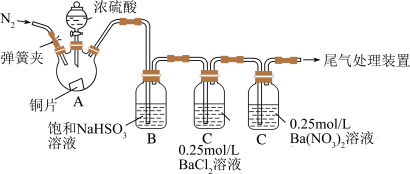
实验操作和现象如下:
Ⅰ.关闭弹簧夹,滴加一定量的浓硫酸并加热,A中有白雾生成,铜片表面产生气泡;C中有气泡冒出,产生少量白色沉淀;D中产生大量白色沉淀,液面上方略显浅棕色并逐渐消失。
Ⅱ.从C、D中分别取少量白色沉淀,加稀盐酸,白色沉淀不溶解。
(1)A中发生反应的化学方程式为_______ 。
(2)B装置的作用是_______ 。
(3)分析C中产生少量不溶于稀盐酸的沉淀的原因_______ 。
(4)D中液面上方生成浅棕色气体的化学方程式为_______ 。
(5)为了验证上述分析是否正确,在原实验基础上应增加一步操作,该操作是_______ 。
(6)增加以上操作后,重复实验,发现C中无沉淀生成,而D中仍产生白色沉淀。用离子方程式解释D中仍有白色沉淀的原因_______ 。
(7)由以上实验可得出结论: 与可溶性钡的强酸盐
与可溶性钡的强酸盐_______ (填“能”或“不能”)反应生成 沉淀。
沉淀。
 能否与可溶性钡的强酸盐反应生成
能否与可溶性钡的强酸盐反应生成 沉淀,用下图所示装置进行实验(夹持、加热装置已略,气密性已检验)。
沉淀,用下图所示装置进行实验(夹持、加热装置已略,气密性已检验)。
实验操作和现象如下:
Ⅰ.关闭弹簧夹,滴加一定量的浓硫酸并加热,A中有白雾生成,铜片表面产生气泡;C中有气泡冒出,产生少量白色沉淀;D中产生大量白色沉淀,液面上方略显浅棕色并逐渐消失。
Ⅱ.从C、D中分别取少量白色沉淀,加稀盐酸,白色沉淀不溶解。
(1)A中发生反应的化学方程式为
(2)B装置的作用是
(3)分析C中产生少量不溶于稀盐酸的沉淀的原因
(4)D中液面上方生成浅棕色气体的化学方程式为
(5)为了验证上述分析是否正确,在原实验基础上应增加一步操作,该操作是
(6)增加以上操作后,重复实验,发现C中无沉淀生成,而D中仍产生白色沉淀。用离子方程式解释D中仍有白色沉淀的原因
(7)由以上实验可得出结论:
 与可溶性钡的强酸盐
与可溶性钡的强酸盐 沉淀。
沉淀。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去)。化合物B在常温常压下为气体,B和C的相对分子质量之比为4∶5,化合物D是重要的工业原料。

(1)写出B与足量硝酸钡溶液反应的离子方程式:___________ 。
(2)写出E与A的氢化物反应生成A的化学方程式:________ 。
(3)将5 mL 0.10 mol·L-1的E溶液与10 mL 0.10 mol·L-1的NaOH溶液混合。反应后溶液的pH______ 7(填“大于”、“小于”或“等于”),理由用离子方程式表示_______________ ;

(1)写出B与足量硝酸钡溶液反应的离子方程式:
(2)写出E与A的氢化物反应生成A的化学方程式:
(3)将5 mL 0.10 mol·L-1的E溶液与10 mL 0.10 mol·L-1的NaOH溶液混合。反应后溶液的pH
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】某同学为了验证硫铁矿(主要成分为FeS2。含有少量的碳)焙烧产物(产生的气体是SO2,CO2),设计如下装置进行实验:
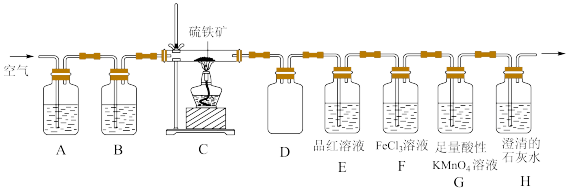
回答下列问题:
(1)装置A、B中的试剂分别是_______ 、_______ 。
(2)装置D的作用是_______ 。
(3)验证焙烧后气体产物的实验现象分别为_______ 、_______ ;若F中颜色发生改变,写出产生颜色变化反应的离子方程式:_______ 。取F中反应后的溶液于洁净的试管中。滴加少量KSCN溶液,溶液不变红,说明溶液中_______ (填“含有”或“不含有”)Fe3+;再继续滴加少量氯水,溶液也不变红。产生这种现象的原因可能是_______ 。
(4)G中盛放足量酸性KMnO4溶液的目的是_______ (用离子方程式表示)。
(5)反应完成后经检验,C中剩余固体物质只有Fe2O3,写出FeS2焙烧反应的化学方程式:_______ 。

回答下列问题:
(1)装置A、B中的试剂分别是
(2)装置D的作用是
(3)验证焙烧后气体产物的实验现象分别为
(4)G中盛放足量酸性KMnO4溶液的目的是
(5)反应完成后经检验,C中剩余固体物质只有Fe2O3,写出FeS2焙烧反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某化学小组为了证明二氧化硫和氯气的漂白性,设计了如下图所示的实验装置:

他们制备二氧化硫和氯气所依据的原理分别是:
Na2SO3+H2SO4 = Na2SO4+H2O+SO2↑
MnO2+4HCl(浓) MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
(1)用来制取氯气的装置是______ (填字母),反应中浓盐酸所表现出________________ 性质。
(2)反应开始一段时间后,B、D试管中的品红溶液均褪色。停止通气后,再给B、D两个试管分别加热____ (填" B”或“D")试管中无明显现象。
(3)装置C的作用是________________________ ;
(4)若装置D中的品红溶液换成紫色的石蕊溶液,则出现的现象是____________________________ ;
(5)该小组同学将两种气体混合后通入品红溶液,一段时间后,品红溶液几乎不褪色。查阅资料得知:两种气体按体积比1:1混合,再与水反应可生成两种常见的酸,因而失去漂白作用,该反应的化学方程式是:________________________________ 。

他们制备二氧化硫和氯气所依据的原理分别是:
Na2SO3+H2SO4 = Na2SO4+H2O+SO2↑
MnO2+4HCl(浓)
 MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑(1)用来制取氯气的装置是
(2)反应开始一段时间后,B、D试管中的品红溶液均褪色。停止通气后,再给B、D两个试管分别加热
(3)装置C的作用是
(4)若装置D中的品红溶液换成紫色的石蕊溶液,则出现的现象是
(5)该小组同学将两种气体混合后通入品红溶液,一段时间后,品红溶液几乎不褪色。查阅资料得知:两种气体按体积比1:1混合,再与水反应可生成两种常见的酸,因而失去漂白作用,该反应的化学方程式是:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某学习小组欲利用如下装置制备SO2,并检验SO2的性质和制取食品抗氧化剂焦亚硫酸钠(Na2S2O5)。
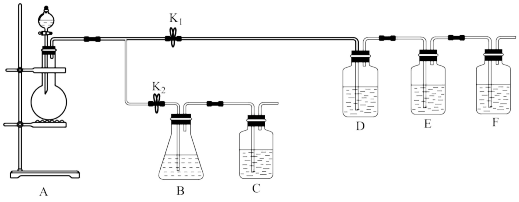
(1)检查A装置气密性的方法是___________ 。
(2)用A装置制备SO2,最适宜的试剂为___________ (填序号)。
a.10%硫酸、Na2SO3固体 b.98%浓硫酸、铜片
c.70%浓硫酸、Na2SO3固体 d.60%浓硝酸、Na2SO3固体
(3)加好药品,打开K1、关闭K2。已知:E装置中盛放FeCl3和BaCl2的混合溶液。
①若D装置的作用是检验SO2的漂白性,则D装置中通常盛放的试剂是___________ 。
②用离子方程式表示E装置中发生的反应:___________ 。
③C装置的作用是___________ 。F装置中可选用的试剂是___________ (填序号)。
a.浓硫酸 b.氢氧化钠溶液 c.酸性高锰酸钾溶液
(4)B装置中盛放的是Na2SO3饱和溶液。打开K2、关闭K1一段时间后B装置中有Na2S2O5晶体析出,B装置中发生反应的化学方程式为___________ 。

(1)检查A装置气密性的方法是
(2)用A装置制备SO2,最适宜的试剂为
a.10%硫酸、Na2SO3固体 b.98%浓硫酸、铜片
c.70%浓硫酸、Na2SO3固体 d.60%浓硝酸、Na2SO3固体
(3)加好药品,打开K1、关闭K2。已知:E装置中盛放FeCl3和BaCl2的混合溶液。
①若D装置的作用是检验SO2的漂白性,则D装置中通常盛放的试剂是
②用离子方程式表示E装置中发生的反应:
③C装置的作用是
a.浓硫酸 b.氢氧化钠溶液 c.酸性高锰酸钾溶液
(4)B装置中盛放的是Na2SO3饱和溶液。打开K2、关闭K1一段时间后B装置中有Na2S2O5晶体析出,B装置中发生反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某学习小组开展下列实验探究活动证明亚硫酸的酸性强于次氯酸:
(1)图一装置A中反应的化学方程式为_____________________ 。
(2)如果利用图一装置A中产生的气体去证明+4价硫具有氧化性,可将气体通入________ (填序号)来证明。
M.H2S溶液 N.Na2S溶液 O.NaOH溶液 P.品红溶液
(3)选用下面的装置和药品探究亚硫酸与次氯酸的酸性强弱:
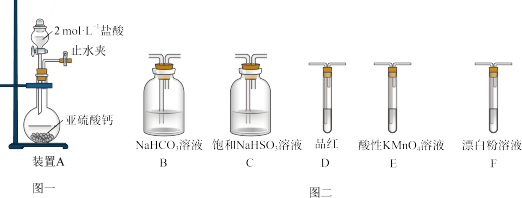
装置连接顺序为A、C、___________ 、__________ 、D、F,其中装置 C的作用是_______ ,通过_________________ 现象即可证明亚硫酸的酸性强于次氯酸。
(1)图一装置A中反应的化学方程式为
(2)如果利用图一装置A中产生的气体去证明+4价硫具有氧化性,可将气体通入
M.H2S溶液 N.Na2S溶液 O.NaOH溶液 P.品红溶液
(3)选用下面的装置和药品探究亚硫酸与次氯酸的酸性强弱:

装置连接顺序为A、C、
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】为探究H2O2、SO2、Br2氧化性强弱,某小组同学设计如下实验(夹持及尾气处理装置已略去,气密性已检验)。

(1)A中发生反应的化学方程式是___________ 。
实验室中常常利用氢氧化钠溶液吸收SO2的离子方式:___________ 。
(2)甲同学通过C中产生白色沉淀,得出结论,氧化性:H2O2>SO2。
①乙同学认为不能得出此结论,认为在滴加浓硫酸之前应增加一步操作,该操作是___________ 。
②将乙和丙同学改进后的方案进行实验,C中产生白色沉淀,得出结论:氧化性H2O2>SO2。
(3)iii中滴入少量H2O2没有明显变化。提出假设:
观点1:H2O2的量少不能氧化Br—
观点2:B中有未反应H2SO3
为验证观点2,应进行的实验操作及现象是___________ 。
(4)通过上述全部实验,得出结论:H2O2、SO2、Br2氧化性由强到弱的顺序是___________ 。

| 实验操作 | 实验现象 |
| i.打开A中分液漏斗活塞,滴加浓硫酸 | A中有气泡产生,B中红棕色溴水褪色,C中有白色沉淀 |
| ii.取C中沉淀加入盐酸 | C中白色沉淀不溶解 |
| iii.打开B中分液漏斗活塞,逐滴滴加H2O2 | 开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成红棕色 |
实验室中常常利用氢氧化钠溶液吸收SO2的离子方式:
(2)甲同学通过C中产生白色沉淀,得出结论,氧化性:H2O2>SO2。
①乙同学认为不能得出此结论,认为在滴加浓硫酸之前应增加一步操作,该操作是
②将乙和丙同学改进后的方案进行实验,C中产生白色沉淀,得出结论:氧化性H2O2>SO2。
(3)iii中滴入少量H2O2没有明显变化。提出假设:
观点1:H2O2的量少不能氧化Br—
观点2:B中有未反应H2SO3
为验证观点2,应进行的实验操作及现象是
(4)通过上述全部实验,得出结论:H2O2、SO2、Br2氧化性由强到弱的顺序是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某校化学兴趣小组学习了“氯气的实验室制法”后,利用如图所示实验装置对 的制备及性质进行探究。回答下列问题:
的制备及性质进行探究。回答下列问题:
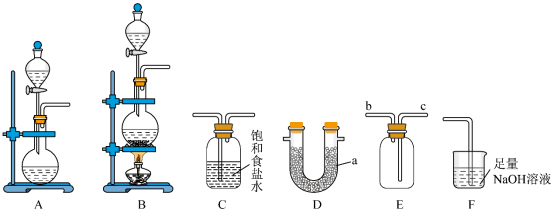
(1)仪器 的名称为
的名称为___________ 。
(2)实验室若选用 固体和浓盐酸在常温条件下制取干燥的
固体和浓盐酸在常温条件下制取干燥的 ,则选用的发生装置为
,则选用的发生装置为___________ (填“A”或“B”);该反应的化学方程式为___________ 。
(3)装置C的主要作用为___________ ;装置 是用于干燥
是用于干燥 ,故装置
,故装置 中的试剂为
中的试剂为___________ (填化学式)。
(4)用装置 收集
收集 ,进气口为
,进气口为___________ (填“b”或“c”)。
(5)装置F中发生反应的离子方程式为___________ 。
(6)工业上一般将 通入石灰乳中制取含氯漂白粉,同学们利用如下图装置进行实验。
通入石灰乳中制取含氯漂白粉,同学们利用如下图装置进行实验。
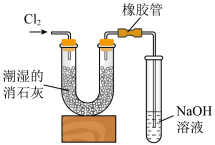
已知:① 与潮湿的消石灰反应是放热反应;
与潮湿的消石灰反应是放热反应;
②温度较高时, 与潮湿
与潮湿 的反应方程式为
的反应方程式为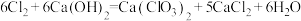 。
。
发现实验所得 产率较低,可能的原因是
产率较低,可能的原因是___________ 。
 的制备及性质进行探究。回答下列问题:
的制备及性质进行探究。回答下列问题:
(1)仪器
 的名称为
的名称为(2)实验室若选用
 固体和浓盐酸在常温条件下制取干燥的
固体和浓盐酸在常温条件下制取干燥的 ,则选用的发生装置为
,则选用的发生装置为(3)装置C的主要作用为
 是用于干燥
是用于干燥 ,故装置
,故装置 中的试剂为
中的试剂为(4)用装置
 收集
收集 ,进气口为
,进气口为(5)装置F中发生反应的离子方程式为
(6)工业上一般将
 通入石灰乳中制取含氯漂白粉,同学们利用如下图装置进行实验。
通入石灰乳中制取含氯漂白粉,同学们利用如下图装置进行实验。
已知:①
 与潮湿的消石灰反应是放热反应;
与潮湿的消石灰反应是放热反应;②温度较高时,
 与潮湿
与潮湿 的反应方程式为
的反应方程式为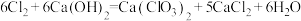 。
。发现实验所得
 产率较低,可能的原因是
产率较低,可能的原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某课外小组在实验室制备氨气,并进行有关氮气的性质探究。
(1)该小组同学加热生石灰与氯化铵的混合物制取并收集干燥的氨气。

①应该选用的仪器及装置有(填字母)___________ 。
②生石灰与氯化铵反应生成氨气的化学方程式为___________ 。
(2)该小组同学设计如图所示装置探究氨气的还原性。
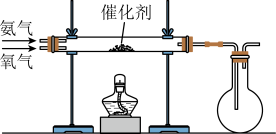
将催化剂加热至红热,撤去酒精灯,可观察到催化剂继续保持红热,有红棕色气体产生及少量白烟生成,在上述过程会同时发生多个反应,根据现象判断氨气的催化氧化为___________ (放热或吸热)反应,白烟的化学式为___________ 。
(3)该小组同学以氨气和二氧化碳为原料制备碳酸氢铵。
①甲同学先将二氧化碳通入水中,充分溶解后,再通入氨气;乙同学先将氨气通入水中,充分溶解后,再通入二氧化碳。合适的方案是___________ (填“甲”或“乙”);
②检验产物中有 的方法为
的方法为___________ 。
(1)该小组同学加热生石灰与氯化铵的混合物制取并收集干燥的氨气。

①应该选用的仪器及装置有(填字母)
②生石灰与氯化铵反应生成氨气的化学方程式为
(2)该小组同学设计如图所示装置探究氨气的还原性。

将催化剂加热至红热,撤去酒精灯,可观察到催化剂继续保持红热,有红棕色气体产生及少量白烟生成,在上述过程会同时发生多个反应,根据现象判断氨气的催化氧化为
(3)该小组同学以氨气和二氧化碳为原料制备碳酸氢铵。
①甲同学先将二氧化碳通入水中,充分溶解后,再通入氨气;乙同学先将氨气通入水中,充分溶解后,再通入二氧化碳。合适的方案是
②检验产物中有
 的方法为
的方法为
您最近一年使用:0次