水体中过量氨氮(以NH3表示)含量过高会导致水体富营养化。用次氯酸钠除去氨氮的一种原理如图所示。下列说法正确的是
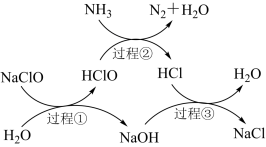

| A.过程①②③均属于氧化还原反应 |
| B.在较高温度下,氨氮去除率会降低 |
| C.每生成一个N2分子,转移6个电子 |
D.过程②中氧化剂与还原剂的物质的量之比是 |
更新时间:2024-03-19 14:10:35
|
相似题推荐
多选题
|
适中
(0.65)
名校
【推荐1】工业上将Na2CO3和Na2S以1:2的物质的量之比配成溶液,再通入SO2,可制取Na2S2O3,同时放出CO2,在该反应中
| A.硫元素既被氧化又被还原 |
| B.氧化剂与还原剂的物质的量之比为1:2 |
| C.每生成1molNa2S2O3,转移4mol电子 |
| D.当转移8mol电子时,还原产物比氧化产物多1mol |
您最近一年使用:0次
【推荐2】向重铬酸盐酸性溶液中加入乙醚和H2O2,水层发生反应:Cr2O +4H2O2+2H+=2CrO5+5H2O(已知CrO5中Cr的化合价为+6价),乙醚层发生反应:CrO5+(C2H5)2O=CrO5•O(C2H5)2(蓝色)。反应现象为上层出现蓝色,一段时间后溶液蓝色褪去,且水相变为绿色(Cr3+),下列说法正确的是
+4H2O2+2H+=2CrO5+5H2O(已知CrO5中Cr的化合价为+6价),乙醚层发生反应:CrO5+(C2H5)2O=CrO5•O(C2H5)2(蓝色)。反应现象为上层出现蓝色,一段时间后溶液蓝色褪去,且水相变为绿色(Cr3+),下列说法正确的是
 +4H2O2+2H+=2CrO5+5H2O(已知CrO5中Cr的化合价为+6价),乙醚层发生反应:CrO5+(C2H5)2O=CrO5•O(C2H5)2(蓝色)。反应现象为上层出现蓝色,一段时间后溶液蓝色褪去,且水相变为绿色(Cr3+),下列说法正确的是
+4H2O2+2H+=2CrO5+5H2O(已知CrO5中Cr的化合价为+6价),乙醚层发生反应:CrO5+(C2H5)2O=CrO5•O(C2H5)2(蓝色)。反应现象为上层出现蓝色,一段时间后溶液蓝色褪去,且水相变为绿色(Cr3+),下列说法正确的是A.由水层反应可知,氧化性:Cr2O >CrO5 >CrO5 |
| B.乙醚在检验过程中作稳定剂和萃取剂,不可用乙醇代替 |
| C.CrO5•O(C2H5)2中不存在非极性键 |
| D.水相变为绿色的离子反应为4CrO5+12H+=4Cr3++6H2O+7O2↑ |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】某离子反应中涉及H2O、ClO-、NH4+、H+、N2、Cl-六种粒子。其中N2的物质的量随时间变化的曲线如图所示。下列判断正确的是( )


| A.该反应的还原剂是Cl- |
| B.消耗1 mol还原剂,转移3 mol电子 |
| C.氧化剂与还原剂的物质的量之比为2∶3 |
| D.反应后溶液的酸性明显增强 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】铁黄(FeOOH)属于铁基颜料,可用硫酸渣(主要成分为Fe2O3、SiO2) 为原料来制备,工艺流程如图所示。
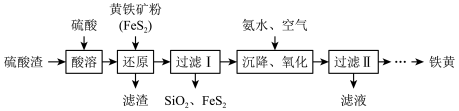
已知:①“还原”时,发生反应: FeS2+Fe3++H2O →SO +Fe2++H+(未配平) ;
+Fe2++H+(未配平) ;
②FeS2不溶于稀H2SO4,可溶于稀硝酸。
下列说法错误的是

已知:①“还原”时,发生反应: FeS2+Fe3++H2O →SO
 +Fe2++H+(未配平) ;
+Fe2++H+(未配平) ;②FeS2不溶于稀H2SO4,可溶于稀硝酸。
下列说法错误的是
| A.FeS2与铁黄中铁元素的化合价不同 |
| B.FeS2溶于稀硝酸时可能生成Fe3+、 NO和S2-等物质 |
| C.“还原”时,氧化产物与还原产物的物质的量之比为2∶15 |
D.“沉降、氧化”时,整个过程可用离子方程式表示如下:4Fe2++ 8NH3·H2O+O2= 8NH +4FeOOH↓+2H2O +4FeOOH↓+2H2O |
您最近一年使用:0次
【推荐1】把碎纸片b、c、d、e补充到a中,可得到一个完整的离子方程式(未配平)。下列说法正确的是


| A.纸条排列的顺序可能是:c、d、a、b、e |
B.通过该反应可知还原性: ClO >SO >SO |
| C.氧化剂与还原剂的物质的量比为2:1 |
| D.每生成1个ClO2,反应转移的电子数为2个 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】实验室既可用浓盐酸与MnO2在加热时反应制备Cl2,也可用KClO3与浓盐酸在常温下反应制备Cl2,下列有关说法中不正确的是
| A.由题目信息知:KClO3的氧化性比MnO2的强 |
| B.制备氯气的整个实验过程中,化学试剂只需要使用氧化剂与还原剂 |
| C.用排气法收集Cl2不需要利用其他试剂就能确定集气瓶中已收集满气体 |
| D.制得等量的Cl2,两种方法转移的电子数相同 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】“84”消毒液、明矾、高铁酸钾 、臭氧等都可以作水处理剂,已知“84”消毒液中的有效成分为
、臭氧等都可以作水处理剂,已知“84”消毒液中的有效成分为 ,下列有关说法错误的是
,下列有关说法错误的是
 、臭氧等都可以作水处理剂,已知“84”消毒液中的有效成分为
、臭氧等都可以作水处理剂,已知“84”消毒液中的有效成分为 ,下列有关说法错误的是
,下列有关说法错误的是A.若有 高铁酸钾转化成氢氧化铁沉淀,则转移 高铁酸钾转化成氢氧化铁沉淀,则转移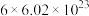 个电子 个电子 |
B.常温常压下,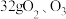 的混合气体所含原子数小于 的混合气体所含原子数小于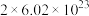 |
C.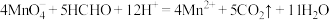 , ,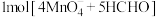 完全反应转移的电子数为 完全反应转移的电子数为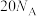 |
D.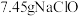 固体中 固体中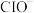 的个数等于 的个数等于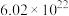 个 个 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】中国科学院科研团队研究表明,在常温常压和可见光下,基于LDH(一种固体催化剂)合成 的原理示意图如图。下列说法不正确的是
的原理示意图如图。下列说法不正确的是

 的原理示意图如图。下列说法不正确的是
的原理示意图如图。下列说法不正确的是
A.该过程可表示为 |
B.该过程中每转移1.2 mol  时,断裂0.6 mol 时,断裂0.6 mol  键 键 |
| C.该过程中,涉及离子键和共价键的断裂与形成 |
D.原料气 可通过分离液态空气获得 可通过分离液态空气获得 |
您最近一年使用:0次

 ,
, ,
, ,
,
 时,转移2个电子
时,转移2个电子
 溶液处理:CH3OH+MnO
溶液处理:CH3OH+MnO +OH-→CO
+OH-→CO +H2O (末配平,下同)
+H2O (末配平,下同)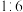


 具有酸性氧化物的性质
具有酸性氧化物的性质 是氧化剂
是氧化剂 处理含
处理含 的废液,反应的离子方程式为:
的废液,反应的离子方程式为: 。下列判断错误的是
。下列判断错误的是


