宏观辨识与微观探析是化学学科核心素养之一。根据所学知识,回答下列问题:
(1)铁的化合物在实际中应用广泛,如氯化铁可用于五金蚀刻、污水处理及作催化剂、凝聚剂等。
①氯化铁常用作印刷电路板的蚀刻剂,写出Cu与 反应的离子方程式:
反应的离子方程式:_______ ;反应后再通入氯气,又可将氯化亚铁转化为氯化铁,则通入氯气后反应的离子方程式为_______ 。
②氯化铁常用于净水,是因为铁离子转化为 胶体,胶体使水中悬浮物聚沉。
胶体,胶体使水中悬浮物聚沉。 胶体分散质粒子直径的范围是
胶体分散质粒子直径的范围是_______ ,检验氢氧化铁胶体是否制备成功常用的方法是_______ 。
(2)用电弧法合成的纳米碳管中常含有大量的杂质碳纳米颗粒,可用氧化气化法提纯,反应的化学方程式为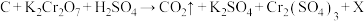 (X中的元素在反应前后未变价,反应未配平)。
(X中的元素在反应前后未变价,反应未配平)。
①该反应中,氧化剂是_______ (填化学式),被氧化的元素是_______ (填元素符号)。
②配平上述方程式:______ 。每生成4.4g  ,该反应转移的电子的物质的量为
,该反应转移的电子的物质的量为______ mol。
(1)铁的化合物在实际中应用广泛,如氯化铁可用于五金蚀刻、污水处理及作催化剂、凝聚剂等。
①氯化铁常用作印刷电路板的蚀刻剂,写出Cu与
 反应的离子方程式:
反应的离子方程式:②氯化铁常用于净水,是因为铁离子转化为
 胶体,胶体使水中悬浮物聚沉。
胶体,胶体使水中悬浮物聚沉。 胶体分散质粒子直径的范围是
胶体分散质粒子直径的范围是(2)用电弧法合成的纳米碳管中常含有大量的杂质碳纳米颗粒,可用氧化气化法提纯,反应的化学方程式为
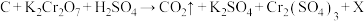 (X中的元素在反应前后未变价,反应未配平)。
(X中的元素在反应前后未变价,反应未配平)。①该反应中,氧化剂是
②配平上述方程式:
 ,该反应转移的电子的物质的量为
,该反应转移的电子的物质的量为
更新时间:2024-04-04 03:41:26
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】“皮鞋很忙”的恶搞段子曾经风靡网络,揭露了某些行业用烂皮鞋制造酸奶或毒胶囊的不法行为。央视《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明胶,出售给浙江绍兴某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬,从而对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)已知Fe(CrO2)2中铁元素是+2价,则其中铬元素是_______ 价。
(2)明胶的水溶液和K2SO4溶液共同具备的性质是_______ (填序号)。
a.都不稳定,密封放置沉淀 b.分散质粒子可通过滤纸 c.丁达尔效应
(3)制备Fe(OH)3胶体的离子方程式_______ 。
(4)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的方法是_______ ,装置是下列中的_______ (填序号)。

(5)现有10 mL明胶的水溶液与5 mL Na2SO4溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明SO 能够透过半透膜:
能够透过半透膜:_______ 。
(1)已知Fe(CrO2)2中铁元素是+2价,则其中铬元素是
(2)明胶的水溶液和K2SO4溶液共同具备的性质是
a.都不稳定,密封放置沉淀 b.分散质粒子可通过滤纸 c.丁达尔效应
(3)制备Fe(OH)3胶体的离子方程式
(4)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的方法是

(5)现有10 mL明胶的水溶液与5 mL Na2SO4溶液混合装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明SO
 能够透过半透膜:
能够透过半透膜:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】现有下列六种物质:①铝 ②Na2CO3 ③CO2 ④H2SO4 ⑤NaOH ⑥红褐色的氢氧化铁胶体
(1)上述物质中属于电解质的有_____________ (填序号)。
(2)写出②在水中的电离方程式:__________________
(3)上述物质中有两种物质在水溶液中发生反应,其离子方程式为H++OH-=H2O, 则该反应的化学方程式为______________________________________________ 。
(4)向⑥的溶液中逐渐滴加④的溶液,看到的现象是_____________________________ 。
(1)上述物质中属于电解质的有
(2)写出②在水中的电离方程式:
(3)上述物质中有两种物质在水溶液中发生反应,其离子方程式为H++OH-=H2O, 则该反应的化学方程式为
(4)向⑥的溶液中逐渐滴加④的溶液,看到的现象是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】现有9种物质:①Na;②盐酸;③NaHCO3;④Cl2;⑤空气;⑥CO2;⑦Fe(OH)3胶体;⑧NaOH;⑨Na2O
(1)属于电解质的是___________ (用序号填空,下同);属于非电解质的是___________ ;属于碱性氧化物的是___________ 。
(2)实验室中少量①通常保存在___________ 中;①在⑤中加热生成的固体颜色是___________ ,化学方程式是___________
(3)将上述物质中的酸性氧化物通入少量的⑧的水溶液中,写出此反应的离子方程式___________ 。
(4)③是一种白色晶体,因受热易分解并产生气体适宜作膨松剂,请写出此物质受热分解的化学方程式___________ 。
(5)向⑦中逐滴滴入过量的②,会出现一系列变化:先出现红褐色沉淀,原因是胶体发生___________ ,随后沉淀溶解,得到黄色溶液,原因___________ (用离子方程式表示)。
(1)属于电解质的是
(2)实验室中少量①通常保存在
(3)将上述物质中的酸性氧化物通入少量的⑧的水溶液中,写出此反应的离子方程式
(4)③是一种白色晶体,因受热易分解并产生气体适宜作膨松剂,请写出此物质受热分解的化学方程式
(5)向⑦中逐滴滴入过量的②,会出现一系列变化:先出现红褐色沉淀,原因是胶体发生
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】连二亚硫酸钠( ),俗称保险粉,易溶于水,常用于印染、纸张漂白等。回答下列问题:
),俗称保险粉,易溶于水,常用于印染、纸张漂白等。回答下列问题:
(1) 中S的化合价为
中S的化合价为_______ 。
(2)向锌粉的悬浮液中通入 ,制备
,制备 ,生成
,生成
 ,反应中转移的电子数为
,反应中转移的电子数为_______ mol;向 溶液中加入适量
溶液中加入适量 ,生成
,生成 并有沉淀产生,该反应的化学方程式为
并有沉淀产生,该反应的化学方程式为_______
 ),俗称保险粉,易溶于水,常用于印染、纸张漂白等。回答下列问题:
),俗称保险粉,易溶于水,常用于印染、纸张漂白等。回答下列问题:(1)
 中S的化合价为
中S的化合价为(2)向锌粉的悬浮液中通入
 ,制备
,制备 ,生成
,生成
 ,反应中转移的电子数为
,反应中转移的电子数为 溶液中加入适量
溶液中加入适量 ,生成
,生成 并有沉淀产生,该反应的化学方程式为
并有沉淀产生,该反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】按要求完成下列各题:
(1)KOH的电子式:____________ , CH(CH3)3的名称为:______________ 。
(2)有五种物质 :①Cu、②H2CO3、③BaSO4、④盐酸、⑤SO2,其中弱电解质是______ (填序号,下同) ,非电解质是________________ 。
(3)钠与水反应的化学方程式为:_____________________ 。
已知在过量的FeSO4溶液中滴入几滴NaClO溶液,并加入过量H2SO4,溶液立即变黄,试写出该反应的离子方程式:_________________________________ 。
(1)KOH的电子式:
(2)有五种物质 :①Cu、②H2CO3、③BaSO4、④盐酸、⑤SO2,其中弱电解质是
(3)钠与水反应的化学方程式为:
已知在过量的FeSO4溶液中滴入几滴NaClO溶液,并加入过量H2SO4,溶液立即变黄,试写出该反应的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】(1)除去FeCl2溶液中混有的少量FeCl3杂质的试剂是___________ ,离子方程式为___________
(2)除去镁粉末中混入的铝粉的试剂是___________ ,化学方程式为___________ 。
(2)除去镁粉末中混入的铝粉的试剂是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】选择最佳试剂 有效除去下列括号中的杂质,写出反应的离子方程式。
(1)NaHCO3溶液(Na2CO3)____________ ;
(2)FeCl3溶液(FeCl2),______________ ;
(1)NaHCO3溶液(Na2CO3)
(2)FeCl3溶液(FeCl2),
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】高锰酸钾受热容易分解,在不同温度下,发生如下反应:


请回答:
(1)取 12.64gKMnO₄固体, 加热至 700℃, 一段时间后剩余固体的质量为 11.04g, 剩余固体中的 MnO₂质量为_______ g。
(2)取(1) 剩余固体与足量的浓盐酸在加热条件下充分反应生成Cl₂,产物中锰元素以Mn²⁺存在, 则 Cl₂的物质的量为_______ mol。


请回答:
(1)取 12.64gKMnO₄固体, 加热至 700℃, 一段时间后剩余固体的质量为 11.04g, 剩余固体中的 MnO₂质量为
(2)取(1) 剩余固体与足量的浓盐酸在加热条件下充分反应生成Cl₂,产物中锰元素以Mn²⁺存在, 则 Cl₂的物质的量为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】阅读下列科普短文,利用所学化学知识回答下列问题.
地表的天然水中含有很多杂质,为满足人们生产生活的需要,必须对其进行处理.利用混凝剂 可除去天然水中的悬浮物.
可除去天然水中的悬浮物. 在水中发生电离,产生的
在水中发生电离,产生的 与水反应生成
与水反应生成 胶体,可以吸附悬浮物与色素.为获得饮用水,还需对天然水消毒杀菌.过去广泛采用氯水作水体的消毒剂,近年来
胶体,可以吸附悬浮物与色素.为获得饮用水,还需对天然水消毒杀菌.过去广泛采用氯水作水体的消毒剂,近年来 和
和 备受关注.
备受关注. 溶于水能释放大量的原子氧,从而有效杀灭水中的病菌,同时生成具有良好吸附性的
溶于水能释放大量的原子氧,从而有效杀灭水中的病菌,同时生成具有良好吸附性的 胶体,所以
胶体,所以 具有广阔的应用前景.
具有广阔的应用前景.
(1)混凝剂 在水中电离产生的阴离子是
在水中电离产生的阴离子是____________ .
(2)氯水中含有____________ 种分子,其中决定氯水颜色的分子是(填分子式)____________ .
(3) 与
与 的关系是互为
的关系是互为____________ ,等质量的 和
和 的分子数之比为
的分子数之比为____________ .
(4) 胶体可以与
胶体可以与 溶液反应,化学方程式为
溶液反应,化学方程式为____________ 。
(5) 溶于水反应的离子方程式:
溶于水反应的离子方程式: ,当生成标准状况下
,当生成标准状况下 的体积为
的体积为 时,反应中共转移电子
时,反应中共转移电子____________  .
.
地表的天然水中含有很多杂质,为满足人们生产生活的需要,必须对其进行处理.利用混凝剂
 可除去天然水中的悬浮物.
可除去天然水中的悬浮物. 在水中发生电离,产生的
在水中发生电离,产生的 与水反应生成
与水反应生成 胶体,可以吸附悬浮物与色素.为获得饮用水,还需对天然水消毒杀菌.过去广泛采用氯水作水体的消毒剂,近年来
胶体,可以吸附悬浮物与色素.为获得饮用水,还需对天然水消毒杀菌.过去广泛采用氯水作水体的消毒剂,近年来 和
和 备受关注.
备受关注. 溶于水能释放大量的原子氧,从而有效杀灭水中的病菌,同时生成具有良好吸附性的
溶于水能释放大量的原子氧,从而有效杀灭水中的病菌,同时生成具有良好吸附性的 胶体,所以
胶体,所以 具有广阔的应用前景.
具有广阔的应用前景.(1)混凝剂
 在水中电离产生的阴离子是
在水中电离产生的阴离子是(2)氯水中含有
(3)
 与
与 的关系是互为
的关系是互为 和
和 的分子数之比为
的分子数之比为(4)
 胶体可以与
胶体可以与 溶液反应,化学方程式为
溶液反应,化学方程式为(5)
 溶于水反应的离子方程式:
溶于水反应的离子方程式: ,当生成标准状况下
,当生成标准状况下 的体积为
的体积为 时,反应中共转移电子
时,反应中共转移电子 .
.
您最近一年使用:0次

 2Fe+Al2O3,
2Fe+Al2O3,

