我国的冶金工业十分发达,钢铁年产量已达到十亿吨,占世界产量的一半以上,同时有色金属产量也超过了七千万吨。
(1)铜是人类最早使用的金属,其电阻率小、延展性好,常用于制作电路板,在使用氯化铁溶液蚀刻铜制电路板时,发生反应的化学方程式为___________ 。
(2)铝与 溶液反应的化学方程式为
溶液反应的化学方程式为___________ ;铝的化学性质较活泼,但在空气中不会完全锈蚀,其原因是___________ 。
(3)电镀是一种常见的金属处理工艺,然而在生产过程中,电镀厂会产生大量的高毒性废水,将其直接排放会造成严重的污染。因此,废水的处理是电镀行业面临的主要问题之一。
①在电镀之前,镀件需要用酸性 溶液浸泡清洗。清洗废液的处理需要去除其中的悬浮颗粒物,并加入足量的
溶液浸泡清洗。清洗废液的处理需要去除其中的悬浮颗粒物,并加入足量的 固体,将
固体,将 还原为
还原为 ,则还原过程中发生反应的离子方程式为
,则还原过程中发生反应的离子方程式为___________ ,当有 被完全处理时,理论上需要加入
被完全处理时,理论上需要加入 的质量为
的质量为___________ 。
②为了减缓镀件表面的金属沉积速率,得到均匀、光滑的镀层,电解液中除重金属盐外,还需要加入剧毒的 。已知
。已知 中各原子均满足8电子稳定结构,则
中各原子均满足8电子稳定结构,则 的电子式为
的电子式为___________ 。在碱性的废电解液中通入氯气可以将 氧化,并生成两种无毒的氧化产物(其中一种为大气中占比最多的成分),则反应的离子方程式为
氧化,并生成两种无毒的氧化产物(其中一种为大气中占比最多的成分),则反应的离子方程式为___________ 。
(1)铜是人类最早使用的金属,其电阻率小、延展性好,常用于制作电路板,在使用氯化铁溶液蚀刻铜制电路板时,发生反应的化学方程式为
(2)铝与
 溶液反应的化学方程式为
溶液反应的化学方程式为(3)电镀是一种常见的金属处理工艺,然而在生产过程中,电镀厂会产生大量的高毒性废水,将其直接排放会造成严重的污染。因此,废水的处理是电镀行业面临的主要问题之一。
①在电镀之前,镀件需要用酸性
 溶液浸泡清洗。清洗废液的处理需要去除其中的悬浮颗粒物,并加入足量的
溶液浸泡清洗。清洗废液的处理需要去除其中的悬浮颗粒物,并加入足量的 固体,将
固体,将 还原为
还原为 ,则还原过程中发生反应的离子方程式为
,则还原过程中发生反应的离子方程式为 被完全处理时,理论上需要加入
被完全处理时,理论上需要加入 的质量为
的质量为②为了减缓镀件表面的金属沉积速率,得到均匀、光滑的镀层,电解液中除重金属盐外,还需要加入剧毒的
 。已知
。已知 中各原子均满足8电子稳定结构,则
中各原子均满足8电子稳定结构,则 的电子式为
的电子式为 氧化,并生成两种无毒的氧化产物(其中一种为大气中占比最多的成分),则反应的离子方程式为
氧化,并生成两种无毒的氧化产物(其中一种为大气中占比最多的成分),则反应的离子方程式为
更新时间:2024-05-08 21:35:09
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】阅读分析下列两个材料:
材料一
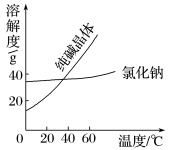
材料二
(1)用微粒符号表示下列微粒。
根据上述材料,将下列混合物分离的方法填在横线上(选填编号):
A.蒸馏法 B.萃取法 C.冷却结晶法 D.分液法
(2)从含氯化钠杂质的纯碱中分离出纯碱,最好选用________ ;
(3)将乙二醇和丙三醇分离的最佳方法是________ 。
材料三:
溴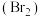 与碘
与碘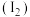 溶解性相似,其稀的水溶液呈黄色。
溶解性相似,其稀的水溶液呈黄色。
(4)从溴水中提取溴的方法是________ ,将溴水移入________ (填仪器名称)中,加入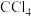 充分振荡并静置,
充分振荡并静置,________ (选填“上层”或“下层”)液体的颜色较深。
(5)若观察发现提取溴以后的水还有颜色,解决该问题的方法是________ 。
材料一

材料二
| 物质 | 熔点/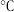 | 沸点/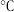 | 密度/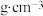 | 溶解性 |
乙二醇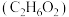 | 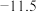 | 198 | 1.11 | 易溶于水和乙醇 |
丙三醇 | 17.9 | 290 | 1.26 | 与水、乙醇以任意比互溶 |
| 结构示意图 | 电子式 | |
| 钠离子 | ||
| 氯原子 |
根据上述材料,将下列混合物分离的方法填在横线上(选填编号):
A.蒸馏法 B.萃取法 C.冷却结晶法 D.分液法
(2)从含氯化钠杂质的纯碱中分离出纯碱,最好选用
(3)将乙二醇和丙三醇分离的最佳方法是
材料三:
溴
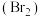 与碘
与碘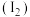 溶解性相似,其稀的水溶液呈黄色。
溶解性相似,其稀的水溶液呈黄色。(4)从溴水中提取溴的方法是
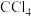 充分振荡并静置,
充分振荡并静置,(5)若观察发现提取溴以后的水还有颜色,解决该问题的方法是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】I.回答下列问题:
(1)Sn为IVA族元素,单质Sn与干燥Cl2反应生成SnCl4。常温常压下SnCl4为无色液体,SnCl4空间构型为____ 。
(2)NH3、PH3、AsH3的沸点由高到低的顺序为____ (填化学式,下同),还原性由强到弱的顺序为____ ,键角由大到小的顺序为____ 。
II.回答下列问题:
(3)气态氢化物热稳定性HF大于HCl的主要原因是____ 。
(4)CaCN2是离子化合物,各原子均满足8电子稳定结构,CaCN2的电子式是____ 。
(5)常温下,在水中的溶解度乙醇大于氯乙烷,原因是____ 。
III.回答下列问题:
(6)比较给出H+能力的相对强弱:H2O____ C2H5OH(填“>”“<”或“=”);用一个化学方程式说明OH-和C2H5O-结合H+能力的相对强弱:____ 。
(7)CaC2是离子化合物,各原子均满足8电子稳定结构.写出CaC2的电子式:____ 。
(8)在常压下,甲醇的沸点(65℃)比甲醛的沸点(-19℃)高,主要原因是____ 。
IV.研究发现,在CO2低压合成甲醇反应(CO2+3H2=CH3OH+H2O)中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
(9)CO2和CH3OH分子中C原子的杂化形式分别为____ 和____ 。
(10)在CO2低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为____ ,原因是____ 。
(11)硝酸锰是制备上述反应催化剂的原料,Mn(NO3)2中的化学键除了σ键外,还存在____ 。
(1)Sn为IVA族元素,单质Sn与干燥Cl2反应生成SnCl4。常温常压下SnCl4为无色液体,SnCl4空间构型为
(2)NH3、PH3、AsH3的沸点由高到低的顺序为
II.回答下列问题:
(3)气态氢化物热稳定性HF大于HCl的主要原因是
(4)CaCN2是离子化合物,各原子均满足8电子稳定结构,CaCN2的电子式是
(5)常温下,在水中的溶解度乙醇大于氯乙烷,原因是
III.回答下列问题:
(6)比较给出H+能力的相对强弱:H2O
(7)CaC2是离子化合物,各原子均满足8电子稳定结构.写出CaC2的电子式:
(8)在常压下,甲醇的沸点(65℃)比甲醛的沸点(-19℃)高,主要原因是
IV.研究发现,在CO2低压合成甲醇反应(CO2+3H2=CH3OH+H2O)中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
(9)CO2和CH3OH分子中C原子的杂化形式分别为
(10)在CO2低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为
(11)硝酸锰是制备上述反应催化剂的原料,Mn(NO3)2中的化学键除了σ键外,还存在
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】我国“四大发明”在人类发展史上起到了非常重要的作用。其中黑火药的爆炸反应:2KNO3+S+3C K2S+N2↑+3CO2↑。
K2S+N2↑+3CO2↑。
(1)该反应中被还原的元素是___________ (填元素符号);氧化性:KNO3___________ CO2(填“>”或“<”)。
(2)硝酸钾是一种氮钾复合肥。从其阳离子看,则属于钾盐,从其阴离子看,则属于硝酸盐,该分类方法称为___________ 。
(3)上述反应物和生成物中属于非电解质的有___________ 。
(4)CO2属于酸性氧化物,可与NaOH、_______ (填与NaOH不同类别的一种具体物质的化学式)等反应。
(5)N2的电子为___________ ;请用电子式表示K2S的形成过程___________ 。
 K2S+N2↑+3CO2↑。
K2S+N2↑+3CO2↑。(1)该反应中被还原的元素是
(2)硝酸钾是一种氮钾复合肥。从其阳离子看,则属于钾盐,从其阴离子看,则属于硝酸盐,该分类方法称为
(3)上述反应物和生成物中属于非电解质的有
(4)CO2属于酸性氧化物,可与NaOH、
(5)N2的电子为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】写出下列化学反应的离子方程式
①NaOH溶液和HCl溶液____________
②Na2CO3和足量HCl____________
③H2SO4溶液和Ba(OH)2溶液____________
①NaOH溶液和HCl溶液
②Na2CO3和足量HCl
③H2SO4溶液和Ba(OH)2溶液
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】(1)写出NaHCO3在水溶液中的电离方程式:____
(2)写出Ag++Cl-=AgCl↓对应的化学方程式:____
(3)写出CuSO4+2NaOH=Cu(OH)2↓+Na2SO4对应的离子方程式:____
(4)写出SO2十2OH-= +H2O对应的化学方程式:
+H2O对应的化学方程式:____
(2)写出Ag++Cl-=AgCl↓对应的化学方程式:
(3)写出CuSO4+2NaOH=Cu(OH)2↓+Na2SO4对应的离子方程式:
(4)写出SO2十2OH-=
 +H2O对应的化学方程式:
+H2O对应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
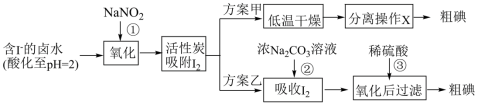
【推荐1】从海水中可以提取很多有用的物质,例如从海水制盐所得到的卤水中可以提取碘。活性炭吸附法是工业提碘的方法之一,其流程如下:
Ⅱ. ;
;
Ⅲ.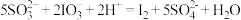 ;
;
方案甲中,根据I2的特性,分离操作X的名称是________ 。
Ⅱ.
 ;
;Ⅲ.
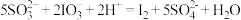 ;
;方案甲中,根据I2的特性,分离操作X的名称是
您最近一年使用:0次
【推荐2】用硫酸酸化的CrO3遇到酒精后,其颜色会从红色变为蓝绿色,人们利用这一反应可以判断司机是否酒后驾车,反应的方程式为:CrO3+C2H5OH+H2SO4→Cr2(SO4)3+CH3CHO+H2O
(1)配平上述反应方程式_____ 。
(2)该反应中氧化剂是_____ ,被氧化的元素是_____ 。
(1)配平上述反应方程式
(2)该反应中氧化剂是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】某铝合金中除了镁铝以外,还有少量的铜、硅和锰(它们都不与盐酸反应),为了测定硬铝中镁的含量,取硬铝6.0g投入足量盐酸中,充分反应过滤后,往滤液中加过量的氢氧化钠溶液,过滤,所得沉淀经干燥、加热后得到0.40g固体,请计算该硬铝中镁的质量分数。 ______ (提示:氢氧化镁加热会分解成氧化镁和水)
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】铝是生活中非常常见的一种金属,运用所学知识回答:
(1)金属铝是活泼的金属,可在生活中应用很广泛,原因是_______ 。
(2)铝盐或铁盐能用于净水,是因为铝盐或铁盐在水溶液中形成了_______ 。
(3)在一个瘪了的铝制易拉罐加入适量的NaOH溶液,并密封,易拉罐会慢慢复原,原因是(用化学方程式表示)_______ 。
(4)铝粉与氧化铁粉末在高温下得到铁的反应叫做“铝热反应”,发生反应的化学方程式为_______ 。
(1)金属铝是活泼的金属,可在生活中应用很广泛,原因是
(2)铝盐或铁盐能用于净水,是因为铝盐或铁盐在水溶液中形成了
(3)在一个瘪了的铝制易拉罐加入适量的NaOH溶液,并密封,易拉罐会慢慢复原,原因是(用化学方程式表示)
(4)铝粉与氧化铁粉末在高温下得到铁的反应叫做“铝热反应”,发生反应的化学方程式为
您最近一年使用:0次

 )=
)=

