(1)根据反应8NH3+3Cl2 6NH4Cl+N2,回答下列问题:
6NH4Cl+N2,回答下列问题:
①该反应中氧化剂是______________ ,氧化产物是___________________ 。
②该反应中被氧化的物质与被还原的物质物质的量之比为________________ 。
(2)某一反应体系中存在下列6种物质:NO、FeSO4、Fe(NO3)3、HNO3、Fe2(SO4)3和H2O。已知存在下列转化关系:HNO3→NO,请完成下列各题:
①该反应的氧化剂是__________ ,还原剂是___________ 。
②该反应中1 mol氧化剂____________ (填“得到”或“失去”)____________ mol电子。
③当有0.1 mol HNO3被还原,此时生成标准状况下NO的体积是__________ L。
④请把各物质填在下面空格处,需配平:______ +□______ □______+□______+□______+□
□______+□______+□______+□
 6NH4Cl+N2,回答下列问题:
6NH4Cl+N2,回答下列问题:①该反应中氧化剂是
②该反应中被氧化的物质与被还原的物质物质的量之比为
(2)某一反应体系中存在下列6种物质:NO、FeSO4、Fe(NO3)3、HNO3、Fe2(SO4)3和H2O。已知存在下列转化关系:HNO3→NO,请完成下列各题:
①该反应的氧化剂是
②该反应中1 mol氧化剂
③当有0.1 mol HNO3被还原,此时生成标准状况下NO的体积是
④请把各物质填在下面空格处,需配平:
 □______+□______+□______+□
□______+□______+□______+□
2017高一·全国·课时练习 查看更多[5]
(已下线)第4单元 氧化还原反应(A卷 基础过关检测)-2021年高考化学一轮复习单元滚动双测卷2018-2019学年鲁科版高一化学必修1《氧化剂和还原剂》同步练习题2018年高一化学(人教版)必修1综合题型练习卷:氧化还原反应高中化学人教版 必修1 第二章 化学物质及其变化 3.氧化还原反应 氧化剂和还原剂(已下线)2.3.2 氧化剂和还原剂
更新时间:2018-10-07 10:44:04
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】聚合氯化铝用于城市给排水净化。氧化铝法制取无水三氯化铝的反应如下: 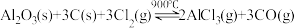
(1)标出上述反应的电子转移方向和数目_______ 。
(2)写出该反应的平衡常数表达式:
_______ 。
(3)Al原子核外有_______ 种不同能量的电子。
聚合氯化铝(PAC)是一种介于 和
和 之间的水溶性无机高分子聚合物,PAC的水解过程中会有一种聚合稳定态物质
之间的水溶性无机高分子聚合物,PAC的水解过程中会有一种聚合稳定态物质 称为
称为 ,
, 对水中胶体和颗粒物具有高度电中和桥联作用,是净水过程中的重要物质。
对水中胶体和颗粒物具有高度电中和桥联作用,是净水过程中的重要物质。
(4) Al13在水解过程中会产生[Al(OH)2]+、[Al(OH)]2+等产物,写出[Al(OH)]2+水解的离子方程式_______ 。
(5) 溶液与NaOH溶液反应,若参与反应的铝离子最终全部转化生成
溶液与NaOH溶液反应,若参与反应的铝离子最终全部转化生成 ,则理论上参与反应的
,则理论上参与反应的 与
与 的物质的量之比是
的物质的量之比是_______
(6)使用 净水时应控制pH在6.8~8.02之间,否则净水效果不佳。请结合使用
净水时应控制pH在6.8~8.02之间,否则净水效果不佳。请结合使用 水解净化水时铝元素存在的形态,分析在强酸性和强碱性环境时净水效果差的原因。
水解净化水时铝元素存在的形态,分析在强酸性和强碱性环境时净水效果差的原因。_______
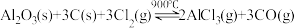
(1)标出上述反应的电子转移方向和数目
(2)写出该反应的平衡常数表达式:

(3)Al原子核外有
聚合氯化铝(PAC)是一种介于
 和
和 之间的水溶性无机高分子聚合物,PAC的水解过程中会有一种聚合稳定态物质
之间的水溶性无机高分子聚合物,PAC的水解过程中会有一种聚合稳定态物质 称为
称为 ,
, 对水中胶体和颗粒物具有高度电中和桥联作用,是净水过程中的重要物质。
对水中胶体和颗粒物具有高度电中和桥联作用,是净水过程中的重要物质。(4) Al13在水解过程中会产生[Al(OH)2]+、[Al(OH)]2+等产物,写出[Al(OH)]2+水解的离子方程式
(5)
 溶液与NaOH溶液反应,若参与反应的铝离子最终全部转化生成
溶液与NaOH溶液反应,若参与反应的铝离子最终全部转化生成 ,则理论上参与反应的
,则理论上参与反应的 与
与 的物质的量之比是
的物质的量之比是(6)使用
 净水时应控制pH在6.8~8.02之间,否则净水效果不佳。请结合使用
净水时应控制pH在6.8~8.02之间,否则净水效果不佳。请结合使用 水解净化水时铝元素存在的形态,分析在强酸性和强碱性环境时净水效果差的原因。
水解净化水时铝元素存在的形态,分析在强酸性和强碱性环境时净水效果差的原因。
您最近半年使用:0次
【推荐2】NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒.已知NaNO2能发生如下反应:2NaNO2+4HI═2NO↑+I2+2NaI+2H2O。
(1)上述反应中氧化剂是___ ,氧化产物是___ (填写化学式)。
(2)根据上述反应,鉴别NaNO2、NaCl.可选用的物质有:①水、②碘化钾淀粉试纸、③淀粉、④白酒、⑤食醋,你认为必须选用的物质有______ (填序号)。
(3)某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是______ (填编号)。
A.NaCl B.NH4Cl C.HNO3 D.浓H2SO4
(4)化学方程式:10Al+6NaNO3+4NaOH═10NaAlO2+3N2↑+2H2O.若反应过程中转移5mole-,则生成标准状况下N2的体积为______ L。
(1)上述反应中氧化剂是
(2)根据上述反应,鉴别NaNO2、NaCl.可选用的物质有:①水、②碘化钾淀粉试纸、③淀粉、④白酒、⑤食醋,你认为必须选用的物质有
(3)某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是
A.NaCl B.NH4Cl C.HNO3 D.浓H2SO4
(4)化学方程式:10Al+6NaNO3+4NaOH═10NaAlO2+3N2↑+2H2O.若反应过程中转移5mole-,则生成标准状况下N2的体积为
您最近半年使用:0次
【推荐3】氧化还原反应是一类重要的反应,请按要求完成下列题目。
(1)对反应NH3+O2——NO+H2O(未配平)作分析,该反应中,________ 是还原剂,________ 是氧化剂,________ 是氧化产物,被还原的物质是________ 。
(2)在一定条件下,反应2NH3+3CuO 3Cu+N2+3H2O能顺利进行,对此反应的分析合理的是
3Cu+N2+3H2O能顺利进行,对此反应的分析合理的是_______ (填序号)。
A.该反应是置换反应
B.反应中NH3被氧化为N2
C.在反应中体现了金属铜的还原性
D.在反应中每生成1 mol H2O转移1 mol电子
(3)在反应H2SO3+2H2S==3H2O+3S↓中被氧化的元素与被还原的元素的质量比______ 。
(1)对反应NH3+O2——NO+H2O(未配平)作分析,该反应中,
(2)在一定条件下,反应2NH3+3CuO
 3Cu+N2+3H2O能顺利进行,对此反应的分析合理的是
3Cu+N2+3H2O能顺利进行,对此反应的分析合理的是A.该反应是置换反应
B.反应中NH3被氧化为N2
C.在反应中体现了金属铜的还原性
D.在反应中每生成1 mol H2O转移1 mol电子
(3)在反应H2SO3+2H2S==3H2O+3S↓中被氧化的元素与被还原的元素的质量比
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如图所示。请回答下列问题:

(1)NaClO2中Cl元素的化合价为_______ 。
(2)“电解”所用食盐水由粗盐水精制而成。精制时,为除去Mg2+和Ca2+,要加入的试剂分别为_______ 、_______ 。
(3)“尾气吸收”发生2NaOH+H2O2+2ClO2═2NaClO2+O2+2H2O反应,氧化剂与还原剂的质量之比为_______ 。

(1)NaClO2中Cl元素的化合价为
(2)“电解”所用食盐水由粗盐水精制而成。精制时,为除去Mg2+和Ca2+,要加入的试剂分别为
(3)“尾气吸收”发生2NaOH+H2O2+2ClO2═2NaClO2+O2+2H2O反应,氧化剂与还原剂的质量之比为
您最近半年使用:0次
【推荐2】根据所学知识回答下列问题:
(1)①写出Fe2(SO4)3在水溶液中的电离方程式:______ 。
②FeCl3与氢碘酸反应时可生成棕色物质,该反应的离子方程式为:_____ 。
③写出Al与氢氧化钠溶液反应的离子方程式:_____ 。
(2)高铁酸钠(Na2FeO4)是一种新型净水剂。制取高铁酸钠所发生的反应如下:
______Fe(NO3)3+______NaOH+______Cl2=______Na2FeO4+______NaNO3+______NaCl+______H2O
①配平并用“双线桥”表示电子转移的方向和数目______ 。
②该反应中Na2FeO4是______ (填“氧化剂”、“还原剂”、“氧化产物”或“还原产物”)。
③若转移的电子数目为0.3NA(NA为阿伏加德罗常数),则消耗的Cl2在标准状况下的体积为______ L。
④黄色气体ClO2可用于污水杀菌和饮用水净化,ClO2可将废水中的Mn2+转化为MnO2而除去,本身还原为Cl-,该反应过程中氧化剂与还原剂的物质的量之比为______ 。
(3)已知M2O 可与R2-作用,R2-被氧化为R单质,M2O
可与R2-作用,R2-被氧化为R单质,M2O 的还原产物中M为+3价;又知c(M2O
的还原产物中M为+3价;又知c(M2O )=0.3mol•L-1的溶液100mL可与c(R2-)=0.6mol•L-1的溶液150mL恰好完全反应,则n值为
)=0.3mol•L-1的溶液100mL可与c(R2-)=0.6mol•L-1的溶液150mL恰好完全反应,则n值为______ 。
(1)①写出Fe2(SO4)3在水溶液中的电离方程式:
②FeCl3与氢碘酸反应时可生成棕色物质,该反应的离子方程式为:
③写出Al与氢氧化钠溶液反应的离子方程式:
(2)高铁酸钠(Na2FeO4)是一种新型净水剂。制取高铁酸钠所发生的反应如下:
______Fe(NO3)3+______NaOH+______Cl2=______Na2FeO4+______NaNO3+______NaCl+______H2O
①配平并用“双线桥”表示电子转移的方向和数目
②该反应中Na2FeO4是
③若转移的电子数目为0.3NA(NA为阿伏加德罗常数),则消耗的Cl2在标准状况下的体积为
④黄色气体ClO2可用于污水杀菌和饮用水净化,ClO2可将废水中的Mn2+转化为MnO2而除去,本身还原为Cl-,该反应过程中氧化剂与还原剂的物质的量之比为
(3)已知M2O
 可与R2-作用,R2-被氧化为R单质,M2O
可与R2-作用,R2-被氧化为R单质,M2O 的还原产物中M为+3价;又知c(M2O
的还原产物中M为+3价;又知c(M2O )=0.3mol•L-1的溶液100mL可与c(R2-)=0.6mol•L-1的溶液150mL恰好完全反应,则n值为
)=0.3mol•L-1的溶液100mL可与c(R2-)=0.6mol•L-1的溶液150mL恰好完全反应,则n值为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】《南村辍耕录》中记载:“杭人削松木为小片,其薄如纸,熔硫磺涂木片顶分许,名曰发烛。”《资治通鉴》中记载:“陈宣帝太建九年,齐后妃贫苦,至以卖烛为业。”文中的“发烛”就是原始的火柴。已知K2Cr2O7用于工业中制造火柴头。

K2Cr2O7+HCl(浓)→KCl+CrCl3+Cl2↑+H2O(未配平)
(1)(填元素名称 )___ 元素被氧化,(填化学式 ,下同)___ 是氧化剂,___ 发生氧化反应。
(2)参加反应的HCl,表现了___ 和___ 。(填“还原性”“氧化性”或“酸性”)
(3)该反应中每生成6个Cl2转移电子个数为___ 个。
(4)配平上述反应,并用单线桥法表示出该反应中电子转移的方向和数目___ 。

K2Cr2O7+HCl(浓)→KCl+CrCl3+Cl2↑+H2O(未配平)
(1)(填
(2)参加反应的HCl,表现了
(3)该反应中每生成6个Cl2转移电子个数为
(4)配平上述反应,并用单线桥法表示出该反应中电子转移的方向和数目
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】NaClO2的漂白能力是漂白粉的4~5倍,NaClO2广泛用于造纸工业、污水处理等。工业上生产NaClO2的工艺流程如下:
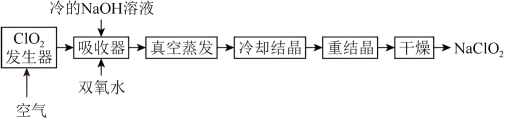
吸收器中生成NaClO2的离子反应方程式为___________ ,其中反应温度不能高于5℃的可能原因:___________ 。

吸收器中生成NaClO2的离子反应方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氧化还原反应在日常生活和工业生产中有重要应用.
Ⅰ.2022年6月,“神舟十四号”载人飞船顺利进入预定轨道,发射飞船的火箭用偏二甲肼 做燃料,四氧化二氮
做燃料,四氧化二氮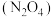 作推进剂,回答下列问题:
作推进剂,回答下列问题:
(1) 中含有的N原子数为
中含有的N原子数为__________ ,与__________  中含有的N原子数相同.
中含有的N原子数相同.
Ⅱ.阅读下面一段材料并回答问题.
【化学式】
【性状】暗紫色具有金属光泽的粉末,无臭无味
【产品特点】干燥品在室温卡稳定,在强碱溶液中稳定,随着 减小,稳定性下降,与水反应放出氧气.
减小,稳定性下降,与水反应放出氧气. 通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质.
通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质. 与水反应还能产生具有强吸附性的
与水反应还能产生具有强吸附性的 胶体,可除去水中细微的悬浮物,有净水作用
胶体,可除去水中细微的悬浮物,有净水作用
【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理
【用量】消毒净化 水投放
水投放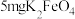 即可达到卫生标准
即可达到卫生标准
……
(2) 中铁元素的化合价为
中铁元素的化合价为__________ .
(3)下列关于 的说法中,不正确的是
的说法中,不正确的是__________ .
a.是强氧化性的盐 b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(4)工业制备 需要在碱性环境下进行,现提供反应体系中7种物质,
需要在碱性环境下进行,现提供反应体系中7种物质,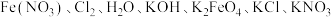 请写出制备
请写出制备 的化学反应方程式
的化学反应方程式__________ .
(5)将 与水反应的化学方程式补充完整并配平:
与水反应的化学方程式补充完整并配平:__________
__________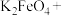 __________
__________ __________
__________ (胶体)+__________+__________
(胶体)+__________+__________
该反应消耗 时,转移的电子数为
时,转移的电子数为__________
(6)消毒净化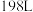 水,按照卫生标准投入
水,按照卫生标准投入 ,则
,则 与水充分反应后产生的
与水充分反应后产生的 质量为
质量为__________ g.
Ⅰ.2022年6月,“神舟十四号”载人飞船顺利进入预定轨道,发射飞船的火箭用偏二甲肼
 做燃料,四氧化二氮
做燃料,四氧化二氮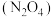 作推进剂,回答下列问题:
作推进剂,回答下列问题:(1)
 中含有的N原子数为
中含有的N原子数为 中含有的N原子数相同.
中含有的N原子数相同.Ⅱ.阅读下面一段材料并回答问题.
高铁酸钾使用说明书
【化学式】

【性状】暗紫色具有金属光泽的粉末,无臭无味
【产品特点】干燥品在室温卡稳定,在强碱溶液中稳定,随着
 减小,稳定性下降,与水反应放出氧气.
减小,稳定性下降,与水反应放出氧气. 通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质.
通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质. 与水反应还能产生具有强吸附性的
与水反应还能产生具有强吸附性的 胶体,可除去水中细微的悬浮物,有净水作用
胶体,可除去水中细微的悬浮物,有净水作用【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理
【用量】消毒净化
 水投放
水投放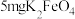 即可达到卫生标准
即可达到卫生标准……
(2)
 中铁元素的化合价为
中铁元素的化合价为(3)下列关于
 的说法中,不正确的是
的说法中,不正确的是a.是强氧化性的盐 b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(4)工业制备
 需要在碱性环境下进行,现提供反应体系中7种物质,
需要在碱性环境下进行,现提供反应体系中7种物质,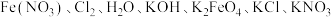 请写出制备
请写出制备 的化学反应方程式
的化学反应方程式(5)将
 与水反应的化学方程式补充完整并配平:
与水反应的化学方程式补充完整并配平:__________
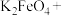 __________
__________ __________
__________ (胶体)+__________+__________
(胶体)+__________+__________
该反应消耗
 时,转移的电子数为
时,转移的电子数为(6)消毒净化
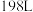 水,按照卫生标准投入
水,按照卫生标准投入 ,则
,则 与水充分反应后产生的
与水充分反应后产生的 质量为
质量为
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】按要求完成下列化学方程式:
(1)铁丝在氧气中燃烧的产物能溶于稀盐酸,试写出反应的化学方程式___________ 。
(2)“神舟五号”火箭的动力来源是联氨 和四氧化二氮的反应,反应生成无公害物质,试写出反应的化学方程式
和四氧化二氮的反应,反应生成无公害物质,试写出反应的化学方程式___________ 。
(3)已知 和
和 都是易分解的二元弱酸,且
都是易分解的二元弱酸,且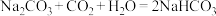 。试写出将过量
。试写出将过量 通入到少量NaOH溶液中反应的化学方程式
通入到少量NaOH溶液中反应的化学方程式___________ 。
(4)已知硫和氧的性质相似,对应化合物的性质也相似,且 (硫代碳酸钠),试写出
(硫代碳酸钠),试写出 和
和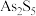 反应的化学方程式
反应的化学方程式___________ 。
(1)铁丝在氧气中燃烧的产物能溶于稀盐酸,试写出反应的化学方程式
(2)“神舟五号”火箭的动力来源是联氨
 和四氧化二氮的反应,反应生成无公害物质,试写出反应的化学方程式
和四氧化二氮的反应,反应生成无公害物质,试写出反应的化学方程式(3)已知
 和
和 都是易分解的二元弱酸,且
都是易分解的二元弱酸,且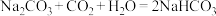 。试写出将过量
。试写出将过量 通入到少量NaOH溶液中反应的化学方程式
通入到少量NaOH溶液中反应的化学方程式(4)已知硫和氧的性质相似,对应化合物的性质也相似,且
 (硫代碳酸钠),试写出
(硫代碳酸钠),试写出 和
和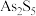 反应的化学方程式
反应的化学方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)向Na2CO3溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有NaHCO3生成,该反应的化学方程式是___ 。
(2)Na2CO3浓溶液中通入氯气时,可产生气体CO2和化合物NaClO3。反应的化学方程式为___ 。
(1)向Na2CO3溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有NaHCO3生成,该反应的化学方程式是
(2)Na2CO3浓溶液中通入氯气时,可产生气体CO2和化合物NaClO3。反应的化学方程式为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】请根据硫元素的价类二维图,回答下列问题:___________ (填化学式)。
(2)宋代著名法医学家宋慈的 洗冤集录
洗冤集录 中有关于“银针验毒”的记载,银针主要用于检验是否有含硫元素的有毒物质。其反应原理之一为:Ag + X + O2 →Ag2S + H2O(反应未配平),已知:Ag2S为一种不溶于水的灰黑色固体。以下有关说法
中有关于“银针验毒”的记载,银针主要用于检验是否有含硫元素的有毒物质。其反应原理之一为:Ag + X + O2 →Ag2S + H2O(反应未配平),已知:Ag2S为一种不溶于水的灰黑色固体。以下有关说法错误 的是___________(填字母)。
(3)Y转化为Z可以选择下列试剂___________ 。
A.酸性KMnO4溶液 B.FeCl2溶液 C.NaOH溶液 D.X的水溶液
写出你所选试剂将Y转化为Z的离子方程式___________ 。
(4)若N是CuSO4,某同学设计了甲和乙两种方法制备:
甲: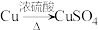 乙:
乙:
①写出甲方法反应的化学方程式:___________ 。
②甲和乙方法更合理的是___________ (填“甲”或“乙”),理由是___________ (答两点)。
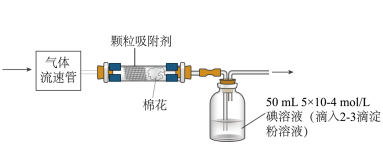
(5)已知空气中SO2的最大允许排放浓度不得超过0.02 mg•L-1,可通过下列装置定量分析空气中SO2的含量。___________ mg•L-1(结果精确到0.001)。

(2)宋代著名法医学家宋慈的
 洗冤集录
洗冤集录 中有关于“银针验毒”的记载,银针主要用于检验是否有含硫元素的有毒物质。其反应原理之一为:Ag + X + O2 →Ag2S + H2O(反应未配平),已知:Ag2S为一种不溶于水的灰黑色固体。以下有关说法
中有关于“银针验毒”的记载,银针主要用于检验是否有含硫元素的有毒物质。其反应原理之一为:Ag + X + O2 →Ag2S + H2O(反应未配平),已知:Ag2S为一种不溶于水的灰黑色固体。以下有关说法| A.当银针变黑时,说明所检验的物质中可能有毒 |
| B.银针验毒时,Ag被氧化 |
| C.X在上述验毒反应中作还原剂 |
| D.上述验毒反应中氧化剂和还原剂的物质的量之比为4∶1 |
(3)Y转化为Z可以选择下列试剂
A.酸性KMnO4溶液 B.FeCl2溶液 C.NaOH溶液 D.X的水溶液
写出你所选试剂将Y转化为Z的离子方程式
(4)若N是CuSO4,某同学设计了甲和乙两种方法制备:
甲:
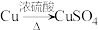 乙:
乙:
①写出甲方法反应的化学方程式:
②甲和乙方法更合理的是
(5)已知空气中SO2的最大允许排放浓度不得超过0.02 mg•L-1,可通过下列装置定量分析空气中SO2的含量。
您最近半年使用:0次
【推荐3】已知:2 KMnO4 + 16HCl(浓) = 2MnCl2 +2 KCl + 5Cl2↑+ 8H2O
(1)反应中元素化合价降低的物质是______ (填化学式),含该元素的物质发生______ 反应(填“氧化”或“还原”);
(2)该反应中,还原剂是______ ,还原产物是______ (填化学式);
(3)用“双线桥法”标明反应中电子转移的方向和数目;_____ 2 KMnO4 + 16HCl(浓)=2MnCl2 +2 KCl + 5Cl2↑+ 8H2O
(4)该反应中浓盐酸体现______ 性 、______ 性。
(1)反应中元素化合价降低的物质是
(2)该反应中,还原剂是
(3)用“双线桥法”标明反应中电子转移的方向和数目;
(4)该反应中浓盐酸体现
您最近半年使用:0次



