山东省2007年高中学生化学竞赛夏令营试题
山东
高二
竞赛
2021-08-16
280次
整体难度:
适中
考查范围:
物质结构与性质、竞赛、化学反应原理、有机化学基础
山东省2007年高中学生化学竞赛夏令营试题
山东
高二
竞赛
2021-08-16
280次
整体难度:
适中
考查范围:
物质结构与性质、竞赛、化学反应原理、有机化学基础
一、解答题 添加题型下试题
解答题-结构与性质
|
适中(0.65)
1. 1937年,意大利化学家西格雷等用氘核去轰击某一元素,两种原子核融合制得了第一个人造元素锝Tc。
(1)请指出,西格雷等用氘核去轰击的是_______ 元素。
(2)金属Tc属于六方最密堆积,Tc原子的金属半径为0.136nm,求金属Tc的密度_______ ;
(3)下图是立方和六方最密堆积中原子的配位多面体,请指出哪一种对应晶体中Tc原子的配位多面体_______ ;

(4)对锰副族的最高价氧化物的水化物HMnO4、HTcO4、HReO4,酸性顺序如何_______ ?
(5)从合成锝Tc之后,科学家又何成了许多新元素。关于新元素的命名,国际化学会无机化学分会决定,从110号元素之后,不再以人名或国名来命名元素的名称,而采用拉丁文数字缩写来命名,如110号Ununilium(元素符号Uun),111号Ununnilium(元素符号Uuu),112号Ununbium(元素符号Uub),113号Ununtrium(元素符号Uut),114号Ununquadium(元素符号Uuq),115号Ununpentium(元素符号Uup),116号Ununhexium(元素符号Uuh),117号Ununseptium(元素符号Uus),118号Ununoctium(元素符号Uuo),119号Ununennium(元素符号Uue)。请你根据命名规律命名126号和128号元素_______ ,同时给出元素符号_______ ;
(6)请根据电子的填充规律,说明从多少号元素开始填充5g轨道_______ 。
(1)请指出,西格雷等用氘核去轰击的是
(2)金属Tc属于六方最密堆积,Tc原子的金属半径为0.136nm,求金属Tc的密度
(3)下图是立方和六方最密堆积中原子的配位多面体,请指出哪一种对应晶体中Tc原子的配位多面体

(4)对锰副族的最高价氧化物的水化物HMnO4、HTcO4、HReO4,酸性顺序如何
(5)从合成锝Tc之后,科学家又何成了许多新元素。关于新元素的命名,国际化学会无机化学分会决定,从110号元素之后,不再以人名或国名来命名元素的名称,而采用拉丁文数字缩写来命名,如110号Ununilium(元素符号Uun),111号Ununnilium(元素符号Uuu),112号Ununbium(元素符号Uub),113号Ununtrium(元素符号Uut),114号Ununquadium(元素符号Uuq),115号Ununpentium(元素符号Uup),116号Ununhexium(元素符号Uuh),117号Ununseptium(元素符号Uus),118号Ununoctium(元素符号Uuo),119号Ununennium(元素符号Uue)。请你根据命名规律命名126号和128号元素
(6)请根据电子的填充规律,说明从多少号元素开始填充5g轨道
您最近一年使用:0次
二、填空题 添加题型下试题
填空题
|
适中(0.65)
解题方法
2. 三乙撑四胺H2N-CH2CH2-NH-CH2CH2-NH-CH2CH2-NH2在过氧化氢溶液中,与Fe3+形成了含氮20.82%的配合物,该配合物溶于水时电离出配离子与OH-的摩尔比为1:2,画出该配离子的结构简图_______ (氢原子不用画出),并讨论该配离子的异构现象_______ 。
您最近一年使用:0次
填空题
|
较难(0.4)
3. 硼是一种重要的非金属元素,单质硼可以通过硼镁矿Mg2B2O5·H2O来制取,先将硼镁矿用浓碱NaOH处理分解,得到NaBO2,然后向NaBO2浓溶液中通入CO2调节碱度,浓缩后用结晶析出硎砂Na2B4O7·10H2O,将硎砂溶于水后,用H2SO4调节酸度析出硼酸晶体,加热硼酸脱水后用镁还原得到粗单质硼。
(1)写出由硼镁矿Mg2B2O5·H2O制取硼的化学方程式_______ ;
(2)将制得的粗硼在一定条件下反应全部生成BI3,然后使BI3热分解可以得到纯净的单质硼。0.20g粗硼制成的BI3分解得到的I2全部收集后,用2.00mol/L的Na2S2O3滴定,用去27.00mlNa2S2O3溶液,求粗硼中的硼的含量_______ ;
(3)硼酸晶体属于离子晶体、原子晶体、分子晶体、混合型晶体中的哪一种_______ ?指出硼酸中的硼采取的杂化形式_______ ,以及硼酸中的大π键类型_______ ;
(4)指出化合物H3B-NH3的熔点比其等电子体H3C-CH3等要高的多的原因,并画出示意图__ ;
(5)指出硼烷B4H10中,存在几个双电子三中心键_______ 。
(1)写出由硼镁矿Mg2B2O5·H2O制取硼的化学方程式
(2)将制得的粗硼在一定条件下反应全部生成BI3,然后使BI3热分解可以得到纯净的单质硼。0.20g粗硼制成的BI3分解得到的I2全部收集后,用2.00mol/L的Na2S2O3滴定,用去27.00mlNa2S2O3溶液,求粗硼中的硼的含量
(3)硼酸晶体属于离子晶体、原子晶体、分子晶体、混合型晶体中的哪一种
(4)指出化合物H3B-NH3的熔点比其等电子体H3C-CH3等要高的多的原因,并画出示意图
(5)指出硼烷B4H10中,存在几个双电子三中心键
您最近一年使用:0次
填空题
|
适中(0.65)
4. 二元弱酸的电离常数如下:
H2A⇌HA-+H+ K1=4.50×10-9
HA-⇌A2-+H+ K2=4.68×10-11
用0.300mol·L-1的盐酸滴定含有K2A和KHA的一份20.00mL的溶液,滴定进程用pH计跟踪,滴定曲线上的2个点的对应数据如下:
(1)加入1.00mL盐酸时首先与HCl反应的物种是_______ ,产物是_______ 。
(2)加入1.00mL盐酸生成的产物有_______ mmol。
(3)写出(1)中产物与溶剂反应的方程式___ ,并求出该反应的平衡常数____ (Kw=1×10-l4)。
(4)请通过推导详细计算出达到第二个等当点所需上述盐酸的总体积_______ 。
H2A⇌HA-+H+ K1=4.50×10-9
HA-⇌A2-+H+ K2=4.68×10-11
用0.300mol·L-1的盐酸滴定含有K2A和KHA的一份20.00mL的溶液,滴定进程用pH计跟踪,滴定曲线上的2个点的对应数据如下:
| 加入HCl的毫升数 | pH |
| 1.00 | 10.33 |
| 10.00 | 9.34 |
(1)加入1.00mL盐酸时首先与HCl反应的物种是
(2)加入1.00mL盐酸生成的产物有
(3)写出(1)中产物与溶剂反应的方程式
(4)请通过推导详细计算出达到第二个等当点所需上述盐酸的总体积
【知识点】 溶液的酸碱性与pH 弱电解质的电离平衡常数
您最近一年使用:0次
三、解答题 添加题型下试题
解答题-有机推断题
|
适中(0.65)
5. 生于110年前的德国化学家GeorgWittig,1954年发现了广泛用于有机合成的Wittig反应,为此获得1979年诺贝尔化学奖。下面就是与Wittig有关的反应:
CH3CH2OH CH3CH2Br
CH3CH2Br B
B C
C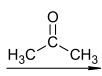 D+E
D+E
上面的反应产物中D是一种烯烃,画出试剂或中间体A、B、C、D、E的结构,并给出D的名称:A_______ 、B_______ 、C_______ 、D_______ 、_______ 、E_______ 。
CH3CH2OH
 CH3CH2Br
CH3CH2Br B
B C
C D+E
D+E上面的反应产物中D是一种烯烃,画出试剂或中间体A、B、C、D、E的结构,并给出D的名称:A
您最近一年使用:0次
解答题-有机推断题
|
适中(0.65)
6. 有机化学家曾合成出一种张力很大的笼状烷烃,红外光谱和核磁共振谱表明其分子中的碳原子和氢原子的化学环境没有区别,该烃含碳92.26%,含氢7.74%;该笼状烷烃中有多个四元环和2个五元环,不含四元环和五元环外的其他多元环。
(1)请推出该烃的分子式_______ ;
(2)请画出该分子的可能结构_______ 。
(1)请推出该烃的分子式
(2)请画出该分子的可能结构
您最近一年使用:0次
解答题-结构与性质
|
适中(0.65)
7. 钒酸根在溶液中以多种离子形式存在,如VO 、V2O
、V2O 、V3O
、V3O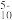 、VO
、VO 等,pH值决定着其主要以什么形式存在。
等,pH值决定着其主要以什么形式存在。
(1)你认为pH越小,_______ 离子越多,pH越大,_______ 离子越多。
(2)画出下列离子的结构图:VO
_______ 、V2O
_______ 、V3O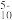
_______ 。
(3)某同学在研究金属钒晶体时,以1个金属原子为中心,考查其它原子与它的距离。已知该晶体属于立方晶系,与该金属原子最近的原子核间距离为262.0pm,次近距离为302.5pm。请计算等放入金属钒晶体空隙中的最大原子半径_______ 。
 、V2O
、V2O 、V3O
、V3O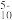 、VO
、VO 等,pH值决定着其主要以什么形式存在。
等,pH值决定着其主要以什么形式存在。(1)你认为pH越小,
(2)画出下列离子的结构图:VO


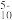
(3)某同学在研究金属钒晶体时,以1个金属原子为中心,考查其它原子与它的距离。已知该晶体属于立方晶系,与该金属原子最近的原子核间距离为262.0pm,次近距离为302.5pm。请计算等放入金属钒晶体空隙中的最大原子半径
【知识点】 晶体
您最近一年使用:0次
解答题-有机推断题
|
适中(0.65)
8. 昆虫信息素的研究一直是化学上研究的热点问题之一、下面是日本丽金龟信息素D的合成路线:

写出中间体A、B、C的结构_______ 、_______ 、_______ ,并用系统命名法命名日本丽金龟信息素D_______ 。

写出中间体A、B、C的结构
【知识点】 有机化学
您最近一年使用:0次
解答题-结构与性质
|
较难(0.4)
解题方法
9. 磷化硼是一种受到高度关注的耐磨涂料,它可用作金属的表面保护层。磷化硼可由三溴化硼和三溴化磷在氢气中高温反应合成。
(1)若磷化硼晶体中磷原子作六方最密堆积,硼原子填入四面体空隙中。画出磷化硼的正当晶胞示意图_______ ;
(2)已知磷化硼晶体中硼原子和磷原子的核间距为207pm,求该晶体的晶胞参数_______ ;
(3)在六方磷化硼正当晶胞中,磷原子形成许多空隙,若晶胞内磷原子的坐标为(0,0,0),( ,
, ,
, ),请写出未被硼原子占据空隙的分数坐标
),请写出未被硼原子占据空隙的分数坐标_______ ;
(4)画出六方磷化硼一个晶胞中的原子沿着c轴方向的投影_______ (用实线圆圈表示P原子的投影,用虚线圆圈表示B原子的投影)。
(5)若磷原子的半径为R,求在该晶体中磷原子形成的各种空隙能填下的最大原子半径____ 。
(1)若磷化硼晶体中磷原子作六方最密堆积,硼原子填入四面体空隙中。画出磷化硼的正当晶胞示意图
(2)已知磷化硼晶体中硼原子和磷原子的核间距为207pm,求该晶体的晶胞参数
(3)在六方磷化硼正当晶胞中,磷原子形成许多空隙,若晶胞内磷原子的坐标为(0,0,0),(
 ,
, ,
, ),请写出未被硼原子占据空隙的分数坐标
),请写出未被硼原子占据空隙的分数坐标(4)画出六方磷化硼一个晶胞中的原子沿着c轴方向的投影
(5)若磷原子的半径为R,求在该晶体中磷原子形成的各种空隙能填下的最大原子半径
【知识点】 晶胞的有关计算解读 金属晶体原子堆积模型解读 晶体
您最近一年使用:0次
四、填空题 添加题型下试题
填空题
|
较难(0.4)
10. 设丙烷和氢气都是理想气体。由石墨和氢气合成丙烷的反应如下:3C(石墨)+4H2 C3H8(g),丙烷在298K时的生成焓和熵值分别为-103.85kJ·mol-1和270.02J·K-1·mol-1,石墨和氢气的熵值分别为5.74J·K-1·mol-1和130.68J·K-1·mol-1。
C3H8(g),丙烷在298K时的生成焓和熵值分别为-103.85kJ·mol-1和270.02J·K-1·mol-1,石墨和氢气的熵值分别为5.74J·K-1·mol-1和130.68J·K-1·mol-1。
(1)在298K时,该反应能否自发进行____ ?求298K时上述反应的平衡常数____ ;
(2)若在298K及101.325kPa下反应,计算平衡时气相混合物中丙烷的摩尔分数_______ ;
(3)若希望丙烷在平衡时气相混合物中的摩尔分数达到0.95,298K时需要加多大的压力____ ?
(4)对有些反应,如水煤气变换反应CO(g)+H2O(g)⇌CO2(g)+H2O(g),加压并不能提高产率,但为什么在实际生产过程中需要加压_______ ?
 C3H8(g),丙烷在298K时的生成焓和熵值分别为-103.85kJ·mol-1和270.02J·K-1·mol-1,石墨和氢气的熵值分别为5.74J·K-1·mol-1和130.68J·K-1·mol-1。
C3H8(g),丙烷在298K时的生成焓和熵值分别为-103.85kJ·mol-1和270.02J·K-1·mol-1,石墨和氢气的熵值分别为5.74J·K-1·mol-1和130.68J·K-1·mol-1。(1)在298K时,该反应能否自发进行
(2)若在298K及101.325kPa下反应,计算平衡时气相混合物中丙烷的摩尔分数
(3)若希望丙烷在平衡时气相混合物中的摩尔分数达到0.95,298K时需要加多大的压力
(4)对有些反应,如水煤气变换反应CO(g)+H2O(g)⇌CO2(g)+H2O(g),加压并不能提高产率,但为什么在实际生产过程中需要加压
【知识点】 化学反应条件的控制及优化 化学平衡常数的有关计算解读 复合判据解读 化学平衡
您最近一年使用:0次
填空题
|
适中(0.65)
11. 化学的特征是创造新分子。若让你用1个氧和2个碳原子来创造分子,画出你认为这3个原子能够形成分子的结构图___ (原子用元素符号表示,每个分子必须同时含有1个氧和2个碳原子),并指出在这些分子中氧原子的杂化情况;若你认为他们不能形成分子,请说明原因___ 。
【知识点】 利用杂化轨道理论判断化学键杂化类型解读 分子结构
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:物质结构与性质、竞赛、化学反应原理、有机化学基础
试卷题型(共 11题)
题型
数量
解答题
6
填空题
5
试卷难度
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、解答题 | |||
| 1 | 0.65 | 配合物的结构与性质 晶胞的有关计算 晶体 | 结构与性质 |
| 5 | 0.65 | 几种常见的酮 有机推断综合考查 有机化学 | 有机推断题 |
| 6 | 0.65 | 有关有机物分子式确定的计算 根据价键规律确定有机结构式 有机化学 | 有机推断题 |
| 7 | 0.65 | 晶体 | 结构与性质 |
| 8 | 0.65 | 有机化学 | 有机推断题 |
| 9 | 0.4 | 晶胞的有关计算 金属晶体原子堆积模型 晶体 | 结构与性质 |
| 二、填空题 | |||
| 2 | 0.65 | 配合物 晶体 | |
| 3 | 0.4 | 分子结构 晶体 | |
| 4 | 0.65 | 溶液的酸碱性与pH 弱电解质的电离平衡常数 | |
| 10 | 0.4 | 化学反应条件的控制及优化 化学平衡常数的有关计算 复合判据 化学平衡 | |
| 11 | 0.65 | 利用杂化轨道理论判断化学键杂化类型 分子结构 | |



