2015届山东省滕州市实验中学高三12月月考理综化学试卷
山东
高三
阶段练习
2017-07-26
270次
整体难度:
适中
考查范围:
化学实验基础、认识化学科学、有机化学基础、常见无机物及其应用、化学反应原理
2015届山东省滕州市实验中学高三12月月考理综化学试卷
山东
高三
阶段练习
2017-07-26
270次
整体难度:
适中
考查范围:
化学实验基础、认识化学科学、有机化学基础、常见无机物及其应用、化学反应原理
一、单选题 添加题型下试题
单选题
|
适中(0.65)
名校
1. 下列说法错误的是( )
| A.萃取操作时,选择有机萃取剂,则溶质在萃取剂的溶解度必须比水大 |
| B.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| C.蒸馏操作时,应使温度计水银球插入混合溶液的液面下 |
| D.配制一定物质的量浓度的溶液时,洗涤烧杯和玻璃棒的溶液必须转入容量瓶中 |
【知识点】 物质分离、提纯的常见物理方法
您最近一年使用:0次
2016-12-09更新
|
194次组卷
|
9卷引用:2012-2013学年福建省福州八县一中高一上学期期末联考化学试卷
(已下线)2012-2013学年福建省福州八县一中高一上学期期末联考化学试卷(已下线)2015届黑龙江省哈尔滨市第32中学高三上学期期中考试化学试卷(已下线)2015届黑龙江省绥化市三校高三上学期期中联考化学试卷2014-2015河南省扶沟县高中高二上学期第三次考试化学试卷2015届山东省滕州市实验中学高三12月月考理综化学试卷2015届河南省郑州盛同学校高三12月月考化学试卷12015届河南省郑州盛同学校高三12月月考化学试卷2黑龙江省哈尔滨市第三十二中学2018届高三上学期期中考试化学试题吉林省长春市九台区第四中学2019-2020学年高一上学期期中考试化学试题
单选题
|
适中(0.64)
2. 在下列溶液中,能大量共存的离子组是
| A.能使pH试纸显蓝色的溶液中:K+、Ba2+、H+、Br- |
| B.加入Al能放出H2的溶液中:K+、Na+、NO3-、Cl- |
| C.含有大量Fe3+的溶液中:SCN-、I-、K+、Br- |
D.能使石蕊试液显红色的溶液中:K+、 、S2-、 、S2-、 |
【知识点】 离子共存
您最近一年使用:0次
2016-12-09更新
|
128次组卷
|
2卷引用:2015届山东省济宁市育才中学高三上学期期中化学试卷
单选题
|
适中(0.64)
3. .绿色化学的核心是反应过程的绿色化,即要求原料物质中的所有原子完全被利用且全部转入期望的产品中,下列过程不符合这一思想的是
A.甲烷与氯气反应制氯仿:CH4+3Cl2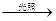 CHCl3+3HCl CHCl3+3HCl |
B.烯烃与水煤气发生的羰基合成反应:RCH=CH2+CO+H2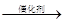 RCH2CH2CHO RCH2CH2CHO |
C.甲烷、CO合成乙酸乙酯:2CH4+2CO 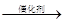 CH3COOCH2CH3 CH3COOCH2CH3 |
D.乙烯合成聚乙烯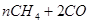  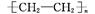 |
【知识点】 合成有机高分子的基本方法
您最近一年使用:0次
单选题
|
适中(0.64)
4. 下列所陈述的事实与解释均正确的是
| 选项 | 事实 | 解释 |
| A | 用pH试纸测出新制氯水的pH为3 | 新制氯水有酸性 |
| B | 用C2H5OH与浓硫酸170℃共热,制得气体使酸性KMnO4溶液褪色 | 一定是制得的乙烯与酸性KMnO4溶液褪色 |
| C | 收集铜与浓硝酸反应生成的气体,用冰水混合物冷却降温,气体颜色变浅 | 生成的红棕色NO2气体部分转化为无色气体 |
| D | 甲苯能使酸性高锰酸钾溶液褪色 | 发生了萃取 |
| A.A | B.B | C.C | D.D |
【知识点】 氮族元素及其化合物
您最近一年使用:0次
单选题
|
较易(0.85)
名校
解题方法
5. 某硫酸厂废气中SO2的回收利用方案如图所示。下列说法错误的是( )


| A.X可能含有2种盐 | B.Y可能含有(NH4)2SO4 |
| C.a是SO3 | D.(NH4)2S2O8中S的化合价不可能为+7 |
【知识点】 二氧化硫 物质分离、提纯综合应用解读 物质制备的探究解读
您最近一年使用:0次
2020-03-21更新
|
231次组卷
|
13卷引用:2013-2014学年福建省福州八市一中高一下学期期中考试化学试卷
(已下线)2013-2014学年福建省福州八市一中高一下学期期中考试化学试卷2015届山东省高密市高三12月检测理综化学试卷2015届山东省滕州市实验中学高三12月月考理综化学试卷2016届福建省厦门一中高三下学期周考六理综化学试卷2017届河北省衡水中学高三上期中化学卷黑龙江省鹤岗市第一中学2016-2017学年高二下学期期末考试化学试题湖北省宜昌市葛洲坝中学2018届高三9月月考化学试题上海市六校2015年高三下学期第二次联考化学试题(已下线)第6单元 常见的非金属元素(B卷 滚动提升检测)-2021年高考化学一轮复习单元滚动双测卷(已下线)考向12 硫及其化合物-备战2022年高考化学一轮复习考点微专题广东省七校联合体2021-2022学年高三上学期第二次联考(11月)化学试题江西省丰城中学2021-2022学年上学期高三创新实验班第四次月考化学试题湖南省株洲市九方中学2022届高三下学期4月月考化学试题
单选题
|
适中(0.64)
6. 某离子反应涉及H2O、ClO—、IO3—、OH—、I2、Cl—六种微粒。其中c(ClO—)随反应进行逐渐减小。下列判断错误的是
| A.该反应的还原剂是I2 |
| B.氧化剂与还原剂的物质的量之比为5:2 |
| C.消耗1 mol氧化剂,转移2 mol电子 |
| D.反应后溶液的碱性明显减弱 |
【知识点】 氧化还原反应基本概念 氧化还原反应有关计算
您最近一年使用:0次
2016-12-09更新
|
140次组卷
|
2卷引用:2015届山东省高密市高三12月检测理综化学试卷
单选题
|
适中(0.64)
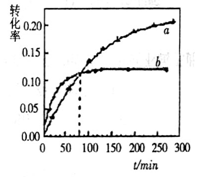
7. 丙酮(CH3COCH3)在某溶剂里,在催化剂作用下发生反应: 取相同浓度的
取相同浓度的 ,分别在40℃和60℃时,测得其转化率
,分别在40℃和60℃时,测得其转化率 随时间变化的关系曲线(
随时间变化的关系曲线( )如图所示。下列说法正确的是
)如图所示。下列说法正确的是
 取相同浓度的
取相同浓度的 ,分别在40℃和60℃时,测得其转化率
,分别在40℃和60℃时,测得其转化率 随时间变化的关系曲线(
随时间变化的关系曲线( )如图所示。下列说法正确的是
)如图所示。下列说法正确的是
A.b代表40℃时 的 的 曲线 曲线 |
| B.升高温度可缩短该反应达平衡的时间并能提高平衡转化率 |
| C.增大压强可缩短该反应达平衡的时间并能提高平衡转化率 |
| D.上述反应的逆反应为吸热反应 |
【知识点】 化学平衡
您最近一年使用:0次
二、填空题 添加题型下试题
填空题
|
困难(0.15)
8. (1)利用H2S废气制取氢气的方法有多种。
①高温热分解法:已知: 在恒容密闭容器中,控制不同温度进行H2S分解实验。
在恒容密闭容器中,控制不同温度进行H2S分解实验。

以H2S起始浓度均为c mol/L测定H2S的转化率,结果见图。图中a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率。 _____________0(填>,=或<):说明随温度的升高,曲线b向曲线a靠近的原因: _____________________。
_____________0(填>,=或<):说明随温度的升高,曲线b向曲线a靠近的原因: _____________________。
②电化学法
该法制氢过程的示意图如图。反应池中反应的离子方程式是___________________;
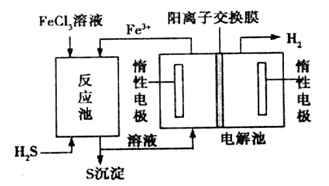
反应后的溶液进入电解池,电解总反应的离子方程式为________________。
(2)以Al和NiO(OH)为电极,NaOH溶液为电解液可以组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2。
①该电池的负极反应式_______________________________________________。
②电池总反应的化学方程式_________________________________________________。
(3)某亚硝酸钠固体中可能含有碳酸钠和氢氧化钠,现测定亚硝酸钠的含量。
已知:5NaNO2+2KMnO4+3H2SO4=5NaNO3+2MnSO4+K2SO4+3H2O
称取4.000g固体,溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol/L,酸性KmnO4溶液进行滴定,实验所得数据如下表所示;
①滴入最后一滴酸性KMnO4溶液,溶液__________________________,30秒内不恢复,可判断达到滴定终点。
②第一组实验数据出现异常,造成这种异常的原因可能是____________(填序号)。
A.酸式滴定管用蒸馏水洗净后未用标准液润洗
B.锥形瓶洗净后未干燥
C.滴定终了仰视读数
③根据表中数据,计算所得固体中亚硝酸钠的质量分数_____________。
①高温热分解法:已知:
 在恒容密闭容器中,控制不同温度进行H2S分解实验。
在恒容密闭容器中,控制不同温度进行H2S分解实验。
以H2S起始浓度均为c mol/L测定H2S的转化率,结果见图。图中a为H2S的平衡转化率与温度关系曲线,b曲线表示不同温度下反应经过相同时间且未达到化学平衡时H2S的转化率。
 _____________0(填>,=或<):说明随温度的升高,曲线b向曲线a靠近的原因: _____________________。
_____________0(填>,=或<):说明随温度的升高,曲线b向曲线a靠近的原因: _____________________。②电化学法
该法制氢过程的示意图如图。反应池中反应的离子方程式是___________________;

反应后的溶液进入电解池,电解总反应的离子方程式为________________。
(2)以Al和NiO(OH)为电极,NaOH溶液为电解液可以组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2。
①该电池的负极反应式_______________________________________________。
②电池总反应的化学方程式_________________________________________________。
(3)某亚硝酸钠固体中可能含有碳酸钠和氢氧化钠,现测定亚硝酸钠的含量。
已知:5NaNO2+2KMnO4+3H2SO4=5NaNO3+2MnSO4+K2SO4+3H2O
称取4.000g固体,溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol/L,酸性KmnO4溶液进行滴定,实验所得数据如下表所示;
| 滴定次数 | 1 | 2 | 3 | 4 |
| KMnO4溶液体积/mL | 20.60 | 20.02 | 20.00 | 19.98 |
①滴入最后一滴酸性KMnO4溶液,溶液__________________________,30秒内不恢复,可判断达到滴定终点。
②第一组实验数据出现异常,造成这种异常的原因可能是____________(填序号)。
A.酸式滴定管用蒸馏水洗净后未用标准液润洗
B.锥形瓶洗净后未干燥
C.滴定终了仰视读数
③根据表中数据,计算所得固体中亚硝酸钠的质量分数_____________。
您最近一年使用:0次
三、解答题 添加题型下试题
解答题-实验探究题
|
较易(0.85)
名校
9. 某工厂对工业生产钛白粉产生的废液进行综合利用,废液中含有大量FeSO4、H2SO4和少量Fe2(SO4)3、TiOSO4,可用于生产颜料铁红和补血剂乳酸亚铁.其生产工艺流程如下:
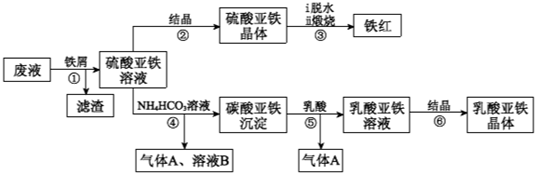
已知:①TiOSO4可溶于水,在水中可以电离为TiO2+和SO42-;
②TiOSO4水解的反应为:TiOSO4+(x+1)H2O→TiO2•xH2O↓+H2SO4.
请回答:
(1)步骤①所得滤渣的主要成分为_____________ ,
(2)步骤③硫酸亚铁在空气中煅烧生成铁红和三氧化硫,该反应中氧化剂和还原剂的物质的量之比为_____________ ,
(3)步骤④需控制反应温度低于35℃,其目的是_____________ ,
(4)步骤④的离子方程式是_____________ ,
(5)已知:FeCO3(S) Fe2+(aq)+CO32-(aq),试用平衡移动原理解释步骤⑤生成乳酸亚铁的原因
Fe2+(aq)+CO32-(aq),试用平衡移动原理解释步骤⑤生成乳酸亚铁的原因_____________ ,
(6)溶液B常被用于电解生产(NH4)2S2O8(过二硫酸铵)。电解时均用惰性电极,阳极发生的电极反应可表示为_____________ ,
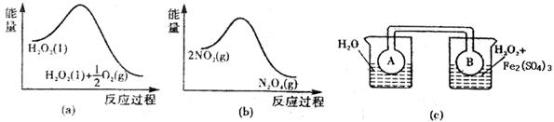
(7)Fe3+对H2O2的分解具有催化作用.利用图2(a)和(b)中的信息,按图2(c)装置(连通的A、B瓶中已充有NO2气体)进行实验.可观察到B瓶中气体颜色比A瓶中的深,其原因是_____________ 。

已知:①TiOSO4可溶于水,在水中可以电离为TiO2+和SO42-;
②TiOSO4水解的反应为:TiOSO4+(x+1)H2O→TiO2•xH2O↓+H2SO4.
请回答:
(1)步骤①所得滤渣的主要成分为
(2)步骤③硫酸亚铁在空气中煅烧生成铁红和三氧化硫,该反应中氧化剂和还原剂的物质的量之比为
(3)步骤④需控制反应温度低于35℃,其目的是
(4)步骤④的离子方程式是
(5)已知:FeCO3(S)
 Fe2+(aq)+CO32-(aq),试用平衡移动原理解释步骤⑤生成乳酸亚铁的原因
Fe2+(aq)+CO32-(aq),试用平衡移动原理解释步骤⑤生成乳酸亚铁的原因(6)溶液B常被用于电解生产(NH4)2S2O8(过二硫酸铵)。电解时均用惰性电极,阳极发生的电极反应可表示为
(7)Fe3+对H2O2的分解具有催化作用.利用图2(a)和(b)中的信息,按图2(c)装置(连通的A、B瓶中已充有NO2气体)进行实验.可观察到B瓶中气体颜色比A瓶中的深,其原因是

您最近一年使用:0次
2016-12-09更新
|
112次组卷
|
4卷引用:2015届山东省高密市高三12月检测理综化学试卷
四、填空题 添加题型下试题
填空题
|
适中(0.65)
10. 下图表示的化合物Ⅰ的名称为甲基环氧乙烷,化合物Ⅰ常用于制备药物和合成高分子材料。
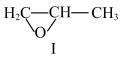
(1)化合物Ⅰ的分子式为______________ 。
(2)化合物Ⅰ在催化剂作用下能与水发生反应得到二元醇,该反应的化学方程式为__________________ 。
(3)慢心律是一种治疗心律失常的药物,它的合成路线如下:
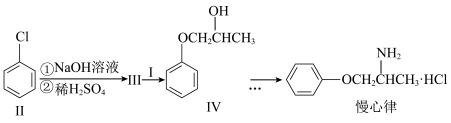
①Ⅲ+Ⅰ→Ⅳ的反应类型为________ ;Ⅲ的结构简式为_________________ 。
②写出化合物Ⅲ与浓溴水反应的化学方程式:______________________ 。
③由Ⅲ和Ⅰ制备Ⅳ的过程中有少量副产物V生成,V与Ⅳ互为同分异构体,V的结构简式为_______________ 。
(4)已知: +CH3COOH→
+CH3COOH→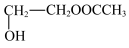 聚合物
聚合物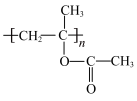 可用于制备高吸水性树脂,其单体的结构简式为
可用于制备高吸水性树脂,其单体的结构简式为__________________ 。以CH3COOH和化合物I为原料可合成该单体,涉及的反应的化学方程式为____________ 、_____________ 。

(1)化合物Ⅰ的分子式为
(2)化合物Ⅰ在催化剂作用下能与水发生反应得到二元醇,该反应的化学方程式为
(3)慢心律是一种治疗心律失常的药物,它的合成路线如下:

①Ⅲ+Ⅰ→Ⅳ的反应类型为
②写出化合物Ⅲ与浓溴水反应的化学方程式:
③由Ⅲ和Ⅰ制备Ⅳ的过程中有少量副产物V生成,V与Ⅳ互为同分异构体,V的结构简式为
(4)已知:
 +CH3COOH→
+CH3COOH→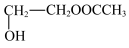 聚合物
聚合物 可用于制备高吸水性树脂,其单体的结构简式为
可用于制备高吸水性树脂,其单体的结构简式为
您最近一年使用:0次
2016-12-09更新
|
332次组卷
|
2卷引用:2015届山东省高密市高三12月检测理综化学试卷
填空题
|
较难(0.4)
11. 【化学——有机化学基础】
“心得安”是治疗心脏病的药物,下面是它的一种合成路线(具体反应条件和部分试剂略):
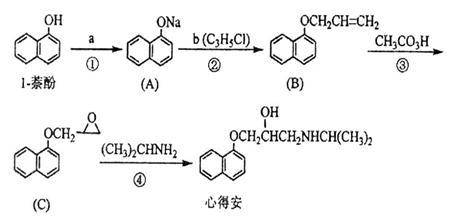
回答下列问题:
(1)试剂a是_________________ 。
(2)③的反应类型是______________ 。
(3)试剂b可由丙烷经三步反应合成:
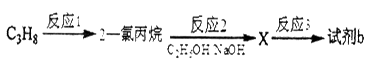
反应l的试剂与条件__________________ ;
反应2的化学方程式为_______________________________________________ ;
反应3的反应方程式为_______________________________________________ 。
(4)芳香化合物D
_____ (填“是”或“不是”)1—萘酚的同分异构体。
“心得安”是治疗心脏病的药物,下面是它的一种合成路线(具体反应条件和部分试剂略):

回答下列问题:
(1)试剂a是
(2)③的反应类型是
(3)试剂b可由丙烷经三步反应合成:
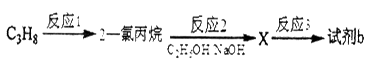
反应l的试剂与条件
反应2的化学方程式为
反应3的反应方程式为
(4)芳香化合物D

【知识点】 有机物的合成与推断
您最近一年使用:0次
2016-12-08更新
|
241次组卷
|
2卷引用:2015届山东省高密市高三12月检测理综化学试卷
试卷分析
整体难度:适中
考查范围:化学实验基础、认识化学科学、有机化学基础、常见无机物及其应用、化学反应原理
试卷题型(共 11题)
题型
数量
单选题
7
填空题
3
解答题
1
试卷难度
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 物质分离、提纯的常见物理方法 | |
| 2 | 0.64 | 离子共存 | |
| 3 | 0.64 | 合成有机高分子的基本方法 | |
| 4 | 0.64 | 氮族元素及其化合物 | |
| 5 | 0.85 | 二氧化硫 物质分离、提纯综合应用 物质制备的探究 | |
| 6 | 0.64 | 氧化还原反应基本概念 氧化还原反应有关计算 | |
| 7 | 0.64 | 化学平衡 | |
| 二、填空题 | |||
| 8 | 0.15 | 化学平衡 电解池 | |
| 10 | 0.65 | 苯酚与溴水的反应 加聚物的单体、链节及聚合度的确定 根据题给物质选择合适合成路线 有机合成综合考查 | |
| 11 | 0.4 | 有机物的合成与推断 | |
| 三、解答题 | |||
| 9 | 0.85 | 化学平衡的移动及其影响因素 物质分离、提纯综合应用 物质性质实验方案的设计 | 实验探究题 |



