3.

是一种氧化剂,可以用来制取氯气。
(1)高锰酸钾溶于水的电离方程式为
_______。它属于
_______(选填“强电解质”、“弱电解质”、“非电解质”);
(2)已知高锰酸钾固体在室温下能将浓盐酸氧化,发生反应:
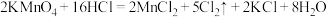
①标明上述化学方程式电子转移方向和数目
_______。
②在该反应中,被还原的元素是
_______,浓盐酸体现了
_______性质(选填字母编号),氧化剂与还原剂的物质的量之比为
_______。
A. 酸性
B. 碱性
C. 氧化性
D. 还原性
③产生

,则转移的电子数目为
_______。
④下列装置中,可用作该反应的气体发生装置的是(选填字母编号)
_______。
A.
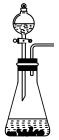
B.
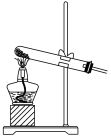
C.
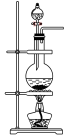
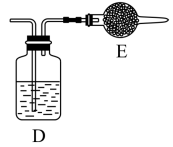
⑤用上述方法制得的氯气中含有杂质,可依次用如图洗气装置净化。装置D中应盛放
_______,装置E中可盛放
_______(均选填字母编号)
A. 浓硫酸
B. NaOH溶液
C. 饱和食盐水
D. 固体

E. 碱石灰
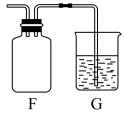
⑥氯气可用排空气法收集,装置G中盛放为NaOH溶液,作用是
_______,并写出反应的离子方程式
_______。
(3)实验室可通过置换反应完成卤素单质活泼性比较的实验。某实验小组设计了装置如图,回答下列问题:
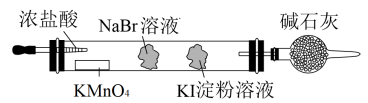
该装置中,吸有KI淀粉溶液的棉球颜色变为
_______。吸有NaBr溶液的棉球中发生反应的离子方程式为
_______。由反应现象能否得出活泼性

的结论?回答并说明理由
_______。
(4)COVID-19在全球的蔓延,对人类的健康和全球的经济带来了很大的影响,为了控制疫情,全球进行了大面积的消杀工作,消毒液发挥了重要的作用,请回答下列有关消毒液的问题。
①生产消毒液是将氯气通入NaOH溶液中,取少量该消毒液滴加酸性

溶液,现象是出现白色沉淀,说明消毒液中有
_______(填离子符号)。
②消毒液稀释后喷洒在空气中,可以生成有漂白性的物质和碳酸氢钠,请写出此过程的化学方程式:
_______;该物质有漂白性是因为它有强氧化性,但是它也很不稳定,请写出它分解的化学方程式:
_______。