上海市行知中学2022-2023学年高二下学期第二次月考化学试题
上海
高二
阶段练习
2023-07-07
84次
整体难度:
适中
考查范围:
认识化学科学、化学反应原理、有机化学基础、物质结构与性质
上海市行知中学2022-2023学年高二下学期第二次月考化学试题
上海
高二
阶段练习
2023-07-07
84次
整体难度:
适中
考查范围:
认识化学科学、化学反应原理、有机化学基础、物质结构与性质
一、填空题 添加题型下试题
填空题
|
适中(0.65)
名校
解题方法
1. 1887年,阿伦尼乌斯在他的《关于溶质在水中的离解》一文中阐述了电离学说的基本观点,他提出“由于溶剂的作用,电解质在水中自动离解成带相反电荷的正、负离子”。
(1)下列属于含有非极性键的强电解质的是_________
(2)下列微粒中,对水的电离平衡不产生影响的是_________
(3)有关叙述正确的是_________
(4)实验室配制FeCl3溶液时,常将FeCl3固体先溶于较浓的盐酸中,再用蒸馏水稀释到所需的浓度,其目的是___________ (结合离子方程式说明)。
(5)等体积混合浓度均为0.1mol/L的氨水和盐酸,所得溶液中离子浓度由大到小的顺序是___________ 。
(6)现有常温下0.1mol/L的纯碱溶液。同学甲就该溶液中粒子间的关系写出了下列四个关系式,你认为其中正确的是___________ 。
a. [Na+]=2[ ] b. [
] b. [ ]>[OH-]>[
]>[OH-]>[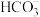 ]>[H2CO3]
]>[H2CO3]
c. [ ]+[
]+[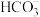 ]=0.1mol/L d. [OH-]=[H+]+[
]=0.1mol/L d. [OH-]=[H+]+[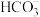 ]+2[H2CO3]
]+2[H2CO3]
(7)现有常温下0.1mol/L的纯碱溶液。同学乙向该溶液中滴几滴酚酞并充分振荡后,再向该溶液中滴入CaCl2溶液,观察到的现象是___________ ,原因是___________ 。
(1)下列属于含有非极性键的强电解质的是_________
| A.HBr | B.Na2O2 | C.KOH | D.NH4Cl |
A. | B.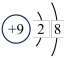 | C.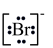 | D.1s22s22p63s1 |
A.加入铝粉生成H2的溶液中,K+、Cu2+、SO 、ClO-可能大量共存 、ClO-可能大量共存 |
B.在[OH-]=10-2mol/L的溶液中,NO 、K+、Cl-、SO 、K+、Cl-、SO 能大量共存 能大量共存 |
C.0.1mol/L NaHCO3溶液中:[CO ]+[OH-]=[H2CO3]+[H+] ]+[OH-]=[H2CO3]+[H+] |
D.0.1mol/L NaHSO3溶液中:[Na+]>[SO ]>[OH-]>[HSO ]>[OH-]>[HSO ]>[H+] ]>[H+] |
(5)等体积混合浓度均为0.1mol/L的氨水和盐酸,所得溶液中离子浓度由大到小的顺序是
(6)现有常温下0.1mol/L的纯碱溶液。同学甲就该溶液中粒子间的关系写出了下列四个关系式,你认为其中正确的是
a. [Na+]=2[
 ] b. [
] b. [ ]>[OH-]>[
]>[OH-]>[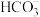 ]>[H2CO3]
]>[H2CO3]c. [
 ]+[
]+[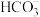 ]=0.1mol/L d. [OH-]=[H+]+[
]=0.1mol/L d. [OH-]=[H+]+[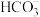 ]+2[H2CO3]
]+2[H2CO3](7)现有常温下0.1mol/L的纯碱溶液。同学乙向该溶液中滴几滴酚酞并充分振荡后,再向该溶液中滴入CaCl2溶液,观察到的现象是
您最近一年使用:0次
二、解答题 添加题型下试题
2. 我们通过更深入地研究化学反应的方向、限度和速率,利用这些规律来解决日常生活和工业生产中的实际问题,让生活更美好。
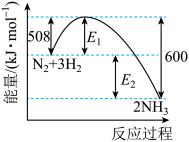
(1)一定条件下,在密闭容器中,氮气与氢气合成氨气,能量变化曲线如图所示。下列说法正确的是___________
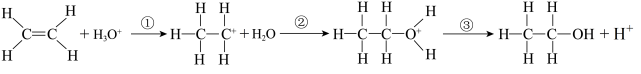
(2)乙烯与水通过加成反应可得乙醇。反应机理、能量变化与反应进程的关系如图所示:
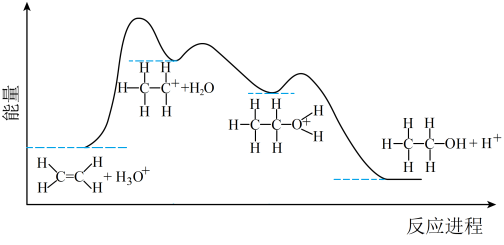
下列叙述正确的是________
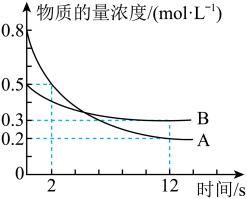
(3)某温度下,在2L恒容密闭容器中投入一定量的A、B,发生反应:3A(g)+bB(g) cC(g)+2D(s),12s时生成C的物质的量为0.8mol(反应进程如图所示)。下列说法中正确的是__________
cC(g)+2D(s),12s时生成C的物质的量为0.8mol(反应进程如图所示)。下列说法中正确的是__________
(4)一定条件下N2O发生如下反应:
Ⅰ. 2N2O(g) 2N2(g)+O2(g)
2N2(g)+O2(g)  =-164kJ·mol-1
=-164kJ·mol-1
Ⅱ. N2O(g)+CO(g) N2(g)+CO2(g)
N2(g)+CO2(g)  =-356kJ·mol-1
=-356kJ·mol-1
①反应Ⅰ平衡常数的表达式K=___________ 。
②恒温恒容条件下,下列可以作为判断反应Ⅰ达到平衡的依据是___________ 。
a. 气体的压强不变 b. 2v正(N2O)=v逆(O2) c. K不变 d. 容器内气体的密度不变
③某温度下,反应Ⅰ的K=0.16,该温度下,测得容器中N2O、N2、O2的浓度分别为0.5mol·L-1、0.5mol·L-1、0.25mol·L-1,此时,反应Ⅰ是否处于平衡状态? 若不是,预测反应的方向。___________
(5)甲为10L的恒温容器。盛有1mol N2O和1mol CO,发生反应Ⅰ和反应Ⅱ,5min时,测得CO转化率为60%,n(N2):n(O2)=8:1,则n(N2O)=___________ mol;0~5min,O2的平均反应速率v(O2)=___________ mol·L-1·min-1。
(6)不同压强的密闭容器中分别充入1mol N2O和1mol CO,发生反应Ⅰ和反应Ⅱ,测得N2O的平衡转化率与温度的关系如图所示。

P1、P2、P3由小到大的顺序为___________ ;温度高于T0℃时,容器内发生的主要反应为___________ (填“Ⅰ”、“Ⅱ”或“Ⅰ和Ⅱ”)。
(1)一定条件下,在密闭容器中,氮气与氢气合成氨气,能量变化曲线如图所示。下列说法正确的是___________

| A.加入催化剂,E1、E2都变小 |
B.N2(g)+3H2(g)  2NH3(g) 2NH3(g)  =-600kJ·mol-1 =-600kJ·mol-1 |
| C.升温可以增大该反应的化学平衡常数 |
| D.通入1mol N2和3mol H2充分反应,放热小于92kJ |


下列叙述正确的是________
| A.①、②、③三步均属于加成反应 |
| B.H+为反应的催化剂 |
| C.①、②、③三步反应均为放热反应 |
| D.总反应是放热反应,不需要加热就能发生 |
 cC(g)+2D(s),12s时生成C的物质的量为0.8mol(反应进程如图所示)。下列说法中正确的是__________
cC(g)+2D(s),12s时生成C的物质的量为0.8mol(反应进程如图所示)。下列说法中正确的是__________
| A.0-2s,D的平均反应速率为0.1mol/(L·s) |
| B.12s时,B的转化率为40% |
| C.化学计量系数之比b:c=1:2 |
| D.图中两曲线相交时,A的消耗速率等于A的生成速率 |
Ⅰ. 2N2O(g)
 2N2(g)+O2(g)
2N2(g)+O2(g)  =-164kJ·mol-1
=-164kJ·mol-1Ⅱ. N2O(g)+CO(g)
 N2(g)+CO2(g)
N2(g)+CO2(g)  =-356kJ·mol-1
=-356kJ·mol-1①反应Ⅰ平衡常数的表达式K=
②恒温恒容条件下,下列可以作为判断反应Ⅰ达到平衡的依据是
a. 气体的压强不变 b. 2v正(N2O)=v逆(O2) c. K不变 d. 容器内气体的密度不变
③某温度下,反应Ⅰ的K=0.16,该温度下,测得容器中N2O、N2、O2的浓度分别为0.5mol·L-1、0.5mol·L-1、0.25mol·L-1,此时,反应Ⅰ是否处于平衡状态? 若不是,预测反应的方向。
(5)甲为10L的恒温容器。盛有1mol N2O和1mol CO,发生反应Ⅰ和反应Ⅱ,5min时,测得CO转化率为60%,n(N2):n(O2)=8:1,则n(N2O)=
(6)不同压强的密闭容器中分别充入1mol N2O和1mol CO,发生反应Ⅰ和反应Ⅱ,测得N2O的平衡转化率与温度的关系如图所示。

P1、P2、P3由小到大的顺序为
您最近一年使用:0次



