19. 某学生对SO
2与漂粉精的反应进行实验探究:
操作
| 现象
|
取适量漂粉精固体,加入100mL水
| 部分固体溶解,溶液略有颜色
|
过滤,测漂粉精溶液的pH
| pH试纸先变蓝,后褪色
|
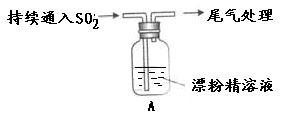
| 液面上方出现白雾;
稍后,出现浑浊,溶液变为黄绿色;
稍后,产生大量白色沉淀,黄绿色褪去
|
(1)写出C1
2和Ca(OH)
2制取漂粉精的化学方程式
;
(2)向水中持续通入SO
2,未观察到白雾。推测现象i的白雾由HCl小液滴形成,进行如下实验:
a.用湿润的碘化钾淀粉试纸检验白雾,无变化;
b.用酸化的AgNO
3溶液检验白雾,产生白色沉淀。
①实验a目的是
;
②由实验a、b不能判断白雾中含有HCl,理由是
;
(3)将A瓶中混合物过滤、洗涤,得到沉淀X
①向沉淀X中加入稀HCl,无明显变化。取上层清液,加入BaC1
2溶液,产生白色沉淀。则沉淀X中含有的物质是
;
②用离子方程式解释现象iii中黄绿色褪去的原因:
。
(4)测定漂粉精有效成分的质量分数。称取2.000 g漂粉精于锥形瓶中,加水溶解,调节溶液的pH,以淀粉为指示剂,用0.2000 mol·L
-1 KI溶液进行滴定,溶液出现稳定浅蓝色时为滴定终点。反应原理为:3C1O
-+ I
- ="=" 3C1
-+ IO
3-IO
3- + 5I
-+ 3H
2O ="=" 6OH
-+ 3I
2实验测得数据如下表所示。
滴定次数
| 1
| 2
| 3
|
KI溶液体积/mL
| 19.98
| 20.02
| 20.00
|
该漂白粉中有效成分的质量分数为
。