2015-2016学年安徽省芜湖市高一下模块考试化学试卷
安徽
高一
阶段练习
2017-07-27
246次
整体难度:
适中
考查范围:
化学反应原理、物质结构与性质、常见无机物及其应用、有机化学基础、认识化学科学、化学实验基础
一、单选题 添加题型下试题
| A.向甲溶液中加入BaCl2溶液,有白色沉淀产生 |
| B.向乙溶液中加入BaCl2溶液,有白色沉淀产生,再加入盐酸沉淀不溶解 |
| C.向丙溶液中加入盐酸使之酸化,无白色沉淀,再加入BaCl2溶液,有白色沉淀产生 |
| D.向丁溶液中加入硝酸酸化,再加入硝酸钡溶液,有白色沉淀产生 |
| A.酸碱中和反应可设计为原电池 |
| B.煤燃烧时化学能只转换为热能 |
| C.太阳能热水器将太阳能转化为热能 |
| D.在化学反应中不一定发生能量变化 |
【知识点】 反应热
| A.油脂在空气中完全燃烧生成H2O和CO2 |
| B.淀粉和纤维素互为同分异构体 |
| C.金属钠可区分乙醇和乙酸 |
| D.苯与饱和溴水混合,发生了取代反应 |
二、未知 添加题型下试题
| A.NH3易液化,液氨常用作制冷剂 |
| B.稀HNO3氧化能力弱于浓HNO3 |
| C.贮存铵态氮肥时要密封保存,并放在阴凉处 |
| D.硝酸只能被Zn、Fe等金属还原成H2 |
【知识点】 氮族元素及其化合物
三、单选题 添加题型下试题
A.F-的原子结构示意图:  | B.乙烯的结构简式:CH2CH2 |
| C.葡萄糖的分子式:C6H12O6 | D.二氧化碳的电子式:  |
【知识点】 化学用语

| A.Zn为负极,Cu为正极 |
| B.正极反应为 Zn-2e-=Zn2+ |
| C.电子从Cu极流出 |
| D.该装置是将电能转化为化学能 |
【知识点】 原电池
 2HI(g)达到平衡状态的标志的是
2HI(g)达到平衡状态的标志的是| A.H—H键和H-I键断键的数目比为1∶2 |
| B.容器内气体的总压强不再变化 |
| C.H2的体积分数不再变化 |
| D.混合气体的颜色不再变化 |
【知识点】 化学平衡
| A.新制的氯水中只含有Cl2和H2O分子 |
| B.新制的氯水可使蓝色石蕊试纸先变红后褪色 |
| C.加入盐酸,再加AgNO3溶液,能说明有Cl-存在 |
| D.氯水放置数天后,溶液酸性减弱 |
【知识点】 卤素及其化合物
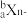 ,下列有关该原子的说法正确的是
,下列有关该原子的说法正确的是A.含有的中子数为 | B.含有的电子数为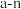 |
C.质量数为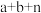 | D.1 该原子的质量约为b g 该原子的质量约为b g |
【知识点】 原子的基本构成解读 原子中相关数值及其之间的相互关系解读
| A.v(X)=0.05 mol·L−1·min−1 |
| B.v(Y)=0.10 mol·L−1·min−1 |
| C.v(Z)=0.10 mol·L−1·min−1 |
| D.v(W)=0.05 mol·L−1·s−1 |
① NaBr ② FeCl3 ③ Na2SO3 ④ AlCl3 ⑤ FeSO4 ⑥ NaHCO3
| A.①③ | B.②④ | C.③④⑥ | D.②③④ |
【知识点】 卤素及其化合物

| A.上下移动①中铜丝可减少SO2的污染 |
| B.②中选用NaOH溶液验证SO2的生成 |
| C.③中选用Ca(OH)2溶液吸收多余的SO2 |
| D.为确认CuSO4生成,向①中加水,观察颜色 |
① 烧碱 ② 纯碱 ③ 金属钠 ④ 氯气 ⑤ 盐酸 ⑥ NaClO
| A.全部 | B.①②③④⑤ | C.①②③⑤⑥ | D.①②④⑤⑥ |

| A.离子半径:乙 <丁 <戊 | B.金属性:甲 >丙 >丁 |
| C.氢氧化物碱性:丙 >丁 >戊 | D.最高化合价:甲 >乙 >戊 |
【知识点】 元素周期表 元素周期律
| A.2种 | B.3种 | C.4种 | D.5种 |
【知识点】 同分异构体的数目的确定解读
| A.O3比O2稳定,由O2转化为O3是吸热反应 |
| B.O2比O3稳定,由O2转化为O3是放热反应 |
| C.等质量的O2比O3能量低,由O2转化为O3是吸热反应 |
| D.等质量的O2比O3能量高,由O2转化为O3是放热反应 |
【知识点】 反应热
| A.a∶b=4∶1 | B.a∶b=4∶3 | C.a="4b+c" | D.a=4b+3c |
【知识点】 氮族元素及其化合物
四、填空题 添加题型下试题
(1)由2个原子核和2个电子形成的分子是
(2)由5个原子核和10个电子形成的分子是
(3)由3个最外层是6个电子的同种原子形成的分子是
(4)由最外层是1个和5个电子的原子形成18个电子的分子是
【知识点】 元素周期表 元素周期律

(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为
(2)这些元素中的最高价氧化物对应的水化物中,酸性最强的是,碱性最强的是
(3)用电子式表示②与④形成化合物的过程
(4)单质⑤与③的最高价氧化物对应的水化物反应的离子方程式是
(5)①和⑥形成的化合物是一种新型的高温结构陶瓷,该化合物中含有的化学键类型是
(6)②、③和⑦元素的原子半径由大到小的顺序是
【知识点】 元素周期表 元素周期律

(1)若以反应中消耗的HCl表示反应速率,设OE段的反应速率为v1,EF段的反应速率为v2,FG段的反应速度为v3,则v1、v2、v3从大到小的顺序为
(2)为了减缓上述反应的速率,欲向该溶液中加入下列物质,你认为可行的是
| A.蒸馏水 | B.Na2CO3 | C.氯化钠溶液 | D.浓盐酸 |
(3)若反应过程中溶液体积的变化忽略不计,则EF段用盐酸表示的化学反应速率v(HCl)=
【知识点】 化学反应的速率
五、解答题 添加题型下试题

试回答下列问题:
(1)A的分子式为
(2)丙烯酸乙酯可能发生的反应类型有
①加成反应 ②取代反应 ③加聚反应 ④中和反应
A.①③ B.①②③
C.①③④ D.①②③④
(3)写出聚丙烯酸的结构简式
(4)写出丙烯酸与B反应的化学方程式
(5)下列有关说法正确的是
A.D与丙烯酸乙酯互为同系物
B.B→C的转化是氧化反应
C.可以用酸性KMnO4溶液鉴别A和丙烯酸
D.蒸馏能分离B和C的混合物

(1)实验室如果用②装置制取氨气,写出该反应的化学方程式
(2)气体的性质是选择气体收集方法的主要依据。下列性质与收集方法无关的是
① 密度 ② 颜色 ③ 溶解性 ④ 热稳定性 ⑤ 与氧气反应
(3)若用①装置与④装置相连制取并收集X气体,则X可以是下列气体中的
①CO2 ②NO ③Cl2 ④H2
六、填空题 添加题型下试题
若将9.60g铜跟一定量的浓硝酸反应,铜消耗完时,共产生气体4.48L(标准状况),则被还原的硝酸的物质的量是
【知识点】 氧化还原反应有关计算 硝酸 硝酸的强氧化性解读 铜与强氧化性酸的反应
试卷分析
试卷题型(共 26题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 燃烧热 | |
| 2 | 0.85 | 元素周期表 元素周期律 | |
| 3 | 0.65 | 硫酸根离子的检验 | |
| 4 | 0.64 | 反应热 | |
| 5 | 0.64 | 烃的衍生物 有机物的结构特点 | |
| 7 | 0.64 | 化学用语 | |
| 8 | 0.64 | 原电池 | |
| 9 | 0.64 | 化学平衡 | |
| 10 | 0.64 | 卤素及其化合物 | |
| 11 | 0.85 | 原子的基本构成 原子中相关数值及其之间的相互关系 | |
| 12 | 0.65 | 化学反应速率的定量表示方法 化学反应速率计算 化学反应速率与化学计量数之间的关系 | |
| 13 | 0.64 | 卤素及其化合物 | |
| 14 | 0.65 | 物质性质的探究 | |
| 15 | 0.64 | 化学实验基础 钠及其化合物 | |
| 16 | 0.64 | 分子结构与性质 | |
| 17 | 0.64 | 元素周期表 元素周期律 | |
| 18 | 0.65 | 同分异构体的数目的确定 | |
| 19 | 0.64 | 反应热 | |
| 20 | 0.4 | 氮族元素及其化合物 | |
| 二、未知 | |||
| 6 | 0.64 | 氮族元素及其化合物 | 未知 |
| 三、填空题 | |||
| 21 | 0.85 | 元素周期表 元素周期律 | |
| 22 | 0.85 | 元素周期表 元素周期律 | |
| 23 | 0.85 | 化学反应的速率 | |
| 26 | 0.4 | 氧化还原反应有关计算 硝酸 硝酸的强氧化性 铜与强氧化性酸的反应 | |
| 四、解答题 | |||
| 24 | 0.65 | 乙烯的聚合反应 乙酸的酯化反应 有机物的合成 有机推断综合考查 | 有机推断题 |
| 25 | 0.4 | 化学实验基础 氮族元素及其化合物 | 实验探究题 |



