Q、R、X、Y、Z为短周期主族元素,且原子序数依次递增。Q的低价氧化物与R单质分子的电子总数相等,X与Q同族,Y和Z的离子与Ar原子的电子结构相同。
(1)Q的最高价氧化物中Q的杂化类型为___ ,分子中含有___ 个σ键,___ 个π键。
(2)X的氢化物分子的立体构型是___ ,属于__ 分子(填“极性”或“非极性”);它与R形成的化合物可作为一种重要的陶瓷材料,其化学式是___ 。
(3)Q分别与Y、Z形成的共价化合物的化学式是___ 和___ ;Q与Y形成的分子的电子式是__ ,属于___ 分子(填“极性”或“非极性”)。
(1)Q的最高价氧化物中Q的杂化类型为
(2)X的氢化物分子的立体构型是
(3)Q分别与Y、Z形成的共价化合物的化学式是
更新时间:2020-04-22 08:18:02
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】X、Y、Z、W是四种短周期元素,X原子M层上的电子数是原子核外电子层数的2倍;Y原子最外层电子数是次外层电子数的2倍;Z元素的单质为双原子分子,Z的氢化物水溶液呈碱性;W元素最高正价是+7价。回答下列问题:
(1)元素X原子结构示意图为_______ 。
(2)元素Y的最高价氧化物的电子式为_______ ;Y的最简单氢化物与O2在碱性条件可以形成原电池,该电池负极的电极反应为_______ 。
(3)元素Z在元素周期表中的位置是_______ ,其简单氢化物的沸点比同主族相邻元素的氢化物的沸点_______ (填“低”、“高”或“相等”),其原因为_______ 。
(4)ZW3常温下呈液态,可与水反应生成一种具有漂白性的酸和一种碱性气体,反应的化学方程式为_______ 。
(1)元素X原子结构示意图为
(2)元素Y的最高价氧化物的电子式为
(3)元素Z在元素周期表中的位置是
(4)ZW3常温下呈液态,可与水反应生成一种具有漂白性的酸和一种碱性气体,反应的化学方程式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】X、Y、Z、W为元素周期表前四周期的元素。其中X为形成的化合物中种类最多的元素,Y的内层电子数是最外层电子数的9倍,Z在元素周期表的各元素中电负性最大,W元素的第三电子层处于全充满状态且第四电子层只有2个电子。请回答下列问题.
(1)W元素在元素周期表中的位置为____________________________ 。
(2)比较XZ4和YZ2的熔沸点大小并说明理由________________________ 。
(3)W2+能与氨气分子形成配离子[W(NH3)4]2+。写出该配离子的结构简式(标明配位键)__ 。
(4)X能与氢、氮,氧三种元素构成化合物XO(NH2)2,其中X原子的杂化方式为__ ,1mol分子中σ键的数目为__ ,该物质易溶水的主要原因是_______________________ 。
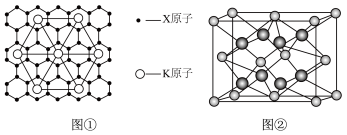
(5)X的某种晶体为层状结构,可与熔融金属钾作用、钾原子填充在各层之间,形成间隙化合物,其常见结构的平面投影如图①所示,则其化学式时表示为_________ 。
(6)元素Y与元素Z形成的晶体结构如图②所示,晶胞中Y离子的配位数为_______ 。

(1)W元素在元素周期表中的位置为
(2)比较XZ4和YZ2的熔沸点大小并说明理由
(3)W2+能与氨气分子形成配离子[W(NH3)4]2+。写出该配离子的结构简式(标明配位键)
(4)X能与氢、氮,氧三种元素构成化合物XO(NH2)2,其中X原子的杂化方式为
(5)X的某种晶体为层状结构,可与熔融金属钾作用、钾原子填充在各层之间,形成间隙化合物,其常见结构的平面投影如图①所示,则其化学式时表示为
(6)元素Y与元素Z形成的晶体结构如图②所示,晶胞中Y离子的配位数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.按要求回答下列问题:
(1)某粒子有1个原子核、核中有17个质子、20个中子,核外有18个电子,该粒子的化学符号是___________ 。
(2)写出下列物质的电子式:
NaOH___________ Cl2 ___________ NH4I ___________ 。
(3)用电子式表示下列化合物的形成过程:
Na2S___________ 。
H2O___________ 。
Ⅱ. 如图为元素周期表的一部分,列出了10种元素在元素周期表中的位置,试回答下列问题:___________ 。(填化学式)。
(5)10种元素中,原子半径最小的是___________ (填序号)。
(6)元素⑦的简单氢化物与元素⑧的单质反应的离子方程式为___________ 。
(7)元素②和⑤的最高价氧化物对应水化物相互反应的化学方程式为___________ 。
(8)元素⑩的原子序数为___________ 。
(9)元素⑨的单质易溶于元素⑥与⑧形成的化合物中,所得溶液颜色为___________ 色。
(1)某粒子有1个原子核、核中有17个质子、20个中子,核外有18个电子,该粒子的化学符号是
(2)写出下列物质的电子式:
NaOH
(3)用电子式表示下列化合物的形成过程:
Na2S
H2O
Ⅱ. 如图为元素周期表的一部分,列出了10种元素在元素周期表中的位置,试回答下列问题:
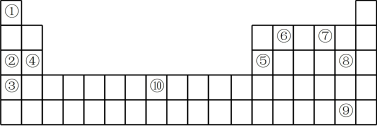
(5)10种元素中,原子半径最小的是
(6)元素⑦的简单氢化物与元素⑧的单质反应的离子方程式为
(7)元素②和⑤的最高价氧化物对应水化物相互反应的化学方程式为
(8)元素⑩的原子序数为
(9)元素⑨的单质易溶于元素⑥与⑧形成的化合物中,所得溶液颜色为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】元素①~⑧在元素周期表中的位置如下,回答有关问题:
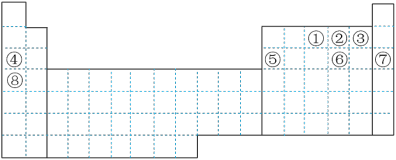
(1)画出⑥的离子结构示意图_______ 。
(2)在②、③、④、⑤四种元素中,其简单离子半径按由大到小的排列顺序为_______ (示例:用r(A2-)>r(B-)的形式表示)。
(3)元素③氢化物分子中的化学键为_______ (填“极性共价键”或“非极性共价键”)。
(4)元素②、③氢化物的稳定性由强到弱的顺序为(填化学式)_______ 。
(5)与③同一主族并且在短周期的元素的某种含氧酸可以消毒杀菌,写出该物质的结构式_______ 。
(6)元素②的氢化物比其同族短周期元素的氢化物的沸点_______ (填“高”或“低”)。

(1)画出⑥的离子结构示意图
(2)在②、③、④、⑤四种元素中,其简单离子半径按由大到小的排列顺序为
(3)元素③氢化物分子中的化学键为
(4)元素②、③氢化物的稳定性由强到弱的顺序为(填化学式)
(5)与③同一主族并且在短周期的元素的某种含氧酸可以消毒杀菌,写出该物质的结构式
(6)元素②的氢化物比其同族短周期元素的氢化物的沸点
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】甲烷干重整反应可以同时转化CH4和CO2两种温室气体,并制备高附加值的合成气(H2和CO混合气体)。
(1)已知转化2mol CH4吸收386.6kJ热量,则可逆反应甲烷干重整的热化学方程式为____ ,反应物总键能____ 生成物总键能(填“大于”“小于”或“等于”)。
(2)T℃、压强为p时,以n(CH4):n(CO2):n(Ar)=1:1:3的投料比,在密闭容器中发生甲烷干重整反应,主要副反应为CO2(g)+H2(g) CO(g)+H2O(g)。
CO(g)+H2O(g)。
①反应体系中加入Ar的作用是____ 。
②CH4和CO2的平衡转化率分别是60%和80%,则H2的产率为____ ,T℃下副反应的平衡常数K=____ 。
(3)北京大学徐东升教授团队开发了一种甲烷干重整光催化剂—Rh/CexWO3,光诱导过程机理如图(Vo表示氧空位)。光照时,光催化剂产生电子(e-)和空穴(h+),驱动反应进行,下列叙述错误的是_____ 。

(4)碱性甲烷燃料电池中,负极的电极反应式为_____ 。
(1)已知转化2mol CH4吸收386.6kJ热量,则可逆反应甲烷干重整的热化学方程式为
(2)T℃、压强为p时,以n(CH4):n(CO2):n(Ar)=1:1:3的投料比,在密闭容器中发生甲烷干重整反应,主要副反应为CO2(g)+H2(g)
 CO(g)+H2O(g)。
CO(g)+H2O(g)。①反应体系中加入Ar的作用是
②CH4和CO2的平衡转化率分别是60%和80%,则H2的产率为
(3)北京大学徐东升教授团队开发了一种甲烷干重整光催化剂—Rh/CexWO3,光诱导过程机理如图(Vo表示氧空位)。光照时,光催化剂产生电子(e-)和空穴(h+),驱动反应进行,下列叙述错误的是

| A.反应过程中有非极性键的断裂和形成 |
| B.e-从Ce原子转移到W,进而转移到吸附在氧空位的CO2分子上 |
| C.h+和Rh附近的晶格氧结合,促进沉积在Rh上的C快速被消耗移除 |
| D.CO2解离后在氧空位留下氧原子,一段时间后催化剂含氧量增加 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】利用工业废铁粉(主要成为Fe3O4、Fe)与硫酸反应可制备硫酸盐。
(1)Fe2+基态核外电子排布式为________ 。
(2)FeSO4隔绝空气受热分解生成SO2、SO3、Fe2O3。SO2分子的空间构型为__________ ,其中S原子的杂化类型为________ 。与SO3互为等电子体的离子与分子分别为________ 、________ (填化学式)。
(3)苯酚可以与Fe3+发生显色反应。1 mol苯酚中含有σ键的数目为________ 。
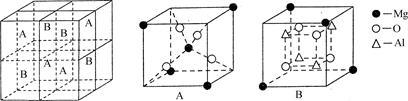
(4)Fe3O4具有反尖晶石结构。某化合物MgxAlyOz与反尖晶石结构相仿,其结构如下图所示,它是由下列A、B方块组成。该化合物的化学式为________ 。
(1)Fe2+基态核外电子排布式为
(2)FeSO4隔绝空气受热分解生成SO2、SO3、Fe2O3。SO2分子的空间构型为
(3)苯酚可以与Fe3+发生显色反应。1 mol苯酚中含有σ键的数目为
(4)Fe3O4具有反尖晶石结构。某化合物MgxAlyOz与反尖晶石结构相仿,其结构如下图所示,它是由下列A、B方块组成。该化合物的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】K4[Fe(CN)6]强热可发生反应:3K4[Fe(CN)6] (CN)2↑+12KCN+N2↑+Fe3C+C
(CN)2↑+12KCN+N2↑+Fe3C+C
(1)基态铁原子价层电子排布式为____________ ,组成K4[Fe(CN)6]的几种元素第一电离能由大到小的顺序为___________ ,K4[Fe(CN)6]中配离子组成为___________ 。
(2)(CN)2分子中各原子均达到稳定的电子层结构,则碳原子杂化轨道类型为___________ ,分子中含有σ键与π键数目比为___________ ,分子构型为_____________ 。
(3)KCN沸点1497℃,熔点563℃,则其晶体类型为___________ ,与NaCN相比,熔点较高的物质是___________ 。
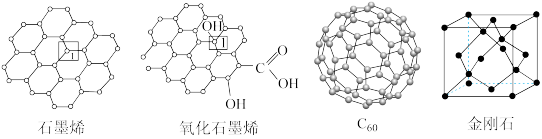
(4)碳可形成多种单质,下图是碳的三种单质与氧化石墨烯的结构示意图。
①若将10nm石墨烯与氧化石墨烯粒子在相同条件下分散到水中,所得到的分散系中,后者的稳定性强于前者,可能的原因是___________ 。
②1mol石墨烯含有的6元环有___________ NA,上述四种物质中,___________ 的化学性质明显不同于另外几种物质。
 (CN)2↑+12KCN+N2↑+Fe3C+C
(CN)2↑+12KCN+N2↑+Fe3C+C(1)基态铁原子价层电子排布式为
(2)(CN)2分子中各原子均达到稳定的电子层结构,则碳原子杂化轨道类型为
(3)KCN沸点1497℃,熔点563℃,则其晶体类型为
(4)碳可形成多种单质,下图是碳的三种单质与氧化石墨烯的结构示意图。

①若将10nm石墨烯与氧化石墨烯粒子在相同条件下分散到水中,所得到的分散系中,后者的稳定性强于前者,可能的原因是
②1mol石墨烯含有的6元环有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E代表前四周期原子序数依次增大的五种元素。A、D同主族且有两种常见化合物DA2和DA3;工业上电解熔融C2A3制取单质C, B、E除最外层均只有2个电子外,其余各层全充满,E位于元素周期表的ds区。回答下列问题:
(1)B、C中第一电离能较大的是___________ 。
(2) H2A比H2D熔沸点高得多的原因是___________ 。
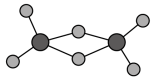
(3)实验测得C与氯元素形成化合物的实际组成为C2Cl6,其球棍模型如图所示。已知C2Cl6在加热时易升华,与过量的NaOH 溶液反应可生成Na[C(OH)4]
①C2Cl6属于___________ 晶体(填晶体类型),其中C原子的杂化轨道类型为___________ 杂化。
②[C(OH)4]-中存在的化学键有___________ 。
(4)B的氯化物、C的氟化物晶格能分别是2957KJ/mol、5492KJ/mol,二者相差很大的原因是___________ 。
(5)D与E所形成化合物晶体的晶胞如图所示。

①原子坐标参数可表示晶胞内部各原子的相对位置。如图晶胞中,原子坐标参数a为(0,0,0);b为(1/2,0,1/2),c为(1/2,1/2,0)。则d原子的坐标为___________ 。
②已知该晶胞的密度为ρg/cm3,则其中两个D,原子之间的距离为___________ pm(列出计算式即可)。
(1)B、C中第一电离能较大的是
(2) H2A比H2D熔沸点高得多的原因是
(3)实验测得C与氯元素形成化合物的实际组成为C2Cl6,其球棍模型如图所示。已知C2Cl6在加热时易升华,与过量的NaOH 溶液反应可生成Na[C(OH)4]

①C2Cl6属于
②[C(OH)4]-中存在的化学键有
(4)B的氯化物、C的氟化物晶格能分别是2957KJ/mol、5492KJ/mol,二者相差很大的原因是
(5)D与E所形成化合物晶体的晶胞如图所示。

①原子坐标参数可表示晶胞内部各原子的相对位置。如图晶胞中,原子坐标参数a为(0,0,0);b为(1/2,0,1/2),c为(1/2,1/2,0)。则d原子的坐标为
②已知该晶胞的密度为ρg/cm3,则其中两个D,原子之间的距离为
您最近一年使用:0次
【推荐3】I.氢能的存储是氢能应用的主要瓶颈,配位氢化物、富氢载体化合韧是目前所采用的主要储氢材料。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。在基态Ti2+中,电子占据的最高能层符号为_______ ,该能层具有的原子轨道数为_____ ;
(2)液氨是富氢物质,是氢能的理想载体,利用 实现储氢和输氢。下列说法正确的是
实现储氢和输氢。下列说法正确的是________ ;
a.NH3分子中氮原子的轨道杂化方式为sp2杂化
b.NH4+与PH4+、CH4、BH4-、ClO4-互为等电子体
c.相同压强时,NH3的沸点比PH3的沸点高
d.[Cu(NH3)4]2+离子中,N原子是配位原子
(3)已知NF3与NH3的空间构型相同,但NF3不易与Cu2+形成配离子,其原因是________ ;
II.氯化钠是生活中的常用调味品,也是结构化学中研究离子晶体时常用的代表物,其晶胞结构如图所示。
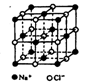
(1)设氯化钠晶体中Na+与跟它最近邻的Cl-之间的距离为r,则该Na+与跟它次近邻的C1-个数为______ ,该Na+与跟它次近邻的Cl—之间的距离为_____ ;
(2)已知在氯化钠晶体中Na+的半径为以a pm,Cl-的半径为b pm,它们在晶
体中是紧密接触的,则在氯化钠晶体中离子的空间利用率为_____ ;(用含a、b的式子袁示)
(3)纳米材料的表面原子占总原子数的比例很大,这是它有许多特殊性质的原因。假设某氯化钠颗粒形状为立方体,边长为氯化钠晶胞的10倍,则该氯化钠颗粒中表面原子占总原子数的百分比为________________ 。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。在基态Ti2+中,电子占据的最高能层符号为
(2)液氨是富氢物质,是氢能的理想载体,利用
 实现储氢和输氢。下列说法正确的是
实现储氢和输氢。下列说法正确的是a.NH3分子中氮原子的轨道杂化方式为sp2杂化
b.NH4+与PH4+、CH4、BH4-、ClO4-互为等电子体
c.相同压强时,NH3的沸点比PH3的沸点高
d.[Cu(NH3)4]2+离子中,N原子是配位原子
(3)已知NF3与NH3的空间构型相同,但NF3不易与Cu2+形成配离子,其原因是
II.氯化钠是生活中的常用调味品,也是结构化学中研究离子晶体时常用的代表物,其晶胞结构如图所示。

(1)设氯化钠晶体中Na+与跟它最近邻的Cl-之间的距离为r,则该Na+与跟它次近邻的C1-个数为
(2)已知在氯化钠晶体中Na+的半径为以a pm,Cl-的半径为b pm,它们在晶
体中是紧密接触的,则在氯化钠晶体中离子的空间利用率为
(3)纳米材料的表面原子占总原子数的比例很大,这是它有许多特殊性质的原因。假设某氯化钠颗粒形状为立方体,边长为氯化钠晶胞的10倍,则该氯化钠颗粒中表面原子占总原子数的百分比为
您最近一年使用:0次
【推荐1】已知和碳元素同主族的X元素位于元素周期表中的第一个长周期,短周期元素Y原子的最外层电子数比内层电子总数少3,它们形成的化合物分子式是XY4试回答:
(1)Y元素的基态原子的核外电子排布式为_______ ,X元素原子价层电子轨道表示式为_______ 。
(2)若X、Y两元素电负性分别为1.8和3.0,则XY4中X与Y之间的化学键为_______ 。(填“共价键”或“离子键”)
(3)该化合物的空间结构为_______ 形,分子为_______ 。(填“极性分子”或“非极性分子”)
(4)该化合物的沸点与SiCl4比较_______ (填化学式)的高。
(5)X元素与C(碳)元素分别形成的简单氢化物稳定性_______ (填化学式)更稳定。
(6)C(碳)元素与H(氢)元素形成的常见有机溶剂中C(碳)原子的轨道杂化方式为_______ 。
(7)有两种元素与Y同一周期,其中一种元素有3个成单电子,另一种元素位于ⅥA族,则三种元素第一电离能由大到小顺序_______ 。(用元素符号表示)
(8)与X元素同周期且成单电子最多的元素在周期表中的位置_______ 。
(1)Y元素的基态原子的核外电子排布式为
(2)若X、Y两元素电负性分别为1.8和3.0,则XY4中X与Y之间的化学键为
(3)该化合物的空间结构为
(4)该化合物的沸点与SiCl4比较
(5)X元素与C(碳)元素分别形成的简单氢化物稳定性
(6)C(碳)元素与H(氢)元素形成的常见有机溶剂中C(碳)原子的轨道杂化方式为
(7)有两种元素与Y同一周期,其中一种元素有3个成单电子,另一种元素位于ⅥA族,则三种元素第一电离能由大到小顺序
(8)与X元素同周期且成单电子最多的元素在周期表中的位置
您最近一年使用:0次
【推荐2】锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因:______ 。
(2)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。CO2和CH4都属于______ 分子(填极性或非极性)。
(3)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为_____ ,微粒之间存在的作用力是_____ 。
(4)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置。如图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为( ,0,
,0, );C为(
);C为( ,
, ,0)。则D原子的坐标参数为
,0)。则D原子的坐标参数为_______ 。______ g·cm-3(列出计算式即可)。
(1)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因:
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/℃ | -49.5 | 26 | 146 |
| 沸点/℃ | 83.1 | 186 | 约400 |
(3)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为
(4)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置。如图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(
 ,0,
,0, );C为(
);C为( ,
, ,0)。则D原子的坐标参数为
,0)。则D原子的坐标参数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D为原子序数依次增大的非金属短周期主族元素,其中A的某种单质是重要的半导体材料。请回答下列问题:
(1)A在元素周期表中的位置为___________ 。
(2)B元素的最高价氧化物的分子式为___________ 。高速通信离不开光导纤维,用于制造光导纤维的基本原料是___________ (填化学式)。
(3)从原子结构角度解释D的非金属性大于C的原因:___________ 。
(4)化合物C2D2在合成橡胶、硬水软化等方面有着重要应用。C2D2分子的结构式为___________ 该分子属于___________ 分子(填“极性”或“非极性”)。
(5)化合物M是制备晶体A的中间产物,它是由A、D和氢三种元素按原子个数比1:3:l组成的。M极易水解,其完全水解的产物除了A的最高价含氧酸外,还有两种气体,这两种气体是___________ (填化学式)。
(1)A在元素周期表中的位置为
(2)B元素的最高价氧化物的分子式为
(3)从原子结构角度解释D的非金属性大于C的原因:
(4)化合物C2D2在合成橡胶、硬水软化等方面有着重要应用。C2D2分子的结构式为
(5)化合物M是制备晶体A的中间产物,它是由A、D和氢三种元素按原子个数比1:3:l组成的。M极易水解,其完全水解的产物除了A的最高价含氧酸外,还有两种气体,这两种气体是
您最近一年使用:0次



