标号为①~⑩的元素,在元素周期表中的位置如下:
试回答下列问题:
(1)写出元素③的名称__ 。
(2)①和④号元素形成的化合物的化学式为__ ,用电子式表示其形成过程为__ 。
(3)⑦和⑧号元素的最高价氧化物的水化物的碱性是:__ ﹥__ (填化学式)。⑨和⑩号元素的最高价氧化物的水化物的酸性是:__ ﹥__ (填化学式)。
(4)①、⑤、⑦号元素形成的一种化合物的电子式是__ ,在该化合物中既含有__ 键,又含有__ 键。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 1 | ① | ② | ||||||
| 2 | ③ | ④ | ⑤ | ⑥ | ||||
| 3 | ⑦ | ⑧ | ⑨ | ⑩ |
(1)写出元素③的名称
(2)①和④号元素形成的化合物的化学式为
(3)⑦和⑧号元素的最高价氧化物的水化物的碱性是:
(4)①、⑤、⑦号元素形成的一种化合物的电子式是
更新时间:2020-04-27 15:40:06
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D、E、F是元素周期表前四周期的六种常见元素,原子序数依次增大。根据表中的相关信息作出合理推断并完成以下问题:
(1)B的原子结构示意图为_______ 。C、D、E三种简单离子的半径由大到小顺序是_______ (填离子符号)。
(2)以上元素分别与氢元素组成含 电子的分子
电子的分子_______ (任写2种),C与D的单质在点燃条件下反应产物含有的化学键是_______
(3)A、B、E的最高价氧化物的水化物酸性从强到弱的顺序是_______ (填化学式)。
(4)F的单质与C的最简单氢化物在一定条件下反应的化学方程式为_______ 。
(5)B的一种氢化物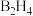 常用作火箭推进剂的燃料,
常用作火箭推进剂的燃料,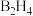 与B的氧化物
与B的氧化物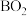 反应生成对环境友好的产物,该反应的化学方程式为
反应生成对环境友好的产物,该反应的化学方程式为_______ 。
| 元素 | 性质 |
| A | A自然界中有多种同素异形体,其中一种是自然界中最硬的单质 |
| B | 单质是空气中的主要成分 |
| C | 地壳中含量最多的元素 |
| D | 第三周期元素中原子半径最大 |
| E | 原子最外层电子数是A、C原子核外电子数之和的一半 |
| F | 常见的金属元素,可形成多种氧化物,其中一种氧化物常用作红色颜料 |
(2)以上元素分别与氢元素组成含
 电子的分子
电子的分子(3)A、B、E的最高价氧化物的水化物酸性从强到弱的顺序是
(4)F的单质与C的最简单氢化物在一定条件下反应的化学方程式为
(5)B的一种氢化物
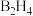 常用作火箭推进剂的燃料,
常用作火箭推进剂的燃料,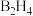 与B的氧化物
与B的氧化物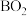 反应生成对环境友好的产物,该反应的化学方程式为
反应生成对环境友好的产物,该反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】如图为元素周期表的一部分,请参照元素①~⑨在图中的位置,回答下列问题。
(1)第三周期元素中非金属性最强的元素的原子结构示意图是_________ 。
(2)①~⑨号元素中,原子半径最大的是:_________ (填元素符号),⑧和⑨的离子半径相比较小的是:_________ (填离子符号);
(3)下列可以判断⑤和⑥金属性强弱的是_________ (填序号)。
a.单质的熔点:⑤<⑥
b.化合价:⑤<⑥
c.单质与水反应的剧烈程度:⑤>⑥
d.最高价氧化物对应水化物的碱性:⑤>⑥
(4)元素⑤和元素⑥各自的最高价氧化物对应水化物相互反应的离子方程式为:_________ 。
(5)为验证第ⅦA族部分元素非金属性的递变规律,设计如图装置进行实验,请回答:
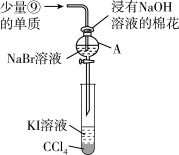
①仪器A的名称是_________ ,A中发生反应的离子方程式是_________ 。
②棉花中浸有 溶液的作用是
溶液的作用是_________ (用离子方程式表示)。
③验证溴与碘的非金属性强弱:通入少量⑨的单质,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到溶液分层,下层液体为紫红色。该实验必须控制⑨单质的加入量,否则得不出溴的非金属性比碘强的结论,理由是_________ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(2)①~⑨号元素中,原子半径最大的是:
(3)下列可以判断⑤和⑥金属性强弱的是
a.单质的熔点:⑤<⑥
b.化合价:⑤<⑥
c.单质与水反应的剧烈程度:⑤>⑥
d.最高价氧化物对应水化物的碱性:⑤>⑥
(4)元素⑤和元素⑥各自的最高价氧化物对应水化物相互反应的离子方程式为:
(5)为验证第ⅦA族部分元素非金属性的递变规律,设计如图装置进行实验,请回答:

①仪器A的名称是
②棉花中浸有
 溶液的作用是
溶液的作用是③验证溴与碘的非金属性强弱:通入少量⑨的单质,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到溶液分层,下层液体为紫红色。该实验必须控制⑨单质的加入量,否则得不出溴的非金属性比碘强的结论,理由是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】现有核电荷数均不超过18的A、B、C、D四种元素,A是一种金属元素,其原子的核外有三个电子层,能形成氧化物AO,B元素的二价阴离子与C元素原子核外的电子层结构相同,都是M层为最外层且有8个电子,D元素可形成D+且D+只有一个质子
(1)写出元素符号:A_______ ,B_______ ,C_______ ,D_______ 。
(2)上述4种元素中的某种元素能自相形成双原子分子,则该双原子分子的化学式为_______ 。
(3)A元素形成的简单离子的结构示意图为_______ 。
(4)B的简单阴离子的电子式为_______ 。
(1)写出元素符号:A
(2)上述4种元素中的某种元素能自相形成双原子分子,则该双原子分子的化学式为
(3)A元素形成的简单离子的结构示意图为
(4)B的简单阴离子的电子式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】用图表来处理数据是发现科学规律的一种重要方法。
(1)下图是原子序数为1~18的元素原子的最外层电子数随原子序数变化的直方图。图中元素a 是__ ,b 是____ 。

(2)下图表示元素的一种性质随原子序数变化的情况,根据分析,该图纵坐标表示的是_________ 。

(3)下表给出了部分元素的原子半径。
请根据表中数据分析同周期元素原子半径的递变规律是______ ,同主族元素原子半径的递变规律是_____ 根据表中得出的规律比较Ca2+和Cl-的半径大小:r(Ca2+)_____ r(Cl-)(填“>”“<”或“=”)。
(1)下图是原子序数为1~18的元素原子的最外层电子数随原子序数变化的直方图。图中元素a 是

(2)下图表示元素的一种性质随原子序数变化的情况,根据分析,该图纵坐标表示的是

(3)下表给出了部分元素的原子半径。
| 元素符号 | Li | Be | B | C | N | O | F | Na | K | Rb | Cs |
| 原子半径/nm | 0.152 | 0.089 | 0.082 | 0.077 | 0.075 | 0.074 | 0.071 | 0.186 | 0.227 | 0.248 | 0.265 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】用 生产含氯有机物时会产生HCl。利用反应:
生产含氯有机物时会产生HCl。利用反应: 可实现氯的循环利用。完成下列填空:
可实现氯的循环利用。完成下列填空:
(1)上述反应中所有元素原子半径由大到小的顺序为___________ 。与氯元素同族的短周期元素原子最外层电子的轨道表示式为___________ 。
(2)判断氯、溴非金属性强弱的依据是___________ (选填序号)。
a.熔点:Cl2<Br2 b.氧化性:Cl2>Br2
c.热稳定性:HCl>HBr d.酸性:HCl<HBr
(3)若反应在固定体积的密闭容器中发生,能说明反应已达平衡的是___________ (选填序号)。
a.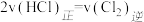 b.体系压强不再改变
b.体系压强不再改变
c.混合气体密度不变 d.
(4)若反应容器容积为2L,4molHCl与1mol 混合气体反应至8min时,恢复至原来温度,测得容器内气体压强减小了10%,则用HCl表示该反应的化学反应速率为
混合气体反应至8min时,恢复至原来温度,测得容器内气体压强减小了10%,则用HCl表示该反应的化学反应速率为___________ 。
(5)如下图是在2种不同投料比[ =1,6 ]下,温度对HCl平衡转化率影响的曲线。
=1,6 ]下,温度对HCl平衡转化率影响的曲线。

①曲线a对应的投料比 =
=___________ 。
②使曲线a达到曲线b相同的HCl平衡转化率,不改变投料比,可采取的措施有___________ ;___________ 。
 生产含氯有机物时会产生HCl。利用反应:
生产含氯有机物时会产生HCl。利用反应: 可实现氯的循环利用。完成下列填空:
可实现氯的循环利用。完成下列填空:(1)上述反应中所有元素原子半径由大到小的顺序为
(2)判断氯、溴非金属性强弱的依据是
a.熔点:Cl2<Br2 b.氧化性:Cl2>Br2
c.热稳定性:HCl>HBr d.酸性:HCl<HBr
(3)若反应在固定体积的密闭容器中发生,能说明反应已达平衡的是
a.
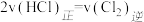 b.体系压强不再改变
b.体系压强不再改变c.混合气体密度不变 d.

(4)若反应容器容积为2L,4molHCl与1mol
 混合气体反应至8min时,恢复至原来温度,测得容器内气体压强减小了10%,则用HCl表示该反应的化学反应速率为
混合气体反应至8min时,恢复至原来温度,测得容器内气体压强减小了10%,则用HCl表示该反应的化学反应速率为(5)如下图是在2种不同投料比[
 =1,6 ]下,温度对HCl平衡转化率影响的曲线。
=1,6 ]下,温度对HCl平衡转化率影响的曲线。
①曲线a对应的投料比
 =
=②使曲线a达到曲线b相同的HCl平衡转化率,不改变投料比,可采取的措施有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某研究性学习小组的甲、乙同学分别设计了以下实验来验证元素周期律。
I.甲同学验证同一周期从左到右元素的金属性强弱。实验药品有小块钠,表面积相同的镁、铝,稀盐酸,蒸馏水。
(1)请填写实验操作。
Ⅱ.乙同学利用如图所示装置可以验证非金属性的变化规律,实验室中药品有Na2S溶液、KMnO4、浓盐酸、MnO2。

(2)干燥管D的作用是___________ 设计实验来验证氯的非金属性强于硫,装置A、B、C中所装药品分别为___________ 、___________ 、___________ ,装置C中的实验现象为___________ 。
(3)用上述装置证明非金属性:S>C>Si,则装置A、B、C中所装药品分别为___________ 、___________ 、___________ 。
I.甲同学验证同一周期从左到右元素的金属性强弱。实验药品有小块钠,表面积相同的镁、铝,稀盐酸,蒸馏水。
(1)请填写实验操作。
| 实验目的 | 实验操作 | 实验结论 |
| 比较钠、镁金属性强弱 | Na>Mg | |
| 比较镁、铝金属性强弱 | Mg>A1 |
Ⅱ.乙同学利用如图所示装置可以验证非金属性的变化规律,实验室中药品有Na2S溶液、KMnO4、浓盐酸、MnO2。

(2)干燥管D的作用是
(3)用上述装置证明非金属性:S>C>Si,则装置A、B、C中所装药品分别为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】有A、B、C、D、E五种短周期主族元素,它们的原子序数依次增大,已知A的L层电子数是K层电子数的两倍,D是短周期元素中原子半径最大的元素,D的单质在高温下与C的单质充分反应,可以得到与E单质颜色相同的淡黄色固态化合物,试根据以上叙述回答:
(1)元素名称:A____________ ; B_____________ ;
(2)元素E在周期表中的位置_________________________ ;
(3)元素C与D可以形成两种不同的化合物,用电子式表示D2C的形成过程_____ D2C2的化学键类型为_____________________ (填“离子键”“非极性共价键”或“极性共价键”)。
(4)AC2的结构式为______________ ,写出 与
与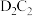 反应的化学方程式
反应的化学方程式_____________
(1)元素名称:A
(2)元素E在周期表中的位置
(3)元素C与D可以形成两种不同的化合物,用电子式表示D2C的形成过程
(4)AC2的结构式为
 与
与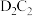 反应的化学方程式
反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D、E五种短周期主族元素,原子序数依次增大,A原子的最外层上有4个电子;C的阴离子和D的阳离子具有相同的电子层结构,两种元素的单质反应,可生成一种淡黄色的固体F,E的L层电子数等于K、M层电子数之和。
(1)B位于第__________ 周期第__________ 族,C常见单质的电子式为________ 。
(2)B、C、D、E元素的简单离子半径由小到大的顺序为__________________________ (用离子符号表示)。
(3)C的一种氢化物分子中含有18个电子,其结构式为____________ 。
(4)已知A、E两种元素形成的化合物H,H结构与干冰相似,属于______________ (填“离子”或“共价”)化合物。7.6 g的H中含有的共用电子对数目为________ 。
(5)E的最高价氧化物对应的水化物的浓溶液和A的单质加热发生反应的化学方程式为___________ 。
(1)B位于第
(2)B、C、D、E元素的简单离子半径由小到大的顺序为
(3)C的一种氢化物分子中含有18个电子,其结构式为
(4)已知A、E两种元素形成的化合物H,H结构与干冰相似,属于
(5)E的最高价氧化物对应的水化物的浓溶液和A的单质加热发生反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】A、B、C、D为四种短周期元素,它们的原子序数依次增大,其中A与C、B与D分别是同主族元素;已知B、D两元素间可形成DB2和DB3两种化合物,两者相对分子质量相差16;又知A、C两元素原子序数之和是B、D两元素原子序数之和的 ,请回答下列问题:
,请回答下列问题:
(1)写出由A、B、C三种元素形成的化合物的电子式:__________________________ ,其晶体中所含化学键的类型有________________________________________________________ 。
(2)A2B的沸点比A2D的沸点(填“高”或“低”)________ ;其原因是_________________ 。
(3)由A、B、C、D四种元素形成的物质X,与盐酸反应能够生成具有刺激性气味的气体,写出X与盐酸反应的离子方程式:___________________________________________________ 。
 ,请回答下列问题:
,请回答下列问题:(1)写出由A、B、C三种元素形成的化合物的电子式:
(2)A2B的沸点比A2D的沸点(填“高”或“低”)
(3)由A、B、C、D四种元素形成的物质X,与盐酸反应能够生成具有刺激性气味的气体,写出X与盐酸反应的离子方程式:
您最近一年使用:0次



