现有X、Y、Z三种非金属元素,A、B、C三种金属元素,有:
①X、Y、Z的单质在常温下均为气体;
②X的单质在Z的单质中燃烧,火焰呈苍白色。产物XZ的水溶液可使石蕊试液变红;
③2molX的单质可与1molY的单质化合生成2molX2Y,X2Y在常温下为液体;
④Z的单质溶于X2Y中所得的溶液具有漂白性;
⑤A的单质可以在Z的单质中燃烧,生成黑棕色固体,该固体溶于水得到棕黄色溶液;
⑥B与Z可形成化合物BZ3,向BZ3的溶液中逐滴滴加NaOH溶液,先生成白色沉淀后沉淀逐渐溶解;
⑦C的单质与Y的单质反应可能得到两种产物,其中一种为淡黄色固体M
请回答下列问题:
(1)写出下列物质的化学式:XZ__________ ,X2Y__________ ,M__________
(2)Z的单质溶于X2Y中所得溶液中起漂白作用的物质是__________ (填化学式)
(3)A的单质与Z的单质反应的化学方程式为__________
(4)BZ3与过量的NaOH溶液反应的离子方程式为__________
(5)X的单质与Z的单质的混合气体经点燃充分反应后,冷却至室温,再通入足量的NaOH溶液中,气体被完全吸收,则原混合气体中X的单质与Z的单质的体积关系可能为__________ (用相应化学式表示X、Z的单质)
①X、Y、Z的单质在常温下均为气体;
②X的单质在Z的单质中燃烧,火焰呈苍白色。产物XZ的水溶液可使石蕊试液变红;
③2molX的单质可与1molY的单质化合生成2molX2Y,X2Y在常温下为液体;
④Z的单质溶于X2Y中所得的溶液具有漂白性;
⑤A的单质可以在Z的单质中燃烧,生成黑棕色固体,该固体溶于水得到棕黄色溶液;
⑥B与Z可形成化合物BZ3,向BZ3的溶液中逐滴滴加NaOH溶液,先生成白色沉淀后沉淀逐渐溶解;
⑦C的单质与Y的单质反应可能得到两种产物,其中一种为淡黄色固体M
请回答下列问题:
(1)写出下列物质的化学式:XZ
(2)Z的单质溶于X2Y中所得溶液中起漂白作用的物质是
(3)A的单质与Z的单质反应的化学方程式为
(4)BZ3与过量的NaOH溶液反应的离子方程式为
(5)X的单质与Z的单质的混合气体经点燃充分反应后,冷却至室温,再通入足量的NaOH溶液中,气体被完全吸收,则原混合气体中X的单质与Z的单质的体积关系可能为
更新时间:2020-04-29 10:40:03
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】某研究性学习小组欲探究氯气的化学性质,设计如图所示的实验装置。
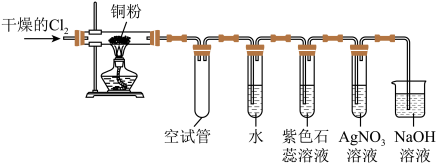
已知:该装置气密性良好;铜粉放在耐高温托盘内(防止硬质玻璃管炸裂)。
请回答下列问题:
(1)为防止铜与空气中的氧气反应,在加热之前应该进行的操作为____ 。
(2)当观察到AgNO3溶液中出现白色沉淀时,点燃酒精灯加热;写出AgNO3溶液中发生反应的化学方程式:____ 。
(3)硬质玻璃管中的反应现象为____ ,反应的化学方程式为____ 。
(4)装置中空试管的作用是____ 。
(5)实验中,观察到紫色石蕊溶液颜色的变化为____ 。
(6)烧杯中氢氧化钠溶液的作用是___ ,发生反应的化学方程式为_____ 。
(7)盛水的试管中,溶液最后的颜色为___ ,说明氯气____ (填“能”或“不能”)溶于水。

已知:该装置气密性良好;铜粉放在耐高温托盘内(防止硬质玻璃管炸裂)。
请回答下列问题:
(1)为防止铜与空气中的氧气反应,在加热之前应该进行的操作为
(2)当观察到AgNO3溶液中出现白色沉淀时,点燃酒精灯加热;写出AgNO3溶液中发生反应的化学方程式:
(3)硬质玻璃管中的反应现象为
(4)装置中空试管的作用是
(5)实验中,观察到紫色石蕊溶液颜色的变化为
(6)烧杯中氢氧化钠溶液的作用是
(7)盛水的试管中,溶液最后的颜色为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】某实验小组进行物质漂白性的实验探究:
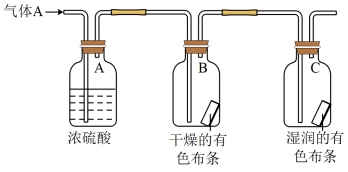
应用如图所示的方法实验,其中气体A的主要成分是氯气,杂质是空气和水蒸气。回答下列问题:
(1)该项研究(实验)的主要目的是___________ 。
(2)浓硫酸的作用是___________ ,与研究目的直接相关的实验现象是___________ 。
(3)将石蕊试液滴到新制氯水中的现象___________ 。
(4)从物质的性质方面看,这套设计还存在隐患,表现为___________ ,该步处理所用试剂为___________ 。

应用如图所示的方法实验,其中气体A的主要成分是氯气,杂质是空气和水蒸气。回答下列问题:
(1)该项研究(实验)的主要目的是
(2)浓硫酸的作用是
(3)将石蕊试液滴到新制氯水中的现象
(4)从物质的性质方面看,这套设计还存在隐患,表现为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】如图所示,将仪器A中的浓盐酸滴加到盛有MnO2的烧瓶中,加热后产生的气体依次通过装置B和C,然后再通过加热的石英玻璃管D(放置有铁粉)。请回答:
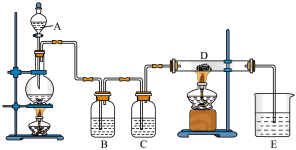
(1)仪器A的名称是____ ,烧瓶中反应的化学方程式是____ 。其中盐酸具有___ (填序号)
①氧化性 ②还原性 ③酸性
(2)装置B中盛放液体是___ ,气体通过装置B的目的是___ 。装置C中盛放的液体是___ 。
(3)D中反应的化学方程式是____ 。
(4)烧杯E中盛放的液体是___ ,作用是___ ,反应的离子方程式是___ 。
(5)资料表明D中产物有以下性质:①受热易升华,冷却后易凝华;②遇H2O(g)剧烈反应。为收集D中产物,在D与E之间,除增加收集装置外,还需要增加___ 装置

(1)仪器A的名称是
①氧化性 ②还原性 ③酸性
(2)装置B中盛放液体是
(3)D中反应的化学方程式是
(4)烧杯E中盛放的液体是
(5)资料表明D中产物有以下性质:①受热易升华,冷却后易凝华;②遇H2O(g)剧烈反应。为收集D中产物,在D与E之间,除增加收集装置外,还需要增加
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】现有A、B、C、D四种气体,A是密度最小的气体;B呈黄绿色;A可以在B中安静地燃烧,发出苍白色的火焰并生成D;把无色无刺激性气味的C气体通入澄清石灰水中,澄清石灰水变浑浊。
(1)A、C的化学式分别为______________ 、___________ 。
(2)写出下列各反应的化学方程式:A与B反应:_______ ,B与水反应:_______ 。
(1)A、C的化学式分别为
(2)写出下列各反应的化学方程式:A与B反应:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】A~E为中学化学常见纯净物,其中A可用于焙制糕点,B是生活中常用的一种调味品,也是重要的化工原料。D、E均为气体,F的水溶液是一种强酸。它们之间的转化关系如下。(部分反应物、生成物已略去)

请回答下列问题:
(1)写出下列物质的化学式:A________ ,B_________ ,C________ 。
(2)A→B的离子方程式是________ 。
(3)D与E反应的化学方程式是________ ,反应现象是________ 。

请回答下列问题:
(1)写出下列物质的化学式:A
(2)A→B的离子方程式是
(3)D与E反应的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】常温下,A是可用来对自来水进行消毒的黄绿色单质气体,A、B、C、D、E都含X元素,其转化关系如图所示:
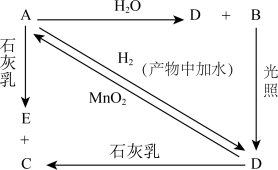
(1)请分别写出下列物质的化学式(如为溶液请填溶质的化学式):
A________ 、B________ 、D________ 。
(2)写出下列反应的化学方程式或离子方程式(请注明反应条件):
A+H2O(离子方程式):_____________ ;
A+石灰乳(化学方程式):______________ ;
E露置在空气中的第1个化学方程式:___________ 。
(3)漂白粉的有效成分是________ (化学名称),保存漂白粉的方法__________ 、______________ 。

(1)请分别写出下列物质的化学式(如为溶液请填溶质的化学式):
A
(2)写出下列反应的化学方程式或离子方程式(请注明反应条件):
A+H2O(离子方程式):
A+石灰乳(化学方程式):
E露置在空气中的第1个化学方程式:
(3)漂白粉的有效成分是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】已知以下物质为铁及其化合物之间的相互转化:
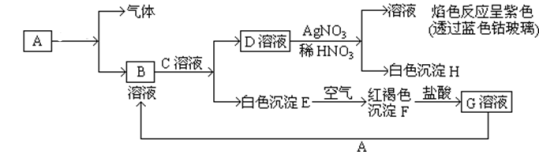
试回答:
(1)写出D的化学式___ ,H的化学式___ 。
(2)鉴别G溶液的试剂为___ 。
(3)写出由E转变成F的化学方程式___ 。

试回答:
(1)写出D的化学式
(2)鉴别G溶液的试剂为
(3)写出由E转变成F的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】金属A能够被磁铁所吸引,A及其A的化合物之间有如图的转化关系:
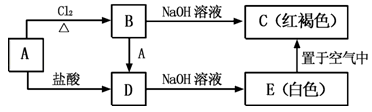
(1)写出A、C的化学式:A__ ;C___ 。
(2)检验B中阳离子的试剂是___ ,现象是__ 。
(3)E→C的实验现象是__ 。
(4)写出下列反应的化学方程式或离子方程式:
A→D的离子方程式___ 。
E→C的化学方程式___ 。

(1)写出A、C的化学式:A
(2)检验B中阳离子的试剂是
(3)E→C的实验现象是
(4)写出下列反应的化学方程式或离子方程式:
A→D的离子方程式
E→C的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】高铁酸盐在能源、环保等方面有着广泛的用途。湿法、干法制备高铁酸盐的原理如下表所示:
(1)工业上用湿法制备高铁酸钾(K2FeO4)的流程如图所示:
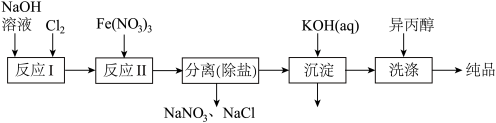
①洗涤粗品时选用异丙醇而不用水的理由是:________ 。
②反应II的离子方程式为___________ 。
③高铁酸钾在水中既能消毒杀菌,又能净水,是一种理想的水处理剂.它能消毒杀菌是因为_______ 它能净水的原因是_______ 。
(2)由流程图可见,湿法制备高铁酸钾时,需先制得高铁酸钠,然后再向高铁酸钠中加入饱和KOH溶液,即可析出高铁酸钾。
①加入饱和KOH溶液的目的是:__________ 。
②由以上信息可知:高铁酸钾的溶解度比高铁酸钠____ (填“大”或“小”)。
(3)干法制备K2FeO4的反应中氧化剂和还原剂的物质的量之比________
| 湿法 | 强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色高铁酸盐溶液 |
| 干法 | Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸盐和KNO2等产物 |
(1)工业上用湿法制备高铁酸钾(K2FeO4)的流程如图所示:

①洗涤粗品时选用异丙醇而不用水的理由是:
②反应II的离子方程式为
③高铁酸钾在水中既能消毒杀菌,又能净水,是一种理想的水处理剂.它能消毒杀菌是因为
(2)由流程图可见,湿法制备高铁酸钾时,需先制得高铁酸钠,然后再向高铁酸钠中加入饱和KOH溶液,即可析出高铁酸钾。
①加入饱和KOH溶液的目的是:
②由以上信息可知:高铁酸钾的溶解度比高铁酸钠
(3)干法制备K2FeO4的反应中氧化剂和还原剂的物质的量之比
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】A、B、C、D、E为原子序数依次增大的同周期元素,已知A、B、E 3种原子最外层共有11个电子,且这3种元素的最高价氧化物对应水化物两两皆能发生反应生成盐和水,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。
(1)写出下列元素符号: A___ ,B____ ,C____ ,D____ ,E________ 。
(2)写出A、B两元素最高价氧化物对应水化物相互反应的化学方程式:_____________________________ 。
(3)比较C、D的最高价氧化物对应水化物的酸性:_____________ (用化学式表示) 。
(4)用离子方程式表示实验室制取E的单质的原理:____________________________
(1)写出下列元素符号: A
(2)写出A、B两元素最高价氧化物对应水化物相互反应的化学方程式:
(3)比较C、D的最高价氧化物对应水化物的酸性:
(4)用离子方程式表示实验室制取E的单质的原理:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】某分子结构式如图所示。其中,X的原子核只有1个质子,元素Y、M、N、W的原子序数依次增大,且均位于X的下一周期;元素E的原子比W原子多8个电子。请用具体的化学用语回答下列问题:
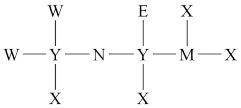
(1)Y在周期表中的位置是_______ , 的电子式为
的电子式为_______ 。
(2)含W的某种化合物的溶液常用来刻蚀玻璃,该化合物的化学式为_______ 。
(3)由X和Y形成的最简单的化合物的空间结构为_______ (填名称)。
(4)M的原子结构示意图为_______ 。由X、M、N三种元素形成的离子化合物的化学式为_______ 。
(5)实验室可用 、
、 分别与XE的浓溶液反应制备E单质,
分别与XE的浓溶液反应制备E单质, 与XE的浓溶液反应的化学方程式为
与XE的浓溶液反应的化学方程式为_______ 。若制备相同物质的量的E单质,消耗的 和
和 的物质的量之比为
的物质的量之比为_______ 。

(1)Y在周期表中的位置是
 的电子式为
的电子式为(2)含W的某种化合物的溶液常用来刻蚀玻璃,该化合物的化学式为
(3)由X和Y形成的最简单的化合物的空间结构为
(4)M的原子结构示意图为
(5)实验室可用
 、
、 分别与XE的浓溶液反应制备E单质,
分别与XE的浓溶液反应制备E单质, 与XE的浓溶液反应的化学方程式为
与XE的浓溶液反应的化学方程式为 和
和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】 X、Y、Z、M、R、Q是短周期主族元素,部分信息如下表所示:
(1)Y在元素周期表中的位置是____________________ ;R在自然界中有质量数为35和37的两种核素,它们之间的关系互为__________ 。
(2)Q的最高价氧化物对应的水化物与Z的最高价氧化物对应的水化物反应的离子方程式是____________________ 。
(3)下列事实能证明Y与R非金属性强弱的是_______ (选填字母序号)。
a.常温下Y的单质呈固态,R的单质呈气态 b.稳定性XR >YX4 c.Y与R形成的化合物中Y呈正价
(4)根据表中数据推测,Y的原子半径的最小范围是_________________ 。
(5)X单质与氧气在强碱性条件下形成燃料电池时的负极反应式为__________________ 。
(6)请用电子式表示Z2M的形成过程___________________________ 。
| X | Y | Z | M | R | Q | |
| 原子半径/nm | 0.186 | 0.074 | 0.099 | 0.143 | ||
| 主要化合价 | -4,+4 | -2 | -1,+7 | +3 | ||
| 其它 | 阳离子核外无电子 | 无机非金属材料的主角 | 焰色反应呈黄色 |
(2)Q的最高价氧化物对应的水化物与Z的最高价氧化物对应的水化物反应的离子方程式是
(3)下列事实能证明Y与R非金属性强弱的是
a.常温下Y的单质呈固态,R的单质呈气态 b.稳定性XR >YX4 c.Y与R形成的化合物中Y呈正价
(4)根据表中数据推测,Y的原子半径的最小范围是
(5)X单质与氧气在强碱性条件下形成燃料电池时的负极反应式为
(6)请用电子式表示Z2M的形成过程
您最近一年使用:0次



