高铁酸钠是一种新型高效水处理剂,主要制备方法如下:
湿法:Fe(OH)3+NaClO+NaOH—Na2FeO4+NaCl+H2O(反应未配平)
干法:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
下列说法正确的是
湿法:Fe(OH)3+NaClO+NaOH—Na2FeO4+NaCl+H2O(反应未配平)
干法:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
下列说法正确的是
| A.高铁酸钠既有杀菌消毒的作用也有净水的作用 |
| B.用湿法制备1molNa2FeO4需消耗1mol NaClO |
| C.干法中被FeSO4还原的Na2O2与做还原剂的Na2O2的物质的量之比为4:1 |
| D.分别用湿法和干法制备等量高铁酸钠,两个反应过程中转移的电子数相同 |
更新时间:2020-05-28 23:55:16
|
相似题推荐
多选题
|
适中
(0.65)
解题方法
【推荐1】已知还原性: >I->Br-,则向NaBr、NaI、Na2SO3的混合溶液中,通入一定量氯气后,将溶液蒸干并充分灼烧,得到固体剩余物质的组成可能是
>I->Br-,则向NaBr、NaI、Na2SO3的混合溶液中,通入一定量氯气后,将溶液蒸干并充分灼烧,得到固体剩余物质的组成可能是
 >I->Br-,则向NaBr、NaI、Na2SO3的混合溶液中,通入一定量氯气后,将溶液蒸干并充分灼烧,得到固体剩余物质的组成可能是
>I->Br-,则向NaBr、NaI、Na2SO3的混合溶液中,通入一定量氯气后,将溶液蒸干并充分灼烧,得到固体剩余物质的组成可能是| A.NaCl、Na2SO4 | B.NaCl、NaBr、Na2SO4 |
| C.NaCl、Na2SO4、Na2SO3 | D.NaCl、NaI、Na2SO4 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】中国科学技术大学的钱逸泰教授等以CCl4和金属钠为原料,在700 ℃时反应制造出纳米级金刚石粉末和另一种常见化合物。该成果发表在世界权威的《科学》杂志上,立即被科学家们高度评价为“稻草变黄金”。同学们对此有下列一些“理解”,你认为其中不正确的是
| A.金刚石属于金属单质 | B.另一种常见化合物为NaCl |
| C.CCl4发生还原反应 | D.这个反应是复分解反应 |
您最近一年使用:0次
【推荐1】铋酸钠(NaBiO3)是一种强氧化剂,不溶于冷水,在酸性条件下能把Mn2+氧化成MnO42-,发生的离子反应为:2Mn2++5NaBiO3+14H+=2MnO4-+5Bi3++5Na++7H2O。下列推断错误的是
| A.该反应可以检验溶液中是否存在Mn2+ |
| B.酸性条件可用稀硫酸提供 |
| C.若有0.2 mol氧化产物生成,转移电子数为0.5NA |
| D.NaBiO3可由下列反应制得:BiCl3+Cl2+NaCl+3H2O=NaBiO3+6HCl |
您最近一年使用:0次
【推荐2】向重铬酸盐酸性溶液中加入乙醚和H2O2,水层发生反应:Cr2O +4H2O2+2H+=2CrO5+5H2O(已知CrO5中Cr的化合价为+6价),乙醚层发生反应:CrO5+(C2H5)2O=CrO5•O(C2H5)2(蓝色)。反应现象为上层出现蓝色,一段时间后溶液蓝色褪去,且水相变为绿色(Cr3+),下列说法正确的是
+4H2O2+2H+=2CrO5+5H2O(已知CrO5中Cr的化合价为+6价),乙醚层发生反应:CrO5+(C2H5)2O=CrO5•O(C2H5)2(蓝色)。反应现象为上层出现蓝色,一段时间后溶液蓝色褪去,且水相变为绿色(Cr3+),下列说法正确的是
 +4H2O2+2H+=2CrO5+5H2O(已知CrO5中Cr的化合价为+6价),乙醚层发生反应:CrO5+(C2H5)2O=CrO5•O(C2H5)2(蓝色)。反应现象为上层出现蓝色,一段时间后溶液蓝色褪去,且水相变为绿色(Cr3+),下列说法正确的是
+4H2O2+2H+=2CrO5+5H2O(已知CrO5中Cr的化合价为+6价),乙醚层发生反应:CrO5+(C2H5)2O=CrO5•O(C2H5)2(蓝色)。反应现象为上层出现蓝色,一段时间后溶液蓝色褪去,且水相变为绿色(Cr3+),下列说法正确的是A.由水层反应可知,氧化性:Cr2O >CrO5 >CrO5 |
| B.乙醚在检验过程中作稳定剂和萃取剂,不可用乙醇代替 |
| C.CrO5•O(C2H5)2中不存在非极性键 |
| D.水相变为绿色的离子反应为4CrO5+12H+=4Cr3++6H2O+7O2↑ |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐3】明代《天工开物》记载了“火法”冶炼锌的方法:“炉甘石十斤,装载入一泥罐内,…然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,……冷淀,毁罐取出,……, 即倭铅也”,现代工业开发了用NH3-NH4Cl水溶液浸出氧化锌烟灰(主要成分为ZnO、少量 Pb、CuO和As2O3)制取高纯锌的工艺流程如图所示。

下列说法不正确的是

下列说法不正确的是
| A.《天工开物》中炼锌的方法中“泥封”的目的是防止得到的锌被氧化 |
| B.滤渣1的主要成分是Pb、As2O3 |
C.“氧化除杂”流程中发生化学反应的离子方程式是2AsCl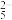 +2H2O2+6NH3·H2O=As2O5(胶体)+10Cl-+6NH +2H2O2+6NH3·H2O=As2O5(胶体)+10Cl-+6NH +5H2O +5H2O |
| D.“电解”含[Zn(NH3)4]2+的溶液时,在阳极上得到高纯锌 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】许多富脂糕点的包装盒内都装有一小包黑色的活性铁粉,长时间放置的糕点,其包装盒内的活性铁粉往往会变成红棕色。下列说法正确的是
| A.富脂食品长时间放置易被还原 |
B.红棕色固体的主要成分是 |
| C.活性铁粉变成红棕色的过程中铁粉发生了氧化反应 |
D.如果在包装盒内放入 ,也可起到与铁粉同样的作用 ,也可起到与铁粉同样的作用 |
您最近一年使用:0次
【推荐2】利用食盐水制取的工业流程如图所示,

装置①中的反应:NaCl+3H2O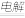 NaClO3+3H2
NaClO3+3H2
装置②中的反应:2NaClO3+4HCl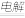 2ClO2+Cl2
2ClO2+Cl2 +2NaCl+2H2O
+2NaCl+2H2O
下列关于该流程说法不正确的是

装置①中的反应:NaCl+3H2O
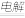 NaClO3+3H2
NaClO3+3H2
装置②中的反应:2NaClO3+4HCl
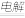 2ClO2+Cl2
2ClO2+Cl2 +2NaCl+2H2O
+2NaCl+2H2O下列关于该流程说法不正确的是
| A.该流程中Cl2、NaCl都可以循环利用 |
| B.装置②中,浓HCl体现了还原性 |
| C.装置②发生的反应中,Cl2是氧化产物,NaCl是还原产物 |
| D.为了使Cl2完全转化为HCl,需要向装置③中补充Cl2 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐3】已知NaBiO3为浅黄色或褐色沉淀。NaBiO3与硝酸酸化的MnSO4溶液发生反应:5NaBiO3+2Mn2++14H+=2MnO +5Bi3++5Na++7H2O。下列推断正确的是
+5Bi3++5Na++7H2O。下列推断正确的是
 +5Bi3++5Na++7H2O。下列推断正确的是
+5Bi3++5Na++7H2O。下列推断正确的是| A.上述反应中的MnSO4溶液也可以用盐酸或硫酸酸化 |
B.可用BiO 检验Na+的存在 检验Na+的存在 |
| C.由上述反应可知氧化性:NaBiO3>HNO3>KMnO4 |
| D.NaBiO3与浓盐酸反应的离子方程式为:NaBiO3+2Cl-+6H+=Bi3++Na++3H2O+Cl2↑ |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】高铁酸钾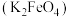 是一种新型、高效、多功能绿色水处理剂。工业上制备高铁酸钾以及高铁酸钾处理污水的部分流程如下:
是一种新型、高效、多功能绿色水处理剂。工业上制备高铁酸钾以及高铁酸钾处理污水的部分流程如下:

以下说法不正确的是
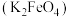 是一种新型、高效、多功能绿色水处理剂。工业上制备高铁酸钾以及高铁酸钾处理污水的部分流程如下:
是一种新型、高效、多功能绿色水处理剂。工业上制备高铁酸钾以及高铁酸钾处理污水的部分流程如下:
以下说法不正确的是
| A.过程①中一定发生了氧化还原反应 |
B.污水处理中产生 胶体,使悬浮物聚沉,利用了 胶体,使悬浮物聚沉,利用了 胶体的强氧化性 胶体的强氧化性 |
C.另一种在碱性条件下制备 的反应可能是: 的反应可能是: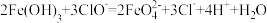 |
D. 还可以用于处理废水,例如可以把废水中的 还可以用于处理废水,例如可以把废水中的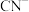 转化为两种无毒气体,反应过程中, 转化为两种无毒气体,反应过程中,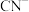 做还原剂,被 做还原剂,被 氧化 氧化 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,下列反应可制K2FeO4:2Fe(OH)3+3Cl2+10KOH=2K2FeO4+6 +8H2O。下列说法不正确的是( )
+8H2O。下列说法不正确的是( )
 +8H2O。下列说法不正确的是( )
+8H2O。下列说法不正确的是( )| A.每转移1mole-,可以得到33gK2FeO4 |
B. 处的物质应为KClO 处的物质应为KClO |
| C.该反应中铁元素的化合价升高 |
| D.该反应条件下氧化性:Cl2>K2FeO4 |
您最近一年使用:0次

 2Sn+a M↑+CO2↑,则下列说法中错误的是
2Sn+a M↑+CO2↑,则下列说法中错误的是

