硬铝(因其主要成分,在此仅看作Al-Cu合金)常用于建筑装潢。1.18g某种硬铝恰好与10mL某浓度的硝酸完全反应,生成的混合气体(其中NO2与NO的体积比为2:1)再与448mL氧气(标准状况)混合,恰好能被水完全吸收。则该硝酸的物质的量浓度_____________ mol/L。请写出简要计算过程。
更新时间:2020-06-26 10:42:07
|
相似题推荐
【推荐1】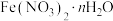 可用作媒染剂、医药、分析试剂、催化剂等,某同学设计实验确定其结晶水数目。用电子天平称取样品17.280g,一定条件下,经热分解测得气体产物中有
可用作媒染剂、医药、分析试剂、催化剂等,某同学设计实验确定其结晶水数目。用电子天平称取样品17.280g,一定条件下,经热分解测得气体产物中有 、
、 、
、 、
、 ,其中水的质量为6.300g,残留的固体产物是
,其中水的质量为6.300g,残留的固体产物是 ,质量为4.800g。
,质量为4.800g。
(1)n=_______ (写出计算过程)。
(2)在标准状况下气体产物中 的体积为
的体积为_______ L。
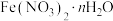 可用作媒染剂、医药、分析试剂、催化剂等,某同学设计实验确定其结晶水数目。用电子天平称取样品17.280g,一定条件下,经热分解测得气体产物中有
可用作媒染剂、医药、分析试剂、催化剂等,某同学设计实验确定其结晶水数目。用电子天平称取样品17.280g,一定条件下,经热分解测得气体产物中有 、
、 、
、 、
、 ,其中水的质量为6.300g,残留的固体产物是
,其中水的质量为6.300g,残留的固体产物是 ,质量为4.800g。
,质量为4.800g。(1)n=
(2)在标准状况下气体产物中
 的体积为
的体积为
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】铜既能与稀硝酸反应,也能与浓硝酸反应,反应方程式为:Cu4HNO3(浓)Cu(NO3)22NO22H2O;3Cu8HNO3(稀)3Cu(NO3)22NO4H2O。现将25.6gCu投入50mL12mol/L的浓硝酸中,充分反应后,收集到4.48L(标准状态)NO和NO2的混合气体。
(1)被还原硝酸的物质的量是_____ mol。
(2)试分析判断25.6gCu和50mL12mo/L的硝酸反应后何者有剩余?______ ;其物质的量是_____ 。
(3)如果4.48L(标准状态)NO和NO2的混合气体是通过排水法进行收集,则收集到的气体的体积是____________ L。
(4)如果向反应后的体系中再加入200mL4mol/L的稀硫酸,是否会有气体逸出_____ (填是或否),如有请计算产生气体的体积(标准状态)为_____ 。
(1)被还原硝酸的物质的量是
(2)试分析判断25.6gCu和50mL12mo/L的硝酸反应后何者有剩余?
(3)如果4.48L(标准状态)NO和NO2的混合气体是通过排水法进行收集,则收集到的气体的体积是
(4)如果向反应后的体系中再加入200mL4mol/L的稀硫酸,是否会有气体逸出
您最近半年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】为了测定某铜银合金的成分,将30.0g合金溶于80mL13.5mol/L的浓硝酸中,待合金完全溶解后,收集到气体6.72L(标准状况),并测得溶液中的c(H+)=1mol/L。假设反应后溶液的体积仍为80mL,试计算:
(1)被还原的硝酸的物质的量________ ;
(2)合金中银的质量分数________ ;
(3)若需要将全部尾气用水吸收,需要的氧气体积(标准状况)________ ;
(4)如果将所得溶液中全部金属阳离子沉淀,至少需加入1mol/LNaOH溶液的体积________ 。
(1)被还原的硝酸的物质的量
(2)合金中银的质量分数
(3)若需要将全部尾气用水吸收,需要的氧气体积(标准状况)
(4)如果将所得溶液中全部金属阳离子沉淀,至少需加入1mol/LNaOH溶液的体积
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】将64 g铜与200 mL一定浓度的硝酸反应,铜完全溶解产生的NO 和NO2混合气体在标准状况下的体积为22.4 L。请回答:
(1)在标准状况下NO的体积为___________________ ?
(2)待产生的气体全部释放后,向溶液中加入500 mL, 5mol/L的NaOH溶液,恰好使溶液中Cu2+全部转化成沉淀,则原硝酸的浓度为__________________ ?
(1)在标准状况下NO的体积为
(2)待产生的气体全部释放后,向溶液中加入500 mL, 5mol/L的NaOH溶液,恰好使溶液中Cu2+全部转化成沉淀,则原硝酸的浓度为
您最近半年使用:0次



