29. 乙醛是一种重要的烃类衍生物,广泛应用于纺织、医药、化纤、染料和食品工业。
(一)以乙烯和氧气(或空气)为原料,在由PdCl
2、CuCl
2、盐酸组成的催化剂水溶液中,进行液相氧化生产乙醛,工业上一般控制反应温度在120~130℃,压强在300~350KPa。又称Wacker法。其反应式为:
主反应:CH
2═CH
2(g) +

O
2(g)

CH
3CHO(g) Δ
H=-243.2 kJ·mol
-1副反应:

CH
2═CH
2(g) +

O
2(g)

CO
2(g)+H
2O(g) Δ
H=-705.5kJ·mol
-1(1)已知:水的汽化热是44.0 kJ·mol
-1,请计算乙烯的燃烧热:Δ
H =
__________ kJ·mol
-1汽化热:在标准大气压(101KPa)下,使1mol物质在一定温度下蒸发所需要的热量。
(2)Wacker法乙烯氧化制乙醛过程,按照以下机理进行:
①乙烯羰基化反应:_____________________________
②金属钯的再氧化反应:Pd + 2CuCl
2 = PdCl
2 + 2CuCl
③氯化亚铜的氧化反应:2CuCl +

O
2 + 2HCl = 2CuCl
2 + H
2O
请写出①的反应方程式
__________________________。
(3)下列有关说法正确的是
_______________ A.Wacker法制乙醛反应中,氯化钯是反应催化剂,氯化铜的作用是使催化剂再生,没有氯化铜的存在,就不能完成此催化过程。
B.工业上采用的原料气中乙烯大量过量,并有大量未反应的乙烯气要循环使用,这样可提高乙烯利用率,同时原料气中加入CO
2有利于提高乙醛选择性。
C.原料气中乙烯大量过量的原因可能是为了让乙烯的体积分数处在爆炸极限范围之外,以避免危险的发生。
D.乙烯氧化生成乙醛的反应是在气-液相中进行的,加压和升温都有利于提高乙烯和氧在液体中的溶解度,加快反应速率。
(4)控制反应条件在120~130℃和300~350KPa,原料气的体积比是V(C
2H
4):V(O
2):V(CO
2):V(N
2) = 15:10.5:9.5:65,以一定流速通入催化剂水溶液中,一段时间后反应达平衡,测得乙烯的体积分数是0.1,氧气的体积分数是0.05,如果充入100mol原料气,请计算反应达平衡时,
n(CH
3CHO) =
___________ mol。(不考虑HCl的挥发)
(二)实际工业生产要求有较高产量,速率不能太低,转化率尽可能大,所以应尽量使平衡正向移动。
(1)可逆反应:aA+bB

rR +s S ,对反应物A,净反应速率为r
A = r
正(X
A) – r
逆(X
A),X
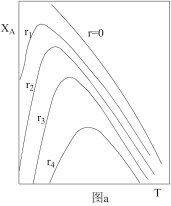
A为反应物A的转化率,图a表示反应物A的转化率和A的净反应速率与温度(T)的关系图。图a分析可知,在相同温度下,净反应速率为
________时,X
A最大(从“r=0、r
1、r
2、r
3、r
4”选填);由图a判断该反应是
__________反应(填“吸热”或“放热”),并简述原因
__________。
(2)请在图a中绘制:在不同r下,符合工业生产要求的最佳温度
__________。