天然石灰石是工业生产中重要的原材料之一,它的主要成分是 CaCO3,一般以CaO 的质量分数表示钙含量,常采用高锰酸钾法测定。步骤如下:
Ⅰ.称取 a g 研细的石灰石样品于 250 mL 烧杯中,加过量稀盐酸溶解,水浴加热 10 分钟;
Ⅱ.稍冷后逐滴加入氨水至溶液 pH≈4,再缓慢加入适量(NH4)2C2O4 溶液,继续水浴加热30 分钟;
Ⅲ.冷却至室温后过滤出沉淀,用另外配制的稀(NH4)2C2O4 溶液洗涤沉淀三次,再用蒸馏水洗涤至洗涤液中无法检出 Cl−;
Ⅳ.加入适量热的稀硫酸至沉淀中,获得的溶液用 c mol·L−1 KMnO4 标准溶液滴定至终点。
Ⅴ.平行测定三次,消耗KMnO4 溶液的体积平均为 V mL。
已知:H2C2O4 是弱酸;CaC2O4 是难溶于水的白色沉淀。
⑴Ⅰ中为了加快反应速率而采取的操作有_____ 。
⑵Ⅱ中加入氨水调节溶液 pH 的作用是_____ 。
⑶Ⅲ中洗涤得到干净的沉淀。
①结合平衡移动原理,解释用稀(NH4)2C2O4 溶液洗涤沉淀的目的__________________________ 。
②检测洗涤液中无 Cl−的试剂和现象是__________________________ 。
③若沉淀中的 Cl−未洗涤干净,则最终测量结果_____ (填“偏大”、“偏小”或“不变”)。
⑷Ⅳ中用 KMnO4 标准溶液滴定。
①滴定时发生反应的离子方程式为_____ 。
②滴定至终点的现象为_____ 。
③样品中以CaO 质量分数表示的钙含量为_____ (列出表达式)。
Ⅰ.称取 a g 研细的石灰石样品于 250 mL 烧杯中,加过量稀盐酸溶解,水浴加热 10 分钟;
Ⅱ.稍冷后逐滴加入氨水至溶液 pH≈4,再缓慢加入适量(NH4)2C2O4 溶液,继续水浴加热30 分钟;
Ⅲ.冷却至室温后过滤出沉淀,用另外配制的稀(NH4)2C2O4 溶液洗涤沉淀三次,再用蒸馏水洗涤至洗涤液中无法检出 Cl−;
Ⅳ.加入适量热的稀硫酸至沉淀中,获得的溶液用 c mol·L−1 KMnO4 标准溶液滴定至终点。
Ⅴ.平行测定三次,消耗KMnO4 溶液的体积平均为 V mL。
已知:H2C2O4 是弱酸;CaC2O4 是难溶于水的白色沉淀。
⑴Ⅰ中为了加快反应速率而采取的操作有
⑵Ⅱ中加入氨水调节溶液 pH 的作用是
⑶Ⅲ中洗涤得到干净的沉淀。
①结合平衡移动原理,解释用稀(NH4)2C2O4 溶液洗涤沉淀的目的
②检测洗涤液中无 Cl−的试剂和现象是
③若沉淀中的 Cl−未洗涤干净,则最终测量结果
⑷Ⅳ中用 KMnO4 标准溶液滴定。
①滴定时发生反应的离子方程式为
②滴定至终点的现象为
③样品中以CaO 质量分数表示的钙含量为
更新时间:2020-07-01 19:20:07
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为:2MnO4-+5H2C2O4+6H+===2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
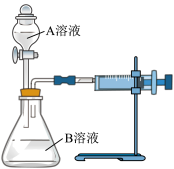
(1)该实验探究的是________ 因素对化学反应速率的影响。相同时间内针筒中所得CO2的体积大小关系是________ >________ (填实验序号)。
(2)若实验①在2 min末收集了4.48 mL CO2(标准状况下),则在2 min末,c(MnO4-)=________ mol·L-1。(假设混合溶液体积为50 mL)
(3)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定________ 来比较化学反应速率。
(4)小组同学发现反应速率变化如下图,其中t1~t2时间内速率变快的主要原因可能是:①产物Mn2+是反应的催化剂、②________ 。


| 实验序号 | A溶液 | B溶液 |
| ① | 20 mL0.1mol·L-1H2C2O4溶液 | 30 mL0.01mol·L-1KMnO4溶液 |
| ② | 20 mL0.2mol·L-1H2C2O4溶液 | 30 mL0.01mol·L-1KMnO4溶液 |
(2)若实验①在2 min末收集了4.48 mL CO2(标准状况下),则在2 min末,c(MnO4-)=
(3)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定
(4)小组同学发现反应速率变化如下图,其中t1~t2时间内速率变快的主要原因可能是:①产物Mn2+是反应的催化剂、②

您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】某同学在实验室研究化学反应快慢的影响因素。
(1)研究催化剂对化学反应快慢的影响,实验步骤如下:
I.向3支大小相同的试管a、b、c中各加入相同体积(2mL)5% 溶液;
溶液;
Ⅱ.向试管a中加入少量 粉末,向试管b中滴加1~2滴
粉末,向试管b中滴加1~2滴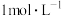
 溶液。
溶液。
得出实验结论: 与
与 均能加快
均能加快 的分解,且前者的催化效率高得多。
的分解,且前者的催化效率高得多。
①步骤Ⅰ中分别向3支试管中加入相同体积的溶液的目的是_________ 。
②设计试管c的目的是_________ 。
③若继续用上述实验药品研究温度对 分解快慢的影响,为了便于观察,选择的催化剂是
分解快慢的影响,为了便于观察,选择的催化剂是_____ ,原因是_________ 。
(2)现提供下列实验用品研究化学反应快慢的影响因素。
实验仪器:试管、烧杯、量筒、天平、秒表
实验药品:铝片、铝粉、 盐酸、
盐酸、 盐酸
盐酸
①利用所提供实验用品,可研究的化学反应快慢的影响因素是________ ,为了便于观察,你建议记录的数据是_____ 。
②设计实验探究温度对化学反应快慢的影响,说明实验步骤(实验仪器和药品任选):________ 。
(1)研究催化剂对化学反应快慢的影响,实验步骤如下:
I.向3支大小相同的试管a、b、c中各加入相同体积(2mL)5%
 溶液;
溶液;Ⅱ.向试管a中加入少量
 粉末,向试管b中滴加1~2滴
粉末,向试管b中滴加1~2滴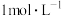
 溶液。
溶液。得出实验结论:
 与
与 均能加快
均能加快 的分解,且前者的催化效率高得多。
的分解,且前者的催化效率高得多。①步骤Ⅰ中分别向3支试管中加入相同体积的溶液的目的是
②设计试管c的目的是
③若继续用上述实验药品研究温度对
 分解快慢的影响,为了便于观察,选择的催化剂是
分解快慢的影响,为了便于观察,选择的催化剂是(2)现提供下列实验用品研究化学反应快慢的影响因素。
实验仪器:试管、烧杯、量筒、天平、秒表
实验药品:铝片、铝粉、
 盐酸、
盐酸、 盐酸
盐酸①利用所提供实验用品,可研究的化学反应快慢的影响因素是
②设计实验探究温度对化学反应快慢的影响,说明实验步骤(实验仪器和药品任选):
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐3】甲醇是有机化工中重要的合成原料,在催化剂的作用下利用甲醇合成乙烯和丙烯的技术被称为 技术。该技术涉及的主要反应为:
技术。该技术涉及的主要反应为:
i.
ii.
请回答下列问题:
(1)反应 的反应热
的反应热
___________ kJ/mol;
(2)在特定催化剂条件下,两反应存在竞争关系,其反应进程中能量的变化如图所示。该催化剂条件下生成___________ 的选择性更高(填化学式 ),理由为___________ ;
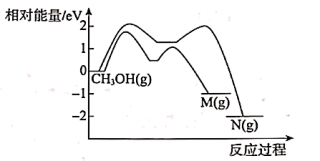
(3)TK时,在体积为1L的恒容密闭容器中充入1molCH3OH(g)发生反应i和反应ii,5min后压强不再改变,此时测得H2O(g)的物质的量浓度为0.8mol/L。
①5min内H2O(g)的生成速率为___________ mol⋅L-1⋅min-1;
②升高温度后,C2H4的平衡产率反而提高,分析原因为___________ 。
 技术。该技术涉及的主要反应为:
技术。该技术涉及的主要反应为:i.

ii.

请回答下列问题:
(1)反应
 的反应热
的反应热
(2)在特定催化剂条件下,两反应存在竞争关系,其反应进程中能量的变化如图所示。该催化剂条件下生成

(3)TK时,在体积为1L的恒容密闭容器中充入1molCH3OH(g)发生反应i和反应ii,5min后压强不再改变,此时测得H2O(g)的物质的量浓度为0.8mol/L。
①5min内H2O(g)的生成速率为
②升高温度后,C2H4的平衡产率反而提高,分析原因为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】某一种胃药中的抑酸剂为碳酸钙,其中所含的抑酸剂质量的测定如下:
①需配制0.1 mol·L-1的HCl溶液和0.1 mol·L-1的NaOH溶液
②取一粒(药片质量相同) 0.2 g的此胃药片,磨碎后加入20.0 mL蒸馏水
③以酚酞为指示剂,用0.1 mol·L-1的NaOH溶液滴定,用去V mL达滴定终点
④加入25 mL 0.1 mol·L-1的HCl溶液
(1)写出实验过程的步骤(写编号顺序)_______ 。
(2)如图所示容器中配制0.1 mol·L-1的HCl溶液和0.1 mol·L-1的NaOH溶液肯定不需要的仪器是(填序号)_______ ,配制上述溶液还需要的玻璃仪器是_______ (填仪器名称)。

(3)配制上述溶液应选用的容量瓶规格是(填字母)_______ 。
A.50 mL 50 mL B.100 mL 100 mL C.100 mL 150 mL D.250 mL 250 mL
(4)写出有关的化学反应方程式:_______ 、_______ 。
(5)每粒胃药中含碳酸钙的质量为_______ g。
①需配制0.1 mol·L-1的HCl溶液和0.1 mol·L-1的NaOH溶液
②取一粒(药片质量相同) 0.2 g的此胃药片,磨碎后加入20.0 mL蒸馏水
③以酚酞为指示剂,用0.1 mol·L-1的NaOH溶液滴定,用去V mL达滴定终点
④加入25 mL 0.1 mol·L-1的HCl溶液
(1)写出实验过程的步骤(写编号顺序)
(2)如图所示容器中配制0.1 mol·L-1的HCl溶液和0.1 mol·L-1的NaOH溶液肯定不需要的仪器是(填序号)

(3)配制上述溶液应选用的容量瓶规格是(填字母)
A.50 mL 50 mL B.100 mL 100 mL C.100 mL 150 mL D.250 mL 250 mL
(4)写出有关的化学反应方程式:
(5)每粒胃药中含碳酸钙的质量为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
【推荐2】“绿水青山就是金山银山”,研究 脱硝和脱硫技术成为人们共同关注的课题。
(1)2NO(g)+O2(g)⇌2NO2(g)的反应历程如下:
反应Ⅰ:2NO(g)⇌N2O2(g)(快);v1正=k1正•c2(NO)、v1逆=k1逆•c(N2O2);
反应Ⅱ:N2O2(g)+O2(g)⇌2NO2(g)(慢);v2正=k2正•c(N2O2)•c(O2)、v2逆=k2逆•c2 (NO2);
在一定条件下,反应2NO(g)+O2(g)⇌2NO2(g)达到平衡状态,平衡常数K=_____ (用含k1正、k1逆、k2正、k2逆的代数式表示)。
(2)烟道气中的NOx是主要的大气污染物之一,为了监测其含量,选用如下检测方法。
将v L气样通入适量酸化的H2O2溶液中,使NO完全被氧化成NO3﹣,加水稀释至100.00 mL.量取20.00 mL该溶液,加入v1 mL c1 mol•L﹣1 FeSO4标准溶液(过量),充分反应后,用c2 mol•L﹣1 K2Cr2O7标准溶液滴定剩余的Fe2+,终点时消耗v2 mL。
①NO被H2O2氧化为NO3﹣ 的离子方程式为________ 。
②加水稀释到100.00mL所用的玻璃仪器除量筒、烧杯、玻璃棒、胶头滴管外,还需要_____ ;
③滴定过程中发生下列反应:
3Fe2++NO3﹣+4H+═NO↑+3Fe3++2H2O
Cr2O72﹣+6Fe2++14H+═2Cr3++6Fe3++7H2O
则气样中NO的含量为_____ mg/L。
下列操作会使滴定结果偏高的是_____
A.滴定管未用标准液润洗
B.锥形瓶洗净后还存留少量的水
C.滴定管滴定前读数正确,滴定后俯视读数
D.FeSO4标准溶液部分变质
(1)2NO(g)+O2(g)⇌2NO2(g)的反应历程如下:
反应Ⅰ:2NO(g)⇌N2O2(g)(快);v1正=k1正•c2(NO)、v1逆=k1逆•c(N2O2);
反应Ⅱ:N2O2(g)+O2(g)⇌2NO2(g)(慢);v2正=k2正•c(N2O2)•c(O2)、v2逆=k2逆•c2 (NO2);
在一定条件下,反应2NO(g)+O2(g)⇌2NO2(g)达到平衡状态,平衡常数K=
(2)烟道气中的NOx是主要的大气污染物之一,为了监测其含量,选用如下检测方法。
将v L气样通入适量酸化的H2O2溶液中,使NO完全被氧化成NO3﹣,加水稀释至100.00 mL.量取20.00 mL该溶液,加入v1 mL c1 mol•L﹣1 FeSO4标准溶液(过量),充分反应后,用c2 mol•L﹣1 K2Cr2O7标准溶液滴定剩余的Fe2+,终点时消耗v2 mL。
①NO被H2O2氧化为NO3﹣ 的离子方程式为
②加水稀释到100.00mL所用的玻璃仪器除量筒、烧杯、玻璃棒、胶头滴管外,还需要
③滴定过程中发生下列反应:
3Fe2++NO3﹣+4H+═NO↑+3Fe3++2H2O
Cr2O72﹣+6Fe2++14H+═2Cr3++6Fe3++7H2O
则气样中NO的含量为
下列操作会使滴定结果偏高的是
A.滴定管未用标准液润洗
B.锥形瓶洗净后还存留少量的水
C.滴定管滴定前读数正确,滴定后俯视读数
D.FeSO4标准溶液部分变质
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】锆(Zr)产品广泛用于陶瓷、化工、电子等行业。我国是氯氧化锆的主要生产和出口国,产能占世界总产能的90%以上。用ZrC(杂质主要含C和SiO2)生产ZrOCl2·8H2O的工艺流程如图所示。

已知:
Ⅰ.Na2ZrO3不溶于水,易溶于无机酸。
Ⅱ.ZrOCl2·8H2O的溶解度随温度升高和酸度降低而升高。
回答下列问题:
(1)“碱熔”前,对ZrC进行机械粉碎的目的是_______ 。
(2)“碱熔”时,生成Na2ZrO3的化学方程式为_______ ,反应应在_______ (填标号)中进行。
A.陶瓷坩埚 B.石英坩埚 C.铁质坩埚 D.铝质坩埚
(3)“碱熔”过程中,配料比(NaOH与ZrC的质量比)对锆转化率的影响如下表所示:
最适宜的配料比为_______ 。
(4)“水洗”的目的是_______ 。
(5)“酸浸”时,滤渣中的Na2ZrO3转化为可溶性的ZrOCl2,以ZrO2+的形式存在于溶液中,该反应的离子方程式为_______ 。为减少产品损失,“操作”中的洗涤液最好选用_______ 。
(6)用EDTA可快速测定酸浸液中锆的含量,其操作步骤如下:
①用移液管吸取10.00 mL酸浸液于250 mL锥形瓶中,加入约100 mL水;
②以6 mol·L-1的盐酸调节溶液pH在0~0.3,加入0.2 g盐酸羟胺,加热煮沸;
③加入2滴二甲酚橙指示剂,趁热用0.02000 mol·L-1 EDTA标准溶液进行滴定,EDTA与ZrO2+按1︰1的比例进行螯合;
④至溶液由紫红色突变为亮黄色且30 s保持不变色,即为终点。
滴定过程中消耗EDTA的相关数据如下图所示:
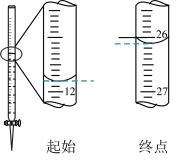
根据相关数据,计算酸浸液中锆的含量(以ZrO2计)为_______ mg·mL-1(保留两位小数)。

已知:
Ⅰ.Na2ZrO3不溶于水,易溶于无机酸。
Ⅱ.ZrOCl2·8H2O的溶解度随温度升高和酸度降低而升高。
回答下列问题:
(1)“碱熔”前,对ZrC进行机械粉碎的目的是
(2)“碱熔”时,生成Na2ZrO3的化学方程式为
A.陶瓷坩埚 B.石英坩埚 C.铁质坩埚 D.铝质坩埚
(3)“碱熔”过程中,配料比(NaOH与ZrC的质量比)对锆转化率的影响如下表所示:
| 配料比 | 1.0 | 1.1 | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 |
| 转化率/% | 84.02 | 89.07 | 91.97 | 93.73 | 99.06 | 99.12 | 99.11 |
(4)“水洗”的目的是
(5)“酸浸”时,滤渣中的Na2ZrO3转化为可溶性的ZrOCl2,以ZrO2+的形式存在于溶液中,该反应的离子方程式为
(6)用EDTA可快速测定酸浸液中锆的含量,其操作步骤如下:
①用移液管吸取10.00 mL酸浸液于250 mL锥形瓶中,加入约100 mL水;
②以6 mol·L-1的盐酸调节溶液pH在0~0.3,加入0.2 g盐酸羟胺,加热煮沸;
③加入2滴二甲酚橙指示剂,趁热用0.02000 mol·L-1 EDTA标准溶液进行滴定,EDTA与ZrO2+按1︰1的比例进行螯合;
④至溶液由紫红色突变为亮黄色且30 s保持不变色,即为终点。
滴定过程中消耗EDTA的相关数据如下图所示:

根据相关数据,计算酸浸液中锆的含量(以ZrO2计)为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】亚氯酸钠( )是一种重要的消每杀菌剂,也常用来漂白织物,可通过下列流程得到
)是一种重要的消每杀菌剂,也常用来漂白织物,可通过下列流程得到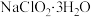 。
。
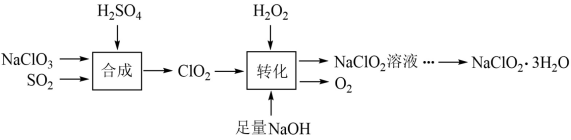
(1)“合成”中发生反应: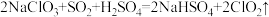 ,该反应是
,该反应是___________ (填反应类型)。 属于
属于___________ (填氧化物、酸、碱或盐),其在水浴液中的电离方程式为___________ 。
(2)将得到的 溶液进行
溶液进行___________ (填实验操作名称),过滤洗涤,得到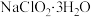 。
。
(3)为确定样品的纯度,某课外兴趣活动小组进行如下实验:
步骤一:称取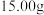 样品,用适量蒸馏水溶解后,加入略过量的
样品,用适量蒸馏水溶解后,加入略过量的 溶液,充分反应。(反应方程式为:
溶液,充分反应。(反应方程式为: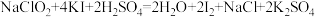 )
)
步骤二:加水,使反应后溶液的总体积变为 ,再取
,再取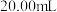 于锥形瓶。向锥形瓶中滴加两滴淀粉溶液,用一定浓度的
于锥形瓶。向锥形瓶中滴加两滴淀粉溶液,用一定浓度的 溶液与之反应。(反应方程式为:
溶液与之反应。(反应方程式为: )
)
步骤三:重复以上操作2~3次,测得平均消耗质量分数为20%的 ,溶液
,溶液 。求该样品的纯度
。求该样品的纯度___________ 。(写出计算过程,计算结果保留两位小数)
 )是一种重要的消每杀菌剂,也常用来漂白织物,可通过下列流程得到
)是一种重要的消每杀菌剂,也常用来漂白织物,可通过下列流程得到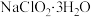 。
。
(1)“合成”中发生反应:
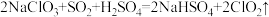 ,该反应是
,该反应是 属于
属于(2)将得到的
 溶液进行
溶液进行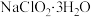 。
。(3)为确定样品的纯度,某课外兴趣活动小组进行如下实验:
步骤一:称取
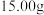 样品,用适量蒸馏水溶解后,加入略过量的
样品,用适量蒸馏水溶解后,加入略过量的 溶液,充分反应。(反应方程式为:
溶液,充分反应。(反应方程式为: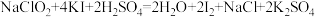 )
)步骤二:加水,使反应后溶液的总体积变为
 ,再取
,再取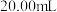 于锥形瓶。向锥形瓶中滴加两滴淀粉溶液,用一定浓度的
于锥形瓶。向锥形瓶中滴加两滴淀粉溶液,用一定浓度的 溶液与之反应。(反应方程式为:
溶液与之反应。(反应方程式为: )
)步骤三:重复以上操作2~3次,测得平均消耗质量分数为20%的
 ,溶液
,溶液 。求该样品的纯度
。求该样品的纯度
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】SO2的污染防治与利用对于环境保护意义重大。某化学小组在实验室中对SO2的制备、性质及回收利用等相关问题进行探究。请回答下列问题:
(1)制备并收集纯净的SO2

①用上图装置制备纯净的SO2,发生装置中反应的化学方程式为_______ 。
②装置的连接顺序为:a→_______ (按气流方向,用字母标号表示)。
(2)设计实验探究SO2中+4价S的性质
限选试剂:NaOH溶液、稀H2SO4、H2O2溶液、FeCl3溶液、淀粉KI溶液、新制H2S溶液
填写表格中相应内容:
①_______ ; ②_______ ;③_______ ; ④_______ 。
(3)设计回收利用SO2的途径: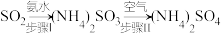 。该小组欲测定步骤II中(NH4)2SO3的转化率(α),设计如下实验方案:一定条件下,向100mLcmol/L的(NH4)2SO3溶液中通入空气,向反应后的溶液中加入过量的盐酸,再加入足量的氯化钡溶液,生成沉淀,将沉淀过滤、洗涤、干燥、称量,质量为mg。
。该小组欲测定步骤II中(NH4)2SO3的转化率(α),设计如下实验方案:一定条件下,向100mLcmol/L的(NH4)2SO3溶液中通入空气,向反应后的溶液中加入过量的盐酸,再加入足量的氯化钡溶液,生成沉淀,将沉淀过滤、洗涤、干燥、称量,质量为mg。
①检验沉淀是否洗净的方法是_______ 。
②α=_______ ×100%(用含c、m的代数式表示)。

(1)制备并收集纯净的SO2

①用上图装置制备纯净的SO2,发生装置中反应的化学方程式为
②装置的连接顺序为:a→
(2)设计实验探究SO2中+4价S的性质
限选试剂:NaOH溶液、稀H2SO4、H2O2溶液、FeCl3溶液、淀粉KI溶液、新制H2S溶液
| 实验操作 | 实验现象 | 实验结论 | |
| 实验一 | 将SO2通入新制H2S溶液中 | 溶液变浑浊 | SO2中+4价S具有________性 |
| 实验二 | 将SO2通入_________中 | ________ | SO2中+4价S具有还原性,反应的离子方程式为_______ |
①
(3)设计回收利用SO2的途径:
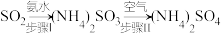 。该小组欲测定步骤II中(NH4)2SO3的转化率(α),设计如下实验方案:一定条件下,向100mLcmol/L的(NH4)2SO3溶液中通入空气,向反应后的溶液中加入过量的盐酸,再加入足量的氯化钡溶液,生成沉淀,将沉淀过滤、洗涤、干燥、称量,质量为mg。
。该小组欲测定步骤II中(NH4)2SO3的转化率(α),设计如下实验方案:一定条件下,向100mLcmol/L的(NH4)2SO3溶液中通入空气,向反应后的溶液中加入过量的盐酸,再加入足量的氯化钡溶液,生成沉淀,将沉淀过滤、洗涤、干燥、称量,质量为mg。①检验沉淀是否洗净的方法是
②α=

您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】实验室用如下装置测定 和
和 固体混合物中
固体混合物中 的质量,D装置的硬质双通玻璃管中的固体物质是
的质量,D装置的硬质双通玻璃管中的固体物质是 和
和 的混合物。
的混合物。
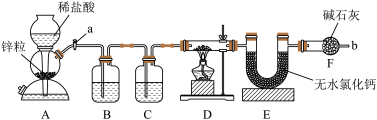
(1)装入药品之前需要___________ 。
(2)为了安全,在点燃D处的酒精灯之前,必须在b处___________ 。
(3)装置B的作用是___________ 。装置C中盛装的液体是___________ ,所起的作用是___________ 。
(4)点燃D处的酒精灯,写出在硬质双通玻璃管中发生反应的化学方程式___________ 。
(5)若 和
和 固体混合物的质量为
固体混合物的质量为 ,反应完全后U形管的质量增加
,反应完全后U形管的质量增加 ,则混合物中
,则混合物中 的质量为
的质量为___________ g。
 和
和 固体混合物中
固体混合物中 的质量,D装置的硬质双通玻璃管中的固体物质是
的质量,D装置的硬质双通玻璃管中的固体物质是 和
和 的混合物。
的混合物。
(1)装入药品之前需要
(2)为了安全,在点燃D处的酒精灯之前,必须在b处
(3)装置B的作用是
(4)点燃D处的酒精灯,写出在硬质双通玻璃管中发生反应的化学方程式
(5)若
 和
和 固体混合物的质量为
固体混合物的质量为 ,反应完全后U形管的质量增加
,反应完全后U形管的质量增加 ,则混合物中
,则混合物中 的质量为
的质量为
您最近一年使用:0次



