短周期元素甲、乙、丙、丁的原子序数依次增大,甲和乙形成的气态化合物的水溶液呈碱性,乙位于第VA族,甲和丙同主族,丁原子最外层电子数与电子层数相等,下列叙述正确的是( )
| A.原子半径:丙<丁<乙 | B.单质的还原性:丁>丙>甲 |
| C.甲、乙、丙的氧化物均为共价化合物 | D.乙、丙、丁的最高价氧化物对应的水化物能相互反应 |
更新时间:2020-07-11 09:23:28
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】短周期元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子总数的3倍,Y原子的最外层只有2个电子,Z单质可制成半导体材料,W与X属于同一主族。下列叙述正确的是
| A.元素X的简单气态氢化物的热稳定性比W的强 |
| B.元素W的最高价氧化物对应水化物的酸性比Z的弱 |
| C.化合物YX、ZX2、WX3中化学键的类型相同 |
| D.原子半径的大小顺序:rZ>rY>rW>rX |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】如图是元素周期表的一部分,W、X、Y、Z为短周期主族元素,W、Z原子的最外层电子数之和等于11。下列说法错误的是
| W | X | ||
| Y | Z |
| A.四种元素中Y的原子半径最大 |
| B.非金属性强弱顺序为X>W>Y |
| C.高纯的Y单质可用于制作光感电池 |
| D.Z的氧化物的水化物酸性一定比W的强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】W、X、Y、Z四种元素在元素周期表中的相对位置如下图所示。W与Z的原子序数相差11,X的最外层电子数是内层的2倍。下列判断正确的是
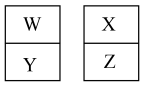
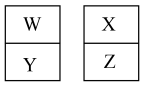
A.原子半径: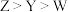 | B. 的最高正价为 的最高正价为 |
C.最高价氧化物对应的水化物的酸性: | D.W的单质在空气中燃烧生成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】元素周期表可以指导人们进行规律性的推测和判断,下列说法不正确的是
A.S和Se分别位于第ⅥA的第三、四周期,则氢化物的热稳定性: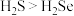 |
B.若 和 和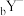 的核外电子层结构相同,则原子序数: 的核外电子层结构相同,则原子序数: |
| C.锗与硅位于金属元素与非金属元素的分界处,都能作半导体材料 |
D.常温下,水溶液的酸性: 可推断出元素的非金属性: 可推断出元素的非金属性: |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】YX4Z(WR4)2常用于抗酸、治疗慢性胃炎。它所含的五种元素均为短周期元素,基态R原子的价层电子排布式为nsnnp2n,R和W位于同主族,Y的最高价氧化物对应的水化物和其最简单氢化物能反应生成离子化合物,Z的周期序数和主族序数相等。下列叙述错误的是
| A.沸点:X2R<X2W |
| B.第一电离能:X<R<Y |
| C.Z元素的最高价氧化物为两性氧化物 |
| D.W元素最高价氧化物的水化物的浓溶液在常温下可以使铁钝化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】短周期元素X、Y、Z、W的原子序数依次增大,它们的原子最外层电子数为互不相等的奇数,且X、Y、W原子最外层电子数之和恰好等于Z元素的核电荷数,X与W的最高化合价之和为8。常见元素Z的单质是目前使用量最大的主族金属元素单质,下列说法中不正确的是
| A.因为Z的氧化物熔点很高,不适宜于电解,故工业上常用电解Z与W的化合物的方法制取单质Z |
| B.沸点:YX3>XW |
| C.化合物YW3遇水能强烈水解,产物之一具有强氧化性 |
| D.离子化合物YX5假如存在。该物质与水反应必然生成气体X2,同时得到一种弱碱溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列物质中既含有离子键又含有共价键的是
| A.KOH | B.CO2 | C.CaO | D.Cl2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
| A.H2O的热稳定性比H2S强,是因为H2O分子间作用力比H2S强 |
| B.离子化合物中一定含有离子键、一定不含共价键 |
| C.NaClO是含有两种类型化学键的离子化合物 |
| D.SiO2熔化破坏共价键和分子间作用力 |
您最近一年使用:0次

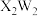 中阴阳离子的个数比为
中阴阳离子的个数比为

 在纸张漂白和废水处理等领域有重要应用。一定条件下用
在纸张漂白和废水处理等领域有重要应用。一定条件下用 和
和 合成
合成
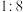
 的漂白原理相同
的漂白原理相同


