乙酰苯胺是一种白色有光泽片状结晶或白色结晶粉末,是磺胺类药物的原料, 可用作止痛剂、退热剂、防腐剂和染料中间体,乙酰苯胺的制备原理为: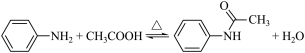 ,有关物质的性质如下表:
,有关物质的性质如下表:
注:刺形分馏柱的作用相当于二次蒸馏,用于沸点差别不太大的混合物的分离。

实验步骤:
步骤 1:在圆底烧瓶中加入无水苯胺 9.2 mL,冰醋酸 17.4 mL,锌粉 0.1 g,安装仪器, 加入沸石,调节加热温度,使分馏柱顶温度控制在 105℃ 左右,反应约 60~80 min,反应 生成的水及少量醋酸被蒸出。
步骤 2:在搅拌下,趁热将烧瓶中的物料以细流状倒入盛 100 mL 冰水的烧杯中,剧烈搅拌,并冷却,结晶,抽滤、洗涤、干燥,得到乙酰苯胺粗品。
步 骤 3:将此粗乙酰苯胺进行重结晶,晾干,称重,计算产率。
(1)仪器 a 的名称____________________ ;
(2)步骤 1 加热可用______________ (填“水浴”或“油浴”);
(3)制备过程中加入锌粒的作用:___________________ ;
(4)从化学平衡的角度分析,控制分馏柱上端的温度在 105℃左右的原因_______________________ ;
(5)乙酰苯胺粗品因含杂质而显色,欲用重结晶进行提纯,步骤如下:粗产品溶于沸水中配 成饱和溶液→再加入少量蒸馏水→加入活性炭脱色→加热煮沸→趁热过滤→________________ →过 滤→洗涤→干燥;
(6)该实验最终得到纯品 10.8g,则乙酰苯胺的产率是______________ ;
(7)如果重结晶过程中,加入活性炭过多,会造成产率下降,其可能原因为_________________ 。
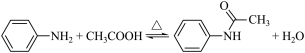 ,有关物质的性质如下表:
,有关物质的性质如下表:名称 | 式量 | 性状 | 密度/g·cm-3 | 沸点/℃ | 溶解度 | |
| 苯胺 | 93 | 无色油状液体,易氧化 | 1.02 | 184.4 | 微溶于水 | 易溶于乙醇、乙醚 |
| 乙酸 | 60 | 无色液体 | 1.05 | 118.1 | 易溶于水 | 易溶于乙醇、乙醚 |
| 乙酰苯胺 | 135 | 白色晶体 | 1.22 | 304 | 微溶于冷水,溶于热水 | 易溶于乙醇、乙醚 |
注:刺形分馏柱的作用相当于二次蒸馏,用于沸点差别不太大的混合物的分离。

实验步骤:
步骤 1:在圆底烧瓶中加入无水苯胺 9.2 mL,冰醋酸 17.4 mL,锌粉 0.1 g,安装仪器, 加入沸石,调节加热温度,使分馏柱顶温度控制在 105℃ 左右,反应约 60~80 min,反应 生成的水及少量醋酸被蒸出。
步骤 2:在搅拌下,趁热将烧瓶中的物料以细流状倒入盛 100 mL 冰水的烧杯中,剧烈搅拌,并冷却,结晶,抽滤、洗涤、干燥,得到乙酰苯胺粗品。
步 骤 3:将此粗乙酰苯胺进行重结晶,晾干,称重,计算产率。
(1)仪器 a 的名称
(2)步骤 1 加热可用
(3)制备过程中加入锌粒的作用:
(4)从化学平衡的角度分析,控制分馏柱上端的温度在 105℃左右的原因
(5)乙酰苯胺粗品因含杂质而显色,欲用重结晶进行提纯,步骤如下:粗产品溶于沸水中配 成饱和溶液→再加入少量蒸馏水→加入活性炭脱色→加热煮沸→趁热过滤→
(6)该实验最终得到纯品 10.8g,则乙酰苯胺的产率是
(7)如果重结晶过程中,加入活性炭过多,会造成产率下降,其可能原因为
更新时间:2020-07-14 11:16:59
|
相似题推荐
解答题-有机推断题
|
适中
(0.65)
名校
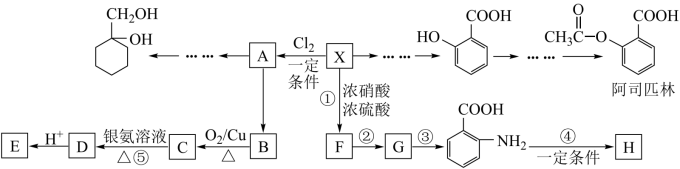
【推荐1】某芳香烃X(C7H8)是一种重要的有机化工原料,研究部门以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去)。其中A是一氯代物,H是一种功能高分子,链节组成为C7H5NO。
(1)X的结构简式为_______ ;F的名称为_______ 。
(2)反应②的反应类型属于_______ 。C中官能团的名称是_______ 。
(3)反应④的化学方程式为_______ 。
(4)阿司匹林(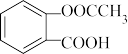 )有多种同分异构体,其中属于二元酸的芳香族化合物共有
)有多种同分异构体,其中属于二元酸的芳香族化合物共有_______ 种;核磁共振氢谱有4组峰,峰值面积比为3∶2∶2∶1的结构简式为_______ (写一种即可)。
(5)请用合成反应流程图表示出由有机物A和其他无机物合成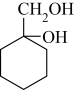 最合理的方案(不超过4步),合成路线为
最合理的方案(不超过4步),合成路线为_______ 。
已知:I.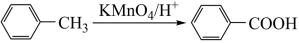
Ⅱ. 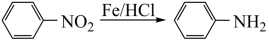 (苯胺,易被氧化)
(苯胺,易被氧化)
(1)X的结构简式为
(2)反应②的反应类型属于
(3)反应④的化学方程式为
(4)阿司匹林(
 )有多种同分异构体,其中属于二元酸的芳香族化合物共有
)有多种同分异构体,其中属于二元酸的芳香族化合物共有(5)请用合成反应流程图表示出由有机物A和其他无机物合成
 最合理的方案(不超过4步),合成路线为
最合理的方案(不超过4步),合成路线为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐2】阿莫西林是一种最常用的半合成青霉素类广谱β-内酰胺类抗生素,某研究小组按下列路 线合成:

已知:

请回答:
(1)B 的结构简式为_____ 。
(2)下列说法正确的是_____ 。
A 化合物 B 的官能团是醛基 B 反应①的目的是为了保护酚羟基
C 化合物 D 能发生消去反应D 阿莫西林的分子式是 C16H19N3O5S
(3)写出第⑨步反应的化学反应方程式_____ 。
(4)设计以 为原料制备水杨酸(
为原料制备水杨酸( )的合成路线 (用流程图表示,无机试剂任选)
)的合成路线 (用流程图表示,无机试剂任选)_____ 。
(5)写出同时符合下列条件的 F 的所有同分异构体的结构简式_____ 。
①分子中有苯环且是苯环的对位二取代物
②分子中含有硝基且不与苯环直接相连
③分子不与金属钠反应放出氢气

已知:

请回答:
(1)B 的结构简式为
(2)下列说法正确的是
A 化合物 B 的官能团是醛基 B 反应①的目的是为了保护酚羟基
C 化合物 D 能发生消去反应D 阿莫西林的分子式是 C16H19N3O5S
(3)写出第⑨步反应的化学反应方程式
(4)设计以
 为原料制备水杨酸(
为原料制备水杨酸( )的合成路线 (用流程图表示,无机试剂任选)
)的合成路线 (用流程图表示,无机试剂任选)(5)写出同时符合下列条件的 F 的所有同分异构体的结构简式
①分子中有苯环且是苯环的对位二取代物
②分子中含有硝基且不与苯环直接相连
③分子不与金属钠反应放出氢气
您最近一年使用:0次
【推荐3】糖类、油脂和蛋白质都是生命中重要的有机物质。
(1)淀粉在硫酸作用下发生水解反应,证明淀粉水解产物中含有醛基:

试剂X为___________ ,试管C的实验现象为___________ 。
(2)某油脂A的结构简式为 。从酯的性质看,油脂A在酸性条件下和碱性条件下均能发生水解,水解的共同产物是
。从酯的性质看,油脂A在酸性条件下和碱性条件下均能发生水解,水解的共同产物是___________ (写结构简式)
(3)蛋白质可以与甲醛作用,该过程称为蛋白质的___________ 。
(4)天然蛋白质水解生成的最简单的氨基酸是甘氨酸,该氨基酸形成的二肽的结构简式是___________ 。
(5)聚丙烯酸钠、涤纶的结构简式如图:

合成聚丙烯酸钠的单体的结构简式是___________ ;合成涤纶有两种单体;其中能和 反应的单体的结构简式是
反应的单体的结构简式是___________ 。
(1)淀粉在硫酸作用下发生水解反应,证明淀粉水解产物中含有醛基:

试剂X为
(2)某油脂A的结构简式为
 。从酯的性质看,油脂A在酸性条件下和碱性条件下均能发生水解,水解的共同产物是
。从酯的性质看,油脂A在酸性条件下和碱性条件下均能发生水解,水解的共同产物是(3)蛋白质可以与甲醛作用,该过程称为蛋白质的
(4)天然蛋白质水解生成的最简单的氨基酸是甘氨酸,该氨基酸形成的二肽的结构简式是
(5)聚丙烯酸钠、涤纶的结构简式如图:

合成聚丙烯酸钠的单体的结构简式是
 反应的单体的结构简式是
反应的单体的结构简式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】环己烯是重要的化工原料。其实验室制备流程如下:
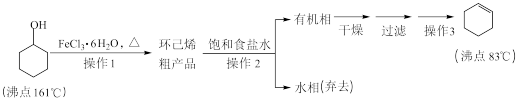
回答下列问题:
Ⅰ.环己烯的制备与提纯
(1)原料环己醇中若含苯酚杂质,检验试剂为__________ ,现象为____________ 。
(2)操作1的装置如图所示(加热和夹持装置已略去)。
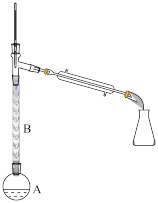
①烧瓶A中进行的可逆反应化学方程式为__________________________________ ,浓硫酸也可作该反应的催化剂,选择FeCl3·6H2O而不用浓硫酸的原因为___________ (填序号)。
a.浓硫酸易使原料炭化并产生SO2
b.FeCl3·6H2O污染小、可循环使用,符合绿色化学理念
c.同等条件下,用FeCl3·6H2O比浓硫酸的平衡转化率高
②仪器B的作用为____________________________ 。
(3)操作2用到的玻璃仪器是__________________________ 。
Ⅱ.环己烯含量的测定
在一定条件下,向a g环己烯样品中加入定量制得的b mol Br2,与环己烯充分反应后,剩余的Br2与足量KI作用生成I2,用c mol·L-1的Na2S2O3标准溶液滴定,终点时消耗Na2S2O3标准溶液V mL(以上数据均已扣除干扰因素)。
测定过程中,发生的反应如下:
①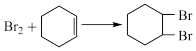
②Br2+2KI=I2+2KBr
③I2+2Na2S2O3=2NaI+Na2S4O6
(4)滴定所用指示剂为__________________________ 。样品中环己烯的质量分数为______________________ (用字母表示)。
(5)下列情况会导致测定结果偏低的是__________________ (填序号)。
a.样品中含有苯酚杂质
b.在测定过程中部分环己烯挥发
c.Na2S2O3标准溶液部分被氧化

回答下列问题:
Ⅰ.环己烯的制备与提纯
(1)原料环己醇中若含苯酚杂质,检验试剂为
(2)操作1的装置如图所示(加热和夹持装置已略去)。

①烧瓶A中进行的可逆反应化学方程式为
a.浓硫酸易使原料炭化并产生SO2
b.FeCl3·6H2O污染小、可循环使用,符合绿色化学理念
c.同等条件下,用FeCl3·6H2O比浓硫酸的平衡转化率高
②仪器B的作用为
(3)操作2用到的玻璃仪器是
Ⅱ.环己烯含量的测定
在一定条件下,向a g环己烯样品中加入定量制得的b mol Br2,与环己烯充分反应后,剩余的Br2与足量KI作用生成I2,用c mol·L-1的Na2S2O3标准溶液滴定,终点时消耗Na2S2O3标准溶液V mL(以上数据均已扣除干扰因素)。
测定过程中,发生的反应如下:
①

②Br2+2KI=I2+2KBr
③I2+2Na2S2O3=2NaI+Na2S4O6
(4)滴定所用指示剂为
(5)下列情况会导致测定结果偏低的是
a.样品中含有苯酚杂质
b.在测定过程中部分环己烯挥发
c.Na2S2O3标准溶液部分被氧化
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】二氯化二硫(S2Cl2)在工业上有着广泛的用途。已知S2Cl2的熔点为-80℃,沸点为138℃。S2Cl2遇水剧烈反应会生成黄色单质、一种能使品红溶液褪色的气体化合物及酸雾,在工业中可由硫和氯气在100~110℃直接化合而成。某小组在实验室用以下装置制备S2Cl2并对尾气进行回收利用。
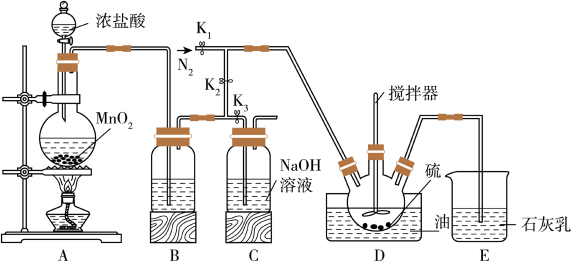
回答下列问题:
(1)S2Cl2的结构式是______ 。S2Cl2与水反应时氧化剂与还原剂的物质的量之比是______ 。
(2)A装置中发生反应的离子方程式是___________ 。B中所装试剂为________ 。
(3)通入N2的目的是___________________ 。
(4)D装置需要油浴加热,为什么不采用水浴加热?原因是_____________ 。搅拌器搅拌的作用是____________ 。
(5)装置E的作用是____________ 。
(6)上述装置制得的二氯化二硫可能不纯,其原因是____________________ ,改进的措施是______________ 。

回答下列问题:
(1)S2Cl2的结构式是
(2)A装置中发生反应的离子方程式是
(3)通入N2的目的是
(4)D装置需要油浴加热,为什么不采用水浴加热?原因是
(5)装置E的作用是
(6)上述装置制得的二氯化二硫可能不纯,其原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】工业上可以利用氟硅酸(H2SiF6)、碳酸氢铵制造冰晶石(Na3AlF6),其工艺流程如下:
请回答下列问题:

(1)反应①中生成的气体A是________ ,滤液①的溶质是________ 。
(2)冰晶石在工业冶炼铝中做助熔剂,写出工业冶炼铝的方程式_____ 。
(3)写出反应②的化学方程式_________ 。
(4)反应②后,过滤得到冰晶石固体,需要在_____ (填装置的名称)中洗涤,请用实验证明冰晶石固体已经洗涤干净__________ 。
(5)温度和c(NH4HCO3)会影响反应①的速率。现设计如下实验方案探究温度和c(NH4HCO3)对反应①速率的影响。请在表格空白处填写适当的反应条件
(6)下图是滤液①溶质的质量分数随温度变化的曲线图:分析t2℃时,滤液①中溶质的质量分数下降的原因_____ 。

请回答下列问题:

(1)反应①中生成的气体A是
(2)冰晶石在工业冶炼铝中做助熔剂,写出工业冶炼铝的方程式
(3)写出反应②的化学方程式
(4)反应②后,过滤得到冰晶石固体,需要在
(5)温度和c(NH4HCO3)会影响反应①的速率。现设计如下实验方案探究温度和c(NH4HCO3)对反应①速率的影响。请在表格空白处填写适当的反应条件
| 实验编号 | 实验目的 | 温度 | c(NH4HCO3) |
| Ⅰ | 为以下实验做参照 | 60℃ | c1 |
| Ⅱ | 探究浓度对反应①速率的影响 | c2 | |
| Ⅲ | 探究温度对反应①速率的影响 | 80℃ |

您最近一年使用:0次



