下列有关物质性质的比较错误的是
| A.熔点:MgO>CaO>KCl | B.沸点:AsH3>PH3>NH3 |
| C.离子半径:S2->Cl->Ca2+ | D.稳定性:H2O>H2S>H2Se |
更新时间:2020-07-16 07:09:40
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列关于硼、硅及其化合物的说法中错误的是
| A.可用H3BO3溶液来中和溅在皮肤上的碱液 |
| B.Si与HF的反应中体现了HF的还原性 |
| C.B2O3熔融时可以与多种碱性氧化物反应 |
| D.Na2SiO3溶液可用作木材防火剂和黏合剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列各组顺序的排列错误的是
| A.半径:F—>Na+>Mg2+>Al3+ |
| B.沸点:H2O<H2S<H2Se |
| C.酸性:HClO4>H2SO4>H3PO4 |
| D.熔点:SiO2>NaCl>CO2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列关于物质结构和元素性质说法正确的是
| A.非金属元素之间形成的化合物一定是共价化合物 |
| B.乙醇可与水以任意比例混溶,是因为与水形成氢键 |
| C.IA族与VIIA族元素原子之间形成的化学键是离子键 |
| D.同主族元素的简单阴离子还原性越强,水解程度越大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法都正确的是
①CO和N2互为等电子体,且前者沸点低于后者;
②CH3-CH2-CH2-CH3和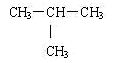 互为同分异构体,且前者熔沸点高于后者;
互为同分异构体,且前者熔沸点高于后者;
③BF3和NH3化学键的类型和分子的极性皆相同;
④F的电负性大于O,但H2O的熔沸点比HF高;
⑤CsCl晶格能小于NaCl;
⑥简单立方堆积和面心立方堆积是由非密置层堆积形成的;
①CO和N2互为等电子体,且前者沸点低于后者;
②CH3-CH2-CH2-CH3和
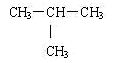 互为同分异构体,且前者熔沸点高于后者;
互为同分异构体,且前者熔沸点高于后者;③BF3和NH3化学键的类型和分子的极性皆相同;
④F的电负性大于O,但H2O的熔沸点比HF高;
⑤CsCl晶格能小于NaCl;
⑥简单立方堆积和面心立方堆积是由非密置层堆积形成的;
| A.①④⑥ | B.③④⑤ | C.②④⑤ | D.②④⑥ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】晶格能能反映离子晶体的稳定性。与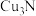 有关的转化如图所示,下列关于晶格能的叙述正确的是
有关的转化如图所示,下列关于晶格能的叙述正确的是
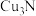 有关的转化如图所示,下列关于晶格能的叙述正确的是
有关的转化如图所示,下列关于晶格能的叙述正确的是
| A.晶格能是指相邻的离子间的静电作用 |
| B.岩浆冷却时,晶格能大的矿物后结晶析出 |
| C.工业上通过电解熔融氯化镁制镁,而不用氧化镁,与晶格能有关 |
D.由图可知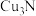 的晶格能为 的晶格能为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】表中原子化热、晶格能、键能的单位都是kJ·mol-1
则下列说法正确的是
| 金属 | 金属原子化热 | 离子化合物 | 晶格能 | 共价键 | 键能 |
| Na | 108.4 | NaCl | 786 | Cl-Cl | 243 |
| Mg | 146.4 | NaBr | 747 | Si-Si | 176 |
| Al | 326.4 | MgO | 3791 | Si-Cl | 360 |
则下列说法正确的是
| A.Na(s)与Cl2(g)反应生成1molNaCl(s)放出的热量为556.1kJ |
| B.Si(s)+2Cl2(g)=SiCl4(g) △H= -602kJ·mol-1 |
| C.从表中可以看出,氯化钠的熔点比晶体硅高 |
| D.从表中数据可以看出,微粒半径越大金属键、离子键的越弱,而共价键却越强 |
您最近一年使用:0次

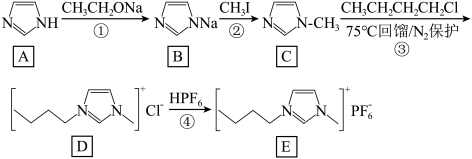


 的能力比另一个N弱
的能力比另一个N弱

