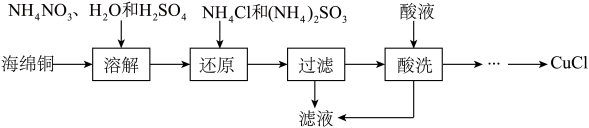
氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl微溶于水,不溶于稀酸,可溶于Cl-浓度较大的体系,在潮湿的空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料,采用硝酸铵氧化分解技术生产CuCl的工艺过程如下:
(1)基态铜原子核外电子排布式为:________ 。
(2)为了提高溶解速率,可以适当加热到60~70℃,还可以采用的措施为________ 。
(3)溶解步骤的温度控制在60~70℃,温度不宜过高的原因是________ 。该步骤中Cu 与NH4NO3反应的离子方程式为 (N元素被还原到最低价)_________________ 。
(4)还原步骤发生反应的离子方程式为______________________ 。
(5)滤液的主要成分为__________ (写化学式)。
(6)酸洗时,可选用稀硫酸或稀盐酸,但不能用浓盐酸的原因是_________________ 。

(1)基态铜原子核外电子排布式为:
(2)为了提高溶解速率,可以适当加热到60~70℃,还可以采用的措施为
(3)溶解步骤的温度控制在60~70℃,温度不宜过高的原因是
(4)还原步骤发生反应的离子方程式为
(5)滤液的主要成分为
(6)酸洗时,可选用稀硫酸或稀盐酸,但不能用浓盐酸的原因是
更新时间:2020-07-16 12:33:14
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】化合物X由三种元素组成,可用于医药、火箭推进剂等,某兴趣小组按如下流程进行实验:
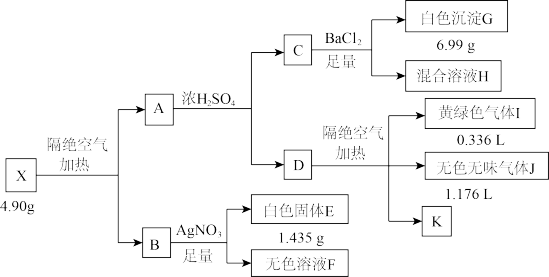
已知:X与A组成元素相同,I为单质,C与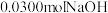 恰好中和,透过蓝色钴玻璃观察F焰色呈紫色,J能使带火星的木条复燃,K为常见无色液体,气体体积均在标准状况下测定。
恰好中和,透过蓝色钴玻璃观察F焰色呈紫色,J能使带火星的木条复燃,K为常见无色液体,气体体积均在标准状况下测定。
请回答:
(1)X的组成元素是___________ ,X的化学式是___________ 。
(2)写出D分解的化学反应方程式___________ 。
(3)电解X的水溶液可制备A,写出该反应的离子方程式___________ 。
(4)设计实验检验溶液F中的阴离子___________ 。

已知:X与A组成元素相同,I为单质,C与
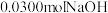 恰好中和,透过蓝色钴玻璃观察F焰色呈紫色,J能使带火星的木条复燃,K为常见无色液体,气体体积均在标准状况下测定。
恰好中和,透过蓝色钴玻璃观察F焰色呈紫色,J能使带火星的木条复燃,K为常见无色液体,气体体积均在标准状况下测定。请回答:
(1)X的组成元素是
(2)写出D分解的化学反应方程式
(3)电解X的水溶液可制备A,写出该反应的离子方程式
(4)设计实验检验溶液F中的阴离子
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某化学自主实验小组利用如图所示装置探究NO2能否被NH3还原(K1、K2为止水夹,夹持固定装置略去)。
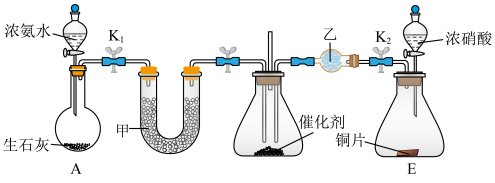
(1)A装置发生的化学反应方程式为_______ 。E装置发生的化学反应方程式为_______ 。
(2)甲、乙分别是_______ (填标号)。
a.硫酸、浓硫酸 b.碱石灰、无水氯化钙
c.碱石灰、碱石灰 d.五氧化二磷、五氧化二磷
(3)请写NH3与O2在催化剂Pt作用下的反应方程式_______ ,该反应中还原剂为_______
(4)若NO2能够被NH3还原,写出发生反应的化学方程式:_______ 。
(5)此实验装置存在一个明显的缺陷是_______ 。

(1)A装置发生的化学反应方程式为
(2)甲、乙分别是
a.硫酸、浓硫酸 b.碱石灰、无水氯化钙
c.碱石灰、碱石灰 d.五氧化二磷、五氧化二磷
(3)请写NH3与O2在催化剂Pt作用下的反应方程式
(4)若NO2能够被NH3还原,写出发生反应的化学方程式:
(5)此实验装置存在一个明显的缺陷是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
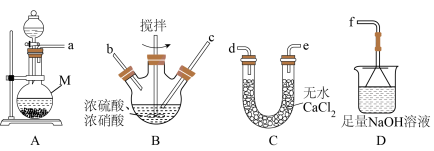
【推荐3】亚硝酰硫酸(NOSO4H)主要用于染料、医疗领域。实验室用如图装置(略去部分夹持装置)制备少量亚硝酰硫酸,并测定产品的纯度。
ii.实验室用浓硫酸、浓硝酸的混合液与SO2反应制备亚硝酰硫酸,原理为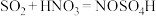 。
。
(1)仪器M的名称为____________ 。
(2)用Na2SO3和70%H2SO4在装置A中制取SO2气体时,发生反应的化学方程式为___________ 。
(3)按气流从左到右的顺序,上述仪器的连接顺序为a→___________ →f。(填仪器接口字母,部分仪器可以重复使用)
(4)为了控制通入B中的SO2的速率,可以采取的措施是__________ 。
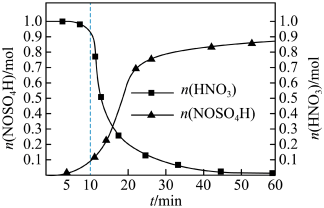
(5)反应过程中,NOSO4H的物质的量和HNO3的物质的量随时间的变化关系如图所示。__________ 。
(6)测定NOSO4H产品的纯度。
准确称取2.5g产品放入锥形瓶中,加入50mL0.20mol·L-1KMnO4标准溶液和足量稀硫酸,摇匀,待充分反应后将反应后的溶液加热,使生成的硝酸全部挥发逸出(不考虑硝酸的分解),冷却至室温,用0.5mol·L-1Na2C2O4标准溶液滴定至终点,消耗Na2C2O4标准溶液的体积为18.00mL。
已知:高锰酸钾可将亚硝酰硫酸氧化为HNO3,自身被还原为Mn2+。
①滴定终点的现象为__________ 。
②亚硝酰硫酸的纯度为__________ %。
ii.实验室用浓硫酸、浓硝酸的混合液与SO2反应制备亚硝酰硫酸,原理为
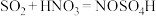 。
。(1)仪器M的名称为
(2)用Na2SO3和70%H2SO4在装置A中制取SO2气体时,发生反应的化学方程式为
(3)按气流从左到右的顺序,上述仪器的连接顺序为a→
(4)为了控制通入B中的SO2的速率,可以采取的措施是
(5)反应过程中,NOSO4H的物质的量和HNO3的物质的量随时间的变化关系如图所示。
(6)测定NOSO4H产品的纯度。
准确称取2.5g产品放入锥形瓶中,加入50mL0.20mol·L-1KMnO4标准溶液和足量稀硫酸,摇匀,待充分反应后将反应后的溶液加热,使生成的硝酸全部挥发逸出(不考虑硝酸的分解),冷却至室温,用0.5mol·L-1Na2C2O4标准溶液滴定至终点,消耗Na2C2O4标准溶液的体积为18.00mL。
已知:高锰酸钾可将亚硝酰硫酸氧化为HNO3,自身被还原为Mn2+。
①滴定终点的现象为
②亚硝酰硫酸的纯度为
您最近一年使用:0次
【推荐1】已知A、B、C、D均为化合物,B、C常温常压下为气体,C气体可使湿润的红色石蕊试纸变蓝色;又知1mol A在200℃时分解仅得1mol B和一定量的水两种产物,A中含有NO 。A、B、C、D间有如图关系:
。A、B、C、D间有如图关系:
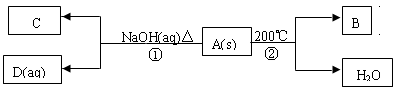
试回答下列问题:
(1)写出A、C的化学式:A_______ ;C_______ 。
(2)写出反应①的离子方程式:_______ 。
(3)写出反应②的化学方程式:_______ 。
 。A、B、C、D间有如图关系:
。A、B、C、D间有如图关系:
试回答下列问题:
(1)写出A、C的化学式:A
(2)写出反应①的离子方程式:
(3)写出反应②的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
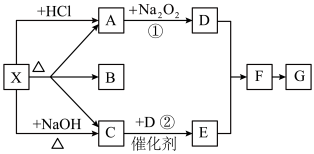
【推荐2】几种常见物质的转化关系如下图所示,图中每一方格表示有关的一种反应物或生成物,其中A、C为无色气体。
(1)物质X可以是_____ ,C是_____ ,F是_____ 。
(2)反应②的化学方程式是_______ 。
(1)物质X可以是
(2)反应②的化学方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】锰铁氧体软磁材料(Fe2O3-MnO)可广泛应用在信息通讯等领域。用软锰矿(主要成分 ,含
,含 、FeO、
、FeO、 、
、 杂质)为主要原料制备锰铁氧体软磁材料的工艺流程如下。
杂质)为主要原料制备锰铁氧体软磁材料的工艺流程如下。
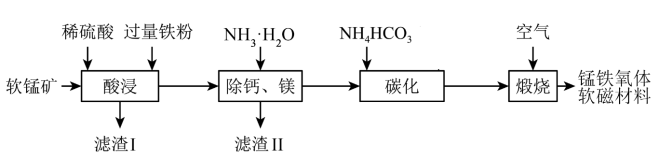
回答下列问题:
(1)滤渣I的主要成分是_______ 。
(2)“酸浸”过程中加入过量铁粉的主要目的是将 还原为
还原为 、
、_______ 。
(3)“碳化”中生成碳酸锰沉淀的离子方程式为_______ 。
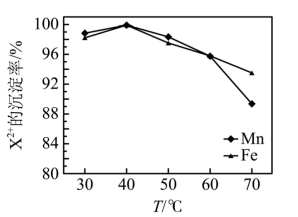
(4)“碳化”时,金属阳离子 的沉淀率与温度关系如图所示。为了使
的沉淀率与温度关系如图所示。为了使 沉淀完全,最适宜的温度是
沉淀完全,最适宜的温度是_____ 。“碳化”过程需加入过量的 ,除了使
,除了使 沉淀完全外,另一原因是
沉淀完全外,另一原因是____ 。
(5)“煅烧”时,碳酸亚铁发生反应的化学方程式为_______ 。
 ,含
,含 、FeO、
、FeO、 、
、 杂质)为主要原料制备锰铁氧体软磁材料的工艺流程如下。
杂质)为主要原料制备锰铁氧体软磁材料的工艺流程如下。
回答下列问题:
(1)滤渣I的主要成分是
(2)“酸浸”过程中加入过量铁粉的主要目的是将
 还原为
还原为 、
、(3)“碳化”中生成碳酸锰沉淀的离子方程式为
(4)“碳化”时,金属阳离子
 的沉淀率与温度关系如图所示。为了使
的沉淀率与温度关系如图所示。为了使 沉淀完全,最适宜的温度是
沉淀完全,最适宜的温度是 ,除了使
,除了使 沉淀完全外,另一原因是
沉淀完全外,另一原因是
(5)“煅烧”时,碳酸亚铁发生反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某校化学实验课上,老师要求学生用硫酸铜溶液与氢氧化钠溶液制备Cu(OH)2,为了缩短实验时间,老师让学生将反应容器放在沸水浴中进行反应,结果出现了如下两种不同的实验现象:
(1)甲同学认为实验一中产生的黑色沉淀是___ (填化学式),理由是___ 。
(2)为验证推测结果是否正确,甲同学将黑色沉淀过滤、洗涤、干燥后称得质量为ag,并按照如图所示装置进行实验,实验前后称得干燥管E的质量分别为cg和dg。
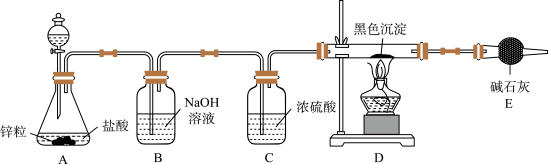
为确保实验的准确性,甲同学认为应在装置A反应一段时间后再接上装置E,点燃D中的酒精灯,其理由是___ 。乙同学认为甲同学的装置仍有不足,应在E的末端连接一个气囊,气囊的作用有两个:___ 。甲同学改进实验装置后完成实验,若a、c、d满足关系式:___ ,则证明甲同学对黑色沉淀的推测是正确的。
(3)丙同学认为实验二中的蓝色沉淀应为Cu(OH)2,丁同学立即提出反对意见,认为该蓝色沉淀一定不是Cu(OH)2。为确认实验二中蓝色沉淀的成分,丁同学从实验时药品的加入顺序考虑,可能是反应物的用量不同导致产物的不同,并上网查阅资料知,当NaOH溶液少量时会生成碱式硫酸铜[Cu2(OH)2SO4],反应的离子方程式为___ 。
(4)进一步查阅资料可知碱式硫酸铜为蓝色物质,难溶于水、可溶于酸。请你设计实验,验证实验二中生成的蓝色沉淀含有SO42-:___ 。
| 操作 | 现象 | |
| 实验一 | 向NaOH溶液中滴加CuSO4溶液 | 黑色沉淀 |
| 实验二 | 向CuSO4溶液中滴加NaOH溶液 | 蓝色沉淀 |
(2)为验证推测结果是否正确,甲同学将黑色沉淀过滤、洗涤、干燥后称得质量为ag,并按照如图所示装置进行实验,实验前后称得干燥管E的质量分别为cg和dg。

为确保实验的准确性,甲同学认为应在装置A反应一段时间后再接上装置E,点燃D中的酒精灯,其理由是
(3)丙同学认为实验二中的蓝色沉淀应为Cu(OH)2,丁同学立即提出反对意见,认为该蓝色沉淀一定不是Cu(OH)2。为确认实验二中蓝色沉淀的成分,丁同学从实验时药品的加入顺序考虑,可能是反应物的用量不同导致产物的不同,并上网查阅资料知,当NaOH溶液少量时会生成碱式硫酸铜[Cu2(OH)2SO4],反应的离子方程式为
(4)进一步查阅资料可知碱式硫酸铜为蓝色物质,难溶于水、可溶于酸。请你设计实验,验证实验二中生成的蓝色沉淀含有SO42-:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
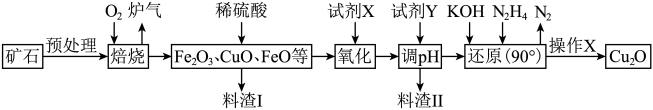
【推荐2】氧化亚铜(Cu2O)是一种用途广泛的光电材料,某工厂以硫化铜矿石(含CuFeS2、Cu2S等)为原料制取Cu2O的工艺流程如下:
常温下几种物质开始形成沉淀与完全沉淀时的pH如下表
(1)炉气中的有害气体成分是__________ ,Cu2S与O2反应时,氧化剂与还原剂的物质的量之比为__________ 。
(2)若试剂X是H2O2溶液,写出相应反应的离子方程式:__________ 。并写出H2O2的电子式__________ ,Fe(铁)在元素周期表中的位置:__________ ;当试剂X是__________ 时,更有利于降低生产成本。
(3)加入试剂Y调pH时,pH的调控范围是__________ 。
(4)操作X包括__________ 、洗涤、烘干,其中烘干时要隔绝空气,其目的是__________ 。
(5)以铜与石墨作电极,电解浓的强碱性溶液可制得纳米级Cu2O,写出阳极上生成Cu2O的电极反应式:__________ 。

常温下几种物质开始形成沉淀与完全沉淀时的pH如下表
| Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
| 开始沉淀 | 7.5 | 2.7 | 4.8 |
| 完全沉淀 | 9.0 | 3.7 | 6.4 |
(1)炉气中的有害气体成分是
(2)若试剂X是H2O2溶液,写出相应反应的离子方程式:
(3)加入试剂Y调pH时,pH的调控范围是
(4)操作X包括
(5)以铜与石墨作电极,电解浓的强碱性溶液可制得纳米级Cu2O,写出阳极上生成Cu2O的电极反应式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】已知①胆矾(CuSO4·5H2O)易溶于水,难溶于乙醇;②溶液中Fe3+和Cu2+完全沉淀时的pH分别为3.7和6.9,某小组用工业废铜焙烧得到的CuO(杂质为氧化铁及泥沙)为原料与稀硫酸反应制备胆矾,并测定其结晶水的含量。回答下列问题:
(1)将CuO加入到适量的稀硫酸中,加热,其主要反应的化学方程式为___ 。与直接用废铜和浓硫酸反应相比,该方法的优点是___ 。
(2)待CuO完全反应后停止加热,边搅拌边加入适量H2O2,冷却后用NH3·H2O调pH为3.5~4.0,再煮沸10min,冷却后过滤。滤液经如下实验操作:加热蒸发、冷却结晶、__ 、乙醇洗涤、__ ,得到胆矾。其中,控制溶液pH为3.5~4.0的目的是__ 。
(3)制备胆矾时,用到的实验仪器除量筒、酒精灯、玻璃棒、漏斗外,还必须使用的仪器有__ (填标号)。
(4)结晶水含量测定(设化学式为CuSO4·xH2O):称量干燥坩埚的质量为m1,加入胆矾后总质量为m2,将坩埚加热至胆矾全部变为白色,置于干燥器中冷至室温后称量,重复上述操作,最终总质量恒定为m3。根据实验数据可知,x=__ (写表达式)。
(5)下列操作中,会导致结晶水含量测定值偏高的是__ (填标号)。
①胆矾未充分干燥
②坩埚未置于干燥器中冷却
③加热时有少胆矾迸溅出来
(1)将CuO加入到适量的稀硫酸中,加热,其主要反应的化学方程式为
(2)待CuO完全反应后停止加热,边搅拌边加入适量H2O2,冷却后用NH3·H2O调pH为3.5~4.0,再煮沸10min,冷却后过滤。滤液经如下实验操作:加热蒸发、冷却结晶、
(3)制备胆矾时,用到的实验仪器除量筒、酒精灯、玻璃棒、漏斗外,还必须使用的仪器有
| A.烧杯 | B.容量瓶 | C.蒸发皿 | D.坩埚 |
(5)下列操作中,会导致结晶水含量测定值偏高的是
①胆矾未充分干燥
②坩埚未置于干燥器中冷却
③加热时有少胆矾迸溅出来
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】用废雷尼镍(主要成分为NiO、Al,少量Cr、Fe、C、S 及有机物)制备Ni(NO3)2·6H2O的实验流程如下:

已知:①在实验条件下,Ni2+、Cr3+在溶液中不能被NaClO或HNO3氧化。
②NiSO4易溶于水,NiCO3难溶于水;Ni(NO3)2在20℃、90℃时溶解度依次为79.2、188g/100g 水。
③已知“酸溶”后的溶液中主要的四种离子开始沉淀与沉淀完全的pH 如下:
(1)“除铝”所用试剂及主要操作为__________ 。
(2)“灼烧”的主要目的是__________ 。
(3)“酸溶” 时,用浓硫酸和水代替稀硫酸的目的是__________ 。
(4)“除铁、铬”时,Fe2+被氧化为Fe3+的离子方程式为__________ ;氧化后需将溶液 pH调整到的范围是__________ 。
(5)请设计由“净化液”制取Ni(NO3)2·6H2O的实验方案:__________ ,离心分离、洗涤、干燥得Ni(NO3)2·6H2O (实验中须使用的试剂有:6mol·L-1硝酸,3 mol·L-1Na2CO3溶液)。

已知:①在实验条件下,Ni2+、Cr3+在溶液中不能被NaClO或HNO3氧化。
②NiSO4易溶于水,NiCO3难溶于水;Ni(NO3)2在20℃、90℃时溶解度依次为79.2、188g/100g 水。
③已知“酸溶”后的溶液中主要的四种离子开始沉淀与沉淀完全的pH 如下:
| Ni2+ | Fe2+ | Fe3+ | Cr3+ | |
| 开始沉淀pH | 6.2 | 7.6 | 2.3 | 4.5 |
| 沉淀完全pH | 8.5 | 9.1 | 3.3 | 5.6 |
(2)“灼烧”的主要目的是
(3)“酸溶” 时,用浓硫酸和水代替稀硫酸的目的是
(4)“除铁、铬”时,Fe2+被氧化为Fe3+的离子方程式为
(5)请设计由“净化液”制取Ni(NO3)2·6H2O的实验方案:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
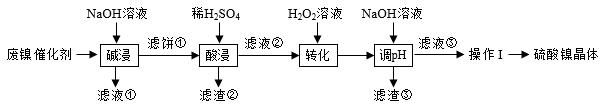
【推荐2】某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其它不溶性物质。采用如图工艺流程回收其中的镍制备硫酸镍晶体(NiSO4·7H2O):
溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
回答下列问题:
(1)“碱浸”中NaOH的两个作用分别是①溶解铝及其化合物,②_______ 。
(2)“滤液②”中含有的金属离子有_______ 。
(3)“转化”中发生的离子方程式为_______ ,若工艺流程改为先“调pH”后“转化”,即:如下操作:
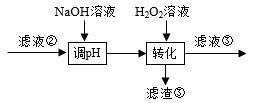
“滤液③”中可能含有的杂质离子为_______ 。
(4)“转化”后加NaOH溶液“调pH”应控制的pH范围是_______ ;操作Ⅰ的具体操作是_______ ,过滤,洗涤,干燥。
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式_______ 。

溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
| 金属离子 | Ni2+ | Al3+ | Fe3+ | Fe2+ |
| 开始沉淀时的pH | 6.2 | 3.7 | 2.2 | 7.5 |
| 沉淀完全时的pH | 8.7 | 4.7 | 3.2 | 9.0 |
回答下列问题:
(1)“碱浸”中NaOH的两个作用分别是①溶解铝及其化合物,②
(2)“滤液②”中含有的金属离子有
(3)“转化”中发生的离子方程式为

“滤液③”中可能含有的杂质离子为
(4)“转化”后加NaOH溶液“调pH”应控制的pH范围是
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】一种以镉废渣(含CdO及少量ZnO、CuO、MnO、FeO杂质)为原料制备镉的工艺流程如下:
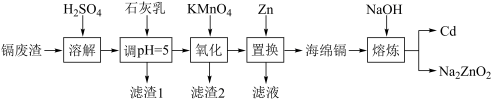
(1)基态Zn2+核外电子排布式为___________ 。
(2)“滤渣2”的主要成分是MnO2、Fe(OH)3。“氧化”过程中KMnO4与Mn2+发生反应的离子方程式为___________ 。
(3)“置换”过程中镉置换率与(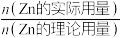 )的关系如图1所示,其中Zn的理论用量以溶液中
)的关系如图1所示,其中Zn的理论用量以溶液中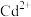 的物质的量为依据。实际生产中
的物质的量为依据。实际生产中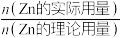 最佳比值为1.3,不宜超过该比值的原因是
最佳比值为1.3,不宜超过该比值的原因是___________ 。
(4)向“置换”所得滤液中加 溶液,经沉淀、过滤、洗涤等系列操作后,得到碱式碳酸锌[化学式为
溶液,经沉淀、过滤、洗涤等系列操作后,得到碱式碳酸锌[化学式为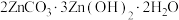 ,摩尔质量为583g/mol]
,摩尔质量为583g/mol]
①碱式碳酸锌高温下完全分解至质量不变的反应方程式为___________ 。
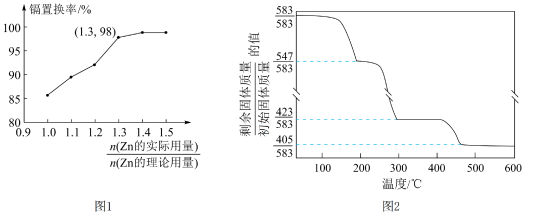
②碱式碳酸锌加热升温过程中固体的质量变化如图2所示。350℃时剩余固体中已不含碳元素,则350℃时剩余固体的成分为___________ 。(填化学式)

(1)基态Zn2+核外电子排布式为
(2)“滤渣2”的主要成分是MnO2、Fe(OH)3。“氧化”过程中KMnO4与Mn2+发生反应的离子方程式为
(3)“置换”过程中镉置换率与(
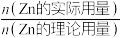 )的关系如图1所示,其中Zn的理论用量以溶液中
)的关系如图1所示,其中Zn的理论用量以溶液中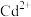 的物质的量为依据。实际生产中
的物质的量为依据。实际生产中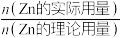 最佳比值为1.3,不宜超过该比值的原因是
最佳比值为1.3,不宜超过该比值的原因是
(4)向“置换”所得滤液中加
 溶液,经沉淀、过滤、洗涤等系列操作后,得到碱式碳酸锌[化学式为
溶液,经沉淀、过滤、洗涤等系列操作后,得到碱式碳酸锌[化学式为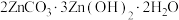 ,摩尔质量为583g/mol]
,摩尔质量为583g/mol]①碱式碳酸锌高温下完全分解至质量不变的反应方程式为
②碱式碳酸锌加热升温过程中固体的质量变化如图2所示。350℃时剩余固体中已不含碳元素,则350℃时剩余固体的成分为
您最近一年使用:0次



