已知非金属单质硫(S)是淡黄色固体粉末,难溶于水。为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:
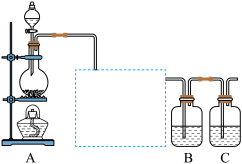
(1)装置A的分液漏斗中盛装的试剂是______ ,烧瓶中加入的试剂是______ 。
(2)画出虚线框内的实验装置图____________ ,并注明所加试剂,说明装置的作用_____________ 。
(3)装置B中盛放的试剂是_____ (选填下列所给试剂的代码),实验现象为________ ,化学反应方程式是________________ 。
A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
(4)从原子结构的角度简要分析氯元素的非金属性比硫元素的非金属性强的原因。_________ 。

(1)装置A的分液漏斗中盛装的试剂是
(2)画出虚线框内的实验装置图
(3)装置B中盛放的试剂是
A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
(4)从原子结构的角度简要分析氯元素的非金属性比硫元素的非金属性强的原因。
更新时间:2020-07-18 10:38:24
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、E均为短周期主族元素,其原子序数依次增大。A元素原子核内只有1个质子;A与C,B与D分别同主族;B、D两元素原子序数之和是A、C两元素原子序数之和的2倍。
请回答下列问题:
(1)B元素在元素周期表中的位置:___________ 。
(2)D和E的最高价氧化物对应水化物酸性较强的为___________ (用化学式表示)。
(3)C2B2的电子式是___________ ;用电子式表示化合物C2D的形成过程:___________ 。
(4)实验室中欲选用下列装置制取并收集纯净干燥的E2气体。

①实验中应选用的装置为___________ (按由左到右的连接顺序填写);
②装置A中发生反应的化学方程式为___________ 。
请回答下列问题:
(1)B元素在元素周期表中的位置:
(2)D和E的最高价氧化物对应水化物酸性较强的为
(3)C2B2的电子式是
(4)实验室中欲选用下列装置制取并收集纯净干燥的E2气体。

①实验中应选用的装置为
②装置A中发生反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】中国疾控中心指出,消毒是疫情防控的重要措施。含氯消毒剂是高效、安全的杀菌消毒剂。实验室制备氯气并验证氯气性质的装置如图所示。

(1)已知,装置A是氯气的发生装置。加入适量的浓盐酸与二氧化锰充分反应有黄绿色气体生成,写出反应的离子方程式:_______
(2)仪器a的名称为_______ 。
(3)装置B的作用是_______ ,同时用作安全瓶(监测实验时装置C中是否发生堵塞)。若装置C发生堵塞,装置B中将观察到的现象是_______ 。
(4)装置C的作用是检验氯气是否具有漂白性,则装置C中III处应放入的是_______ (填“干燥的有色布条”或“湿润的有色布条”)。装置C中II处应放入的试剂是_______ (填标号)
A.浓硫酸B.碱石灰C.无水氯化钙
(5)使用氯气消毒易产生危害人体健康的有机氯化物,用氯气和亚氯酸钠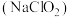 溶液可制备新的绿色消毒剂二氧化氯
溶液可制备新的绿色消毒剂二氧化氯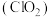 ,反应中还可得到氯化钠。当消耗标准状况下
,反应中还可得到氯化钠。当消耗标准状况下 时,制得
时,制得
_______ g。

(1)已知,装置A是氯气的发生装置。加入适量的浓盐酸与二氧化锰充分反应有黄绿色气体生成,写出反应的离子方程式:
(2)仪器a的名称为
(3)装置B的作用是
(4)装置C的作用是检验氯气是否具有漂白性,则装置C中III处应放入的是
A.浓硫酸B.碱石灰C.无水氯化钙
(5)使用氯气消毒易产生危害人体健康的有机氯化物,用氯气和亚氯酸钠
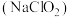 溶液可制备新的绿色消毒剂二氧化氯
溶液可制备新的绿色消毒剂二氧化氯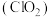 ,反应中还可得到氯化钠。当消耗标准状况下
,反应中还可得到氯化钠。当消耗标准状况下 时,制得
时,制得
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】用如图所示装置制取氯气和“84”消毒液并进行相关探究。
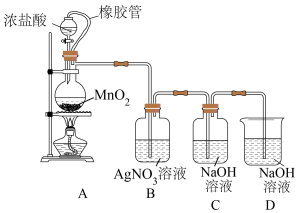
回答下列问题:
(1)装置
 中制取
中制取 的化学方程式为
的化学方程式为(2)装置
 中溶液出现浑浊,能否说明
中溶液出现浑浊,能否说明 与
与 溶液发生反应?
溶液发生反应?(3)为探究
 溶液的性质,某兴趣小组进行以下实验:
溶液的性质,某兴趣小组进行以下实验:ⅰ.取装置 (另外检验到装置
(另外检验到装置 中已无
中已无 剩余,也无溶解的
剩余,也无溶解的 )中溶液于试管中,滴入几滴紫色石蕊试液,溶液变蓝。
)中溶液于试管中,滴入几滴紫色石蕊试液,溶液变蓝。
ⅱ.将步骤ⅰ中蓝色溶液滴入浓盐酸中,蓝色迅速褪去变为无色,同时产生少量黄绿色气体。
ⅲ.取装置 中溶液于试管中,滴入稀
中溶液于试管中,滴入稀 溶液,光照,产生无色气泡。
溶液,光照,产生无色气泡。
ⅳ.取装置 中溶液于试管中,滴入几滴淀粉
中溶液于试管中,滴入几滴淀粉 溶液,溶液变蓝(已知淀粉遇
溶液,溶液变蓝(已知淀粉遇 变蓝色)。
变蓝色)。
①步骤ⅱ中蓝色迅速褪去的原因是
②步骤ⅲ中光照产生无色气泡的原因是
③步骤ⅳ说明 具有
具有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某同学在研究元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系)。
请你帮助该同学整理并完成实验报告。
(1)实验目的:研究__________________ 元素性质递变规律。
(2)实验用品:试剂:金属钠、镁条、铝条、稀盐酸、新制氯水、新制Na2S溶液、AlCl3溶液、NaOH溶液、酚酞溶液等。
仪器:______ 、______ 、滤纸、试管夹、胶头滴管、镊子、小刀、玻璃片、砂纸、火柴等。
(3)实验内容:(填写与实验步骤对应的实验现象的编号和①②的化学方程式及此实验的结论)
①___________________________________________________ ;
②___________________________________________________ ;
此实验的结论:__________________________________________________ 。
| 实验步骤 | 实验现象 |
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色 |
| ②向新制的Na2S溶液中滴加新制的氯水 | B.有气体产生,溶液变成浅红色 |
| ③将一小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体 |
| ④将镁条投入稀盐酸中 | D.反应不十分剧烈,产生无色气体 |
| ⑤将铝条投入稀盐酸中 | E.生成白色胶状沉淀,继而沉淀消失 |
| ⑥向AlCl3溶液中滴加NaOH溶液至过量 | F.生成淡黄色沉淀 |
请你帮助该同学整理并完成实验报告。
(1)实验目的:研究
(2)实验用品:试剂:金属钠、镁条、铝条、稀盐酸、新制氯水、新制Na2S溶液、AlCl3溶液、NaOH溶液、酚酞溶液等。
仪器:
(3)实验内容:(填写与实验步骤对应的实验现象的编号和①②的化学方程式及此实验的结论)
| 实验内容 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 实验现象(填A~F) |
②
此实验的结论:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】动手实践:某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系)。
请你帮助该同学整理并完成实验报告。
(1)实验目的:研究____________ 元素性质递变规律。
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlC13溶液,NaOH溶液,酚酞溶液等。仪器:①__________ ,②__________ ,试管,试管夹,胶头滴管,镊子,小刀,玻璃片,砂纸,火柴等。
(3)实验内容:(填写与实验步骤对应实验现象的编号和②的化学方程式及此实验的结论)__________
①_____________________________________ ,
②_____________________________________ ,
此实验的结论:_______________________________________________________ 。
| 实验步骤 | 实验现象 |
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色 |
| ②向新制得的Na2S溶液中满加新制的氯水 | B.有气体产生,溶液变成浅红色 |
| ③将一小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体 |
| ④将镁条投入稀盐酸中 | D.反应不十分剧烈;产生无色气体 |
| ⑤将铝条投入稀盐酸中 | E.生成白色胶状沉淀,继而沉淀消失 |
| ⑥向A1Cl3溶液中滴加NaOH溶液至过量 | F.生成淡黄色沉锭 |
(1)实验目的:研究
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液,AlC13溶液,NaOH溶液,酚酞溶液等。仪器:①
(3)实验内容:(填写与实验步骤对应实验现象的编号和②的化学方程式及此实验的结论)
| 实验内容 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 实验现象(填A~F) |
②
此实验的结论:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】有A、B、C、D、E五种短周期元素,它们的核电荷数按C、A、B、D、E的顺序增大。C、D都能分别与A按原子个数比为1∶1或2∶1形成化合物;CB可与EA2反应生成C2A与气态物质EB4;E的M层电子数是K层电子数的2倍。
(1)写出下列元素的名称 :B_______ ,E_____ 。
(2)写出电子式:EB4__________ 。
(3)D2A2中含有的化学键为___________ 。
(4)由A、C、D三种元素组成的化合物M属于______ (填“离子”或“共价”)化合物,M溶于水后_____ (填“会”或“不会”)发生化学变化,原因是_______ (从化学键的角度解释)。
(1)写出下列元素的
(2)写出电子式:EB4
(3)D2A2中含有的化学键为
(4)由A、C、D三种元素组成的化合物M属于
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某化学兴趣小组的同学学习了同周期元素性质的递变规律后,设计了一套实验方案进行实验探究,并记录了有关实验现象,如下表。
请你帮助该同学整理并完成实验报告。
(1)实验目的:__________________ 。
(2)实验仪器:①________ ;②________ ;③________ ;④试管夹;⑤镊子;⑥小刀;⑦玻璃片;⑧砂纸;⑨胶头滴管等。
(3)实验药品:钠、镁带、铝条、2 mol·L-1盐酸、新制的氯水、硫化氢饱和溶液、氯化铝溶液、氢氧化钠溶液等。
(4)请你写出上述的实验操作对应的现象(用A~F表示):①________ ;②________ ;③________ ;④________ ;⑤________ ;⑥________ 。
(4)写出实验操作②、⑥中有关反应的离子方程式:实验②__________ ,实验⑥___________ 。
(5)实验结论:__________________________ 。
| 实验操作 | 实验现象 |
| 1、用砂纸擦后的镁带与沸水反应,再向反应后溶液中滴加酚酞 | (A)浮于水面,熔成一个小球,在水面上无定向移动,随之消失,溶液变红色 (B)产生气体,可在空气中燃烧,溶液变成浅红色 (C)反应不十分强烈,产生的气体可以在空气中燃烧 (D)剧烈反应,产生可燃性气体 (E)生成白色胶状沉淀,进而沉淀消失 (F)生成淡黄色沉淀 |
| 2、向新制的H2S饱和溶液中滴加新制的氯水 | |
| 3、钠与滴有酚酞试液的冷水反应 | |
| 4、镁带与2 mol·L-1的盐酸反应 | |
| 5、铝条与2 mol·L-1的盐酸反应 | |
| 6、向AlCl3溶液滴加NaOH溶液至过量 |
请你帮助该同学整理并完成实验报告。
(1)实验目的:
(2)实验仪器:①
(3)实验药品:钠、镁带、铝条、2 mol·L-1盐酸、新制的氯水、硫化氢饱和溶液、氯化铝溶液、氢氧化钠溶液等。
(4)请你写出上述的实验操作对应的现象(用A~F表示):①
(4)写出实验操作②、⑥中有关反应的离子方程式:实验②
(5)实验结论:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某化学小组设计如下图所示的实验装置进行有关实验,以探究碳、硅元素的非金属性的相对强弱。

请回答下列问题:
(1)仪器A的名称是_______ ,B中反应的化学方程式是_______ 。
(2)部分实验步骤如下:连接仪器、_______ 、加药品后,打开a和_______ ,滴加浓硫酸,加热。
(3)装置E的作用是_______ 。
(4)能说明碳元素的非金属性比硅元素强的实验现象是_______ 。
(5)依据试管D中的实验现象,_______ (填“能”或“不能”)证明硫元素的非金属性强于碳元素,理由是_______ 。

请回答下列问题:
(1)仪器A的名称是
(2)部分实验步骤如下:连接仪器、
(3)装置E的作用是
(4)能说明碳元素的非金属性比硅元素强的实验现象是
(5)依据试管D中的实验现象,
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验。
(1)将钠、钾、镁、铝各1 mol分别投入到足量的同浓度的盐酸中,试预测实验结果:________ 与盐酸反应最剧烈,______ 与盐酸反应的速度最慢;________ 与盐酸反应产生的气体最多。
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为_________________________ 。
(3)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH碱性强于NH3·H2O,继而可以验证Na的金属性强于氮,你认为此设计是否合理?并说明理由。_____________ 。
Ⅱ.利用如图装置可验证同主族元素非金属性的变化规律

(4)仪器B的名称为_______ ,干燥管D的作用为___________ 。
(5)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液________________ (填现象),即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,可用______________ 溶液吸收尾气。
(1)将钠、钾、镁、铝各1 mol分别投入到足量的同浓度的盐酸中,试预测实验结果:
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为
(3)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH碱性强于NH3·H2O,继而可以验证Na的金属性强于氮,你认为此设计是否合理?并说明理由。
Ⅱ.利用如图装置可验证同主族元素非金属性的变化规律

(4)仪器B的名称为
(5)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】I.某校化学社团活动小组同学在学习完钠及其化合物后,设计了如图实验探究钠及其化合物的性质,实验装置如图所示(已知:试管A中装入足量的NaHCO3固体,D为固定蚊香的硬纸片)。请回答下列问题:
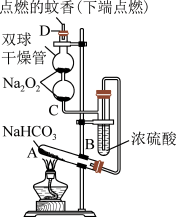
(1)Na2O2固体呈____ 色。
(2)试管A中发生反应的化学方程式为____ 。
(3)D处观察到的实验现象是____ ;故推测Na2O2可用于____ 。
II.钠及其化合物在化工生产和日常生活中都有广泛的用途。已知2NaCl(熔融) 2Na+Cl2↑,物质C、D、E、F、G有如图转化关系(部分反应条件及产物已省略):
2Na+Cl2↑,物质C、D、E、F、G有如图转化关系(部分反应条件及产物已省略):
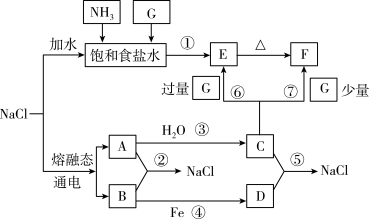
(4)写出上述转化关系中对应物质的化学式:D____ ,F____ 。
(5)反应③的离子方程式为____ 。
(6)若把Na投入到D的水溶液中,观察到的现象是:____ 。
(7)反应①为侯氏制碱法的原理之一,制备时能不能先在饱和食盐水中通入G?____ (填“能”或“不能”);请写出反应①的化学方程式:____ 。

(1)Na2O2固体呈
(2)试管A中发生反应的化学方程式为
(3)D处观察到的实验现象是
II.钠及其化合物在化工生产和日常生活中都有广泛的用途。已知2NaCl(熔融)
 2Na+Cl2↑,物质C、D、E、F、G有如图转化关系(部分反应条件及产物已省略):
2Na+Cl2↑,物质C、D、E、F、G有如图转化关系(部分反应条件及产物已省略):
(4)写出上述转化关系中对应物质的化学式:D
(5)反应③的离子方程式为
(6)若把Na投入到D的水溶液中,观察到的现象是:
(7)反应①为侯氏制碱法的原理之一,制备时能不能先在饱和食盐水中通入G?
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某校学生课外活动小组的同学设计下图所示实验装置,用来验证一氧化碳具有还原性。已知碱石灰的成分是氢氧化钠和氧化钙的混合物;炭与水蒸气在高温条件下发生以下反应:C + H2O(g) CO + H2。回答下列问题:
CO + H2。回答下列问题:

(1)写出装置A中发生反应的离子方程式____________________ 。
(2)若实验中没有装置C,使装置B与装置D直接相连,会对实验造成的影响是:____________ 。
(3)装置D中黑色固体为___________ (填名称)。
(4)按照如图装置进行实验时,首先进行的操作是___________________________________ 。
(5)根据实验中的____________________________ 现象,可证明CO具有还原性。
(6)若要根据装置F中澄清石灰水变浑浊的现象确认一氧化碳具有还原性,应在上图装置____ 与____ 之间连接下图中的____________________ 装置(填序号)。

 CO + H2。回答下列问题:
CO + H2。回答下列问题:
(1)写出装置A中发生反应的离子方程式
(2)若实验中没有装置C,使装置B与装置D直接相连,会对实验造成的影响是:
(3)装置D中黑色固体为
(4)按照如图装置进行实验时,首先进行的操作是
(5)根据实验中的
(6)若要根据装置F中澄清石灰水变浑浊的现象确认一氧化碳具有还原性,应在上图装置

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某小组在探究 性质的实验中观察到异常现象。
性质的实验中观察到异常现象。
资料:i. (红色),
(红色), 中S元素的化合价为-2价
中S元素的化合价为-2价
ii. 是不溶于盐酸的白色沉淀
是不溶于盐酸的白色沉淀
(1)实验I体现了 的
的______ 性,补全 与
与 酸性溶液反应的离子方程式:
酸性溶液反应的离子方程式:______ 。
______ ______
______ ______
______ ______
______ ______
______
(2)探究“红色褪去”的原因,进行实验II:将褪色后的溶液分三份分别进行实验。

实验II得出的结论是:红色褪去的原因是______ 。
(3)为进一步探究“红色褪去”的原因,进行了实验III.
分析上述三个实验,下列叙述正确的是______(填字母)。
(4)上述实验探究过程用到的实验方法有______ (写出一条)。
(5)验证 性质的实验还可以选用
性质的实验还可以选用 溶液和酸化的
溶液和酸化的 溶液,二者发生反应的离子方程式是:
溶液,二者发生反应的离子方程式是:______ 。
 性质的实验中观察到异常现象。
性质的实验中观察到异常现象。| 实验I | 现象 |
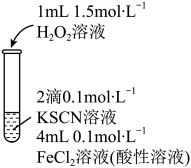 | 溶液变红,片刻红色褪去,有气体生成(经检验为 )。 )。 |
 (红色),
(红色), 中S元素的化合价为-2价
中S元素的化合价为-2价ii.
 是不溶于盐酸的白色沉淀
是不溶于盐酸的白色沉淀(1)实验I体现了
 的
的 与
与 酸性溶液反应的离子方程式:
酸性溶液反应的离子方程式:______
 ______
______ ______
______ ______
______ ______
______
(2)探究“红色褪去”的原因,进行实验II:将褪色后的溶液分三份分别进行实验。

实验II得出的结论是:红色褪去的原因是
(3)为进一步探究“红色褪去”的原因,进行了实验III.
| 实验III | 现象 |
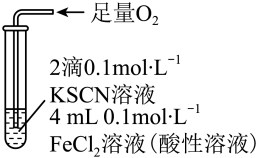 | 溶液变红,一段时间后不褪色。 |
取上述反应后的溶液,滴加盐酸和 溶液 溶液 | 无白色沉淀产生。 |
A.实验III中发生了氧化还原反应: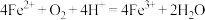 |
B.通过实验III推出实验I中氧化 的只有 的只有 |
C. 在该实验条件下不能使红色溶液褪色 在该实验条件下不能使红色溶液褪色 |
D.实验I中红色褪去与 的氧化性有关 的氧化性有关 |
(5)验证
 性质的实验还可以选用
性质的实验还可以选用 溶液和酸化的
溶液和酸化的 溶液,二者发生反应的离子方程式是:
溶液,二者发生反应的离子方程式是:
您最近一年使用:0次



