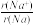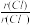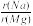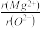下列排列顺序中,正确的是
①热稳定性: ②离子半径:
②离子半径: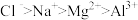 ③酸性:
③酸性: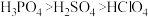 ④沸点:H2O˃H2Se˃H2S
④沸点:H2O˃H2Se˃H2S
①热稳定性:
 ②离子半径:
②离子半径: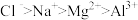 ③酸性:
③酸性: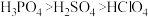 ④沸点:H2O˃H2Se˃H2S
④沸点:H2O˃H2Se˃H2S| A.①③ | B.②③ | C.①④ | D.②④ |
更新时间:2020-07-25 21:48:58
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列关于元素周期表和元素周期律的说法不正确的是
| A.O与S为同主族元素,且O比S的非金属性强 |
| B.HF、HCl、HBr、HI的热稳定性依次逐渐减弱 |
| C.第三周期元素从Na到Cl,金属性逐渐增强 |
| D.原子序数从3依次增加到9,原子半径逐渐减少 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】X、Y、Z、W是四种短周期主族元素,它们在元素周期表中的相对位置如图所示,其中元素X的最高正价为+5。下列说法中正确的是
| X | Y | |||
| Z | W |
| A.Y、W的最高正价相等 |
| B.简单氢化物的稳定性:X>Y>W |
C.Z与W形成的化合物溶液中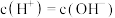 |
| D.X、Y可形成极性分子XY3 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】二氟化二氧(O2F2)是一种极强的氧化剂和氟化剂,分子结构与过氧化氢相似,性质极其不稳定,可以发生反应: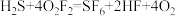 。下列有关说法不正确的是
。下列有关说法不正确的是
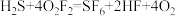 。下列有关说法不正确的是
。下列有关说法不正确的是| A.离子半径:S2->O2->F- |
| B.O2F2分子中氧原子的价层电子对数为4 |
| C.O2F2分子中极性键与非极性键数目之比为2:1 |
| D.HF在标准状况下呈液态,主要原因是极性较强,范德华力较大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中Y是地壳中含量处于第二的元素,下列判断正确的是( )
| X | |||
| Y | Z | W |
| A.原子半径:rW>rZ>rY>rX |
| B.X、Z元素的单质有多种 |
| C.最简单气态氢化物的热稳定性:Z>W |
| D.Y的氧化物是酸性氧化物,不溶于任何酸 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列图像正确的是
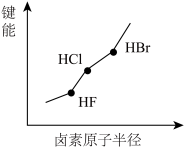 |  | 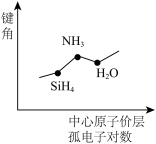 | 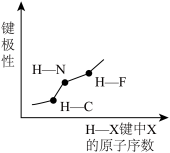 |
| A | B | C | D |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列关于氢键及范德华力的叙述正确的是
| A.氢键比范德华力强,它们都属于化学键 |
| B.分子间形成的氢键会使物质的熔点和沸点升高 |
| C.HF分子间只存在氢键,没有范德华力 |
| D.由于 HF分子间存在氢键,所以 HF比 H2O 更稳定 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】关于氢键,下列说法不正确的是( )
| A.NH3的稳定性很强,是因为其分子间能形成氢键 |
| B.水在结冰时体积膨胀,是由于水分子之间存在氢键 |
| C.HF的沸点比HCl的沸点高是由于HF分子间存在氢键所致 |
| D.在氨水中水分子和氨分子之间也存在着氢键 |
您最近一年使用:0次