A、B、C 为短周期元素,在周期表中所处的位置如图所示.A、C 两元素的原子核外电子数之和等于 B 原子的质子数。
(1)写出 A、B、C 三种元素的元素符号: ______ 、 ______ 、 ______ 。
(2)B 元素位于元素周期表中的______ 周期 ______ 族
(3)C 的原子结构示意图是______ ,C 的单质与水反应的化学反应方程式为 ______ 。
(4)比较 B、C 的原子半径 B______ C,写出过量 A 的简单气态氢化物与 B 的最高价氧化物 对应的水化物反应的化学反应方程式 ____________ 。
| A | C | |
| B |
(2)B 元素位于元素周期表中的
(3)C 的原子结构示意图是
(4)比较 B、C 的原子半径 B
更新时间:2020-08-06 12:57:25
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】人类的农业生产离不开氮肥,几乎所有的氮肥都以氨为原料,某化学兴趣小组利用图一装置制备氨气并探究相关性质。
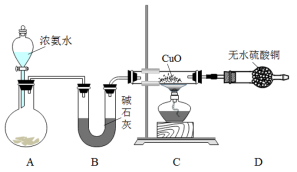
(1)装置B中,碱石灰作用___ , 氨气的空间构型为____ ;
(2)实验中观察到C中CuO粉末变红,D中无水硫酸铜变蓝,并收集到一种单质气体。则该反应相关化学方程式为:___ 。工业上,通过氨的催化氧化等一系列反应最终可以制得硝酸,请写出氨的催化氧化的化学反应方程式____ ;
(3)实验室还可用下图所示装置制备氨气。化学反应方程式为_______ ;
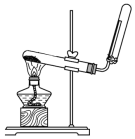
(4)该实验缺少尾气吸收装置。下图中能用来吸收尾气的装置是___ (填装置序号)。

(5)如图装置中,a表示胶头滴管和烧杯中的液体,b表示烧瓶中的气体,不能形成 喷泉实验现象的a中液体和b中气体的组合是___

A. a-NaOH溶液、b- HCl气体 B. a-NaOH 溶液、 b- CO2气体
C. a-HCl溶液、 b-NH3气体 D. a-水、b-CO2

(1)装置B中,碱石灰作用
(2)实验中观察到C中CuO粉末变红,D中无水硫酸铜变蓝,并收集到一种单质气体。则该反应相关化学方程式为:
(3)实验室还可用下图所示装置制备氨气。化学反应方程式为

(4)该实验缺少尾气吸收装置。下图中能用来吸收尾气的装置是

(5)如图装置中,a表示胶头滴管和烧杯中的液体,b表示烧瓶中的气体,

A. a-NaOH溶液、b- HCl气体 B. a-NaOH 溶液、 b- CO2气体
C. a-HCl溶液、 b-NH3气体 D. a-水、b-CO2
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】已知C的相对分子质量比B大16,D为强酸。
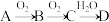
I.若A为淡黄色固体,则:
(1)D的化学式为___________ 。
(2)写出B→C的化学方程式___________ 。
(3)将B通入盛有 溶液的试管中,再滴加少量过氧化氢溶液,现象是
溶液的试管中,再滴加少量过氧化氢溶液,现象是___________ ,说明B具有___________ 性。
II.若A和D可以反应生成盐,则:
(4)A的化学式为___________ ,可用___________ 试纸检验A的存在。
(5)写出C→D的反应中,氧化剂与还原剂的物质的量之比为___________ 。
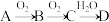
I.若A为淡黄色固体,则:
(1)D的化学式为
(2)写出B→C的化学方程式
(3)将B通入盛有
 溶液的试管中,再滴加少量过氧化氢溶液,现象是
溶液的试管中,再滴加少量过氧化氢溶液,现象是II.若A和D可以反应生成盐,则:
(4)A的化学式为
(5)写出C→D的反应中,氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】如图所示是元素周期表的一部分,表中所列字母分别代表一种元素。

试回答下列问题:
(1)以上元素中,属于d区元素的是_______ (填元素符号),元素k在周期表的位置是_______ 。
(2)画出c的核外电子排布图_______ ,这样排布遵循了构造原理、_______ 原理和_______ 规则。
(3)元素c的电负性_______ 元素g的电负性(填“>”、“=”、“<”),元素b、c、e的第一电离能由大到小的顺序是_______ (用元素符号表示);第三周期元素最高价氧化物对应的水化物中,酸性最强的是_______ (填化合物的化学式)。

试回答下列问题:
(1)以上元素中,属于d区元素的是
(2)画出c的核外电子排布图
(3)元素c的电负性
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】下列编号代表元素周期表中的元素,用化学用语回答下列问题:
(1)画出⑦的原子结构示意图______________ 。
(2)④、⑤、⑥的最高价氧化物的水化物碱性由强到弱顺序为______________ (填化学式,下同);②、③、④形成的简单离子半径由大到小的顺序是______________ 。
(3)写出⑨⑩两元素最高价氧化物对应的水化物之间反应的离子方程式______________ 。
(4)写出实验室制取①的气态氢化物的化学方程式______________ 。
(5)⑧与⑨非金属性较强的是_______________ 填元素符号),下列能证实这一事实的是______________ 。
a.单质的沸点⑨小于⑧
b.氢化物的稳定性⑨大于⑧
c.氢化物水溶液的酸性⑨大于⑧
d.简单阴离子的还原性⑧大于⑨
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 四 | ⑩ |
(2)④、⑤、⑥的最高价氧化物的水化物碱性由强到弱顺序为
(3)写出⑨⑩两元素最高价氧化物对应的水化物之间反应的离子方程式
(4)写出实验室制取①的气态氢化物的化学方程式
(5)⑧与⑨非金属性较强的是
a.单质的沸点⑨小于⑧
b.氢化物的稳定性⑨大于⑧
c.氢化物水溶液的酸性⑨大于⑧
d.简单阴离子的还原性⑧大于⑨
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】下表是元素周期表的一部分,根据表中出的①-⑤元素,回答下列问题:
(1)写出③的元素符号_______ 。
(2)画出④的原子结构示图_______ 。
(3)元素⑤在元素周期表中的位置是_______ 周期_______ 族。
(4)①②③三元素中非金属性最强的是_______ (填元素名称)。
(5)元素③与元素④形成化合物的化学式为_______ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | Ar |
(1)写出③的元素符号
(2)画出④的原子结构示图
(3)元素⑤在元素周期表中的位置是
(4)①②③三元素中非金属性最强的是
(5)元素③与元素④形成化合物的化学式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】下图是元素周期表的一部分,根据① ~ ⑨在周期表中的位置按题目要求回答:
(1)在元素①~⑨中,金属性最强的元素是__ (填元素符号)。
(2)①、②、③三种元素的原子半径由大到小的顺序是________ (填元素符号)。
(3)⑧和⑨两种元素的最高价氧化物对应的水化物中酸性较强的是____ (填化学式)。
(4)元素④的简单氢化物比元素⑧的简单氢化物的稳定性_____ (填“强”或“弱”)。
(5)⑥、⑦、⑨三种元素的常见离子的半径最小的是_______ (用化学式表示)。
(6)元素②和元素④形成的一种化合物在大气中的含量过高时会产生温室效应,写出该化合物的电子式_______ 。
(7)⑤和⑦两种元素的最高价氧化物对应的水化物之间发生反应的离子方程式为____ 。
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(2)①、②、③三种元素的原子半径由大到小的顺序是
(3)⑧和⑨两种元素的最高价氧化物对应的水化物中酸性较强的是
(4)元素④的简单氢化物比元素⑧的简单氢化物的稳定性
(5)⑥、⑦、⑨三种元素的常见离子的半径最小的是
(6)元素②和元素④形成的一种化合物在大气中的含量过高时会产生温室效应,写出该化合物的电子式
(7)⑤和⑦两种元素的最高价氧化物对应的水化物之间发生反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】随着原子序数的递增,八种短周期元素(用字母x、y、z…表示)的原子半径的相对大小、最高正价或最低负价的变化如下图所示。请根据判断出的元素回答下列问题
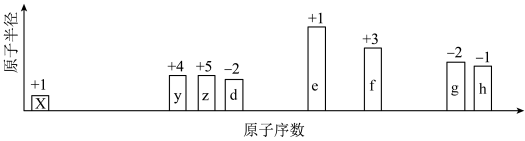
(1)f在元素周期表中的位置:___________ 。
(2)比较d、e、f简单离子的半径大小:___________ (用化学符号表示,且用“>”连接,下同)。比较g、h的最高价氧化物对应的水化物的酸性强弱:___________ 。
(3)写出x与d形成的常见的四原子化合物的电子式___________ 。
(4)向1L浓度均为0.2mol·L-1z和g的最高价含氧酸的混合溶液中加入足量的铁粉,则最多能溶解铁粉的质量为___________ 。
(5)上述元素可组成盐R:zx4f(gd4)2,向盛有10 mL 1mol·L-1 R溶液的烧杯中滴加1 mol·L-1 NaOH溶液,沉淀的物质的量随NaOH溶液体积的变化示意图如下:
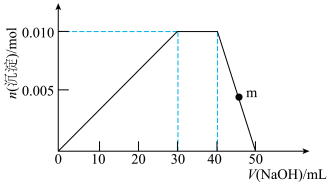
①m点反应的离子方程式:___________ 。
②若向10 mL 1mol·L-1R溶液中改加20 mL 1.2mol·L-1 Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为___________ mol。

(1)f在元素周期表中的位置:
(2)比较d、e、f简单离子的半径大小:
(3)写出x与d形成的常见的四原子化合物的电子式
(4)向1L浓度均为0.2mol·L-1z和g的最高价含氧酸的混合溶液中加入足量的铁粉,则最多能溶解铁粉的质量为
(5)上述元素可组成盐R:zx4f(gd4)2,向盛有10 mL 1mol·L-1 R溶液的烧杯中滴加1 mol·L-1 NaOH溶液,沉淀的物质的量随NaOH溶液体积的变化示意图如下:

①m点反应的离子方程式:
②若向10 mL 1mol·L-1R溶液中改加20 mL 1.2mol·L-1 Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐3】C、O、Na、Al、Si、S、Cl是生活中常见的几种元素。请回答下列问题:
(1)铝在元素周期表中的位置为_____ 。
(2)用“大于”“小于”或“等于”填空:
(3)在C、O、Si、S、Cl元素形成的简单氢化物中,稳定性最差的氢化物的电子式为_____ 。
(4)利用图装置可验证同主族元素非金属性的变化规律:
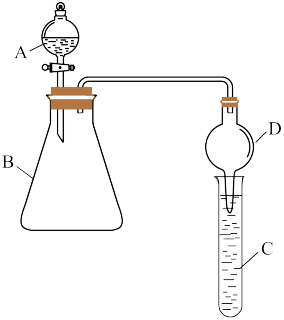
①仪器A的名称为_____ ,仪器D的作用为_____ 。
②若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成Cl2),C中加KI-淀粉混合溶液,观察到C中溶液_____ 的现象,即可证明,反应的离子方程式为_____ 。
(1)铝在元素周期表中的位置为
(2)用“大于”“小于”或“等于”填空:
| ①原子半径 | ②酸性 | ③得电子能力 |
| O | H2CO3 | 35Cl |
(4)利用图装置可验证同主族元素非金属性的变化规律:

①仪器A的名称为
②若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成Cl2),C中加KI-淀粉混合溶液,观察到C中溶液
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】下表列出了A-F6种元素在周期表中短周期的位置。
请回答下列问题:
(1)C元素在周期表中的位置___ ;C元素的一种氧化物是温室气体,该氧化物的电子式为:___ 。
(2)A和B的最高价氧化物对应的水化物碱性较强的是___ ;(填化学式)
(3)D与同族下一周期元素的气态氢化物的沸点较高的是___ (填化学式),原因是___ 。
(4)元素E与元素F相比,非金属性较强的是___ (用元素符号填写),下列表述中能证明这一事实的是___ (可多选)。
①F的氢化物比E的氢化物稳定
②常温下F的单质和E的单质状态不同
③一定条件下F和E的单质都能与氢氧化钠溶液反应
④F的氧化物的水化物的酸性比E的氧化物的水化物的酸性强
⑤F可以把E从其氢化物水溶液中置换出来
(5)元素E的一种氧化物通入氯化钡溶液无沉淀,通入硝酸钡溶液却会产生白色沉淀,写出少量该氧化物通入硝酸钡溶液的离子方程式___ 。
| C | D | ||||||
| A | B | E | F |
(1)C元素在周期表中的位置
(2)A和B的最高价氧化物对应的水化物碱性较强的是
(3)D与同族下一周期元素的气态氢化物的沸点较高的是
(4)元素E与元素F相比,非金属性较强的是
①F的氢化物比E的氢化物稳定
②常温下F的单质和E的单质状态不同
③一定条件下F和E的单质都能与氢氧化钠溶液反应
④F的氧化物的水化物的酸性比E的氧化物的水化物的酸性强
⑤F可以把E从其氢化物水溶液中置换出来
(5)元素E的一种氧化物通入氯化钡溶液无沉淀,通入硝酸钡溶液却会产生白色沉淀,写出少量该氧化物通入硝酸钡溶液的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,回答下列问题:
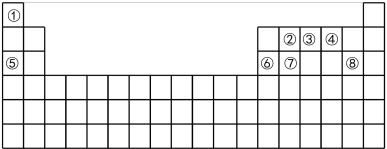
(1)写出元素⑥在周期表中的位置___________ 。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是___________ (填化学式)。
(3)元素①与④能组成一种质子数为10、电子数也为10的微粒,写出元素⑤的单质和该微粒反应的化学方程式:___________ 。
(4)写出实验室制取元素⑧的单质的化学方程式:___________ 。
(5)碘(Ⅰ)在元素周期表中位于ⅦA族,是人体必需的微量元素之一、下列事实能够用“碘的非金属性比氯的弱”来解释的是___________ (填标号)。
a.Cl2能使淀粉KI试纸变蓝 b.HClO3的酸性强于HIO3
c.Cl2比I2更容易与H2化合 d.HCl比HI更不易分解

(1)写出元素⑥在周期表中的位置
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
(3)元素①与④能组成一种质子数为10、电子数也为10的微粒,写出元素⑤的单质和该微粒反应的化学方程式:
(4)写出实验室制取元素⑧的单质的化学方程式:
(5)碘(Ⅰ)在元素周期表中位于ⅦA族,是人体必需的微量元素之一、下列事实能够用“碘的非金属性比氯的弱”来解释的是
a.Cl2能使淀粉KI试纸变蓝 b.HClO3的酸性强于HIO3
c.Cl2比I2更容易与H2化合 d.HCl比HI更不易分解
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】五种短周期元素A、B、C、D、E的原子序数依次增大,A和C同族,B和D同族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物在水中呈中性。回答下列问题:
(1)五种元素中,原子半径最大的是__________ ,非金属性最强的是__________ (填元素符号);
(2)由A和B、D、E所形成的共价型化合物中,热稳定性最差的是__________ (用化学式表示);
(3)A和E形成的化合物与A和B形成的化合物反应,产物的电子式为_______________ 。
(1)五种元素中,原子半径最大的是
(2)由A和B、D、E所形成的共价型化合物中,热稳定性最差的是
(3)A和E形成的化合物与A和B形成的化合物反应,产物的电子式为
您最近一年使用:0次




