实验小组的同学们将三种金属按照下表的装置进行实验。回答问题:
(1)装置甲中铁极的电极反应式是____________ ,溶液中H+向_____ 极移动(填“正”或“负”)。
(2)装置乙中铜极发生____________ (填“氧化”或“还原”)反应。
(3)装置丙中M极为______ (填“正极”或“负极”),一段时间后溶液的酸性_____________ (填“增强”“减弱”或“不变”)。
(4)Fe、Cu、M中金属活动性最强的是_____________ 。
| 序号 | 甲 | 乙 | 丙 |
| 装置 |  | 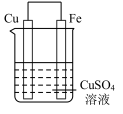 | 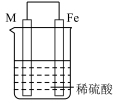 |
| 现象 | 溶液变为浅绿色,Cu极产生大量气泡 | Cu极的质量增加 | M极的质量减少 |
(1)装置甲中铁极的电极反应式是
(2)装置乙中铜极发生
(3)装置丙中M极为
(4)Fe、Cu、M中金属活动性最强的是
更新时间:2020-08-08 18:36:54
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】某兴趣小组为了探究铝电极在电池中的作用,设计并进行了以下系列实验,实验结果记录如下:
注:①实验均为常温下完成;②电流计指针偏转方向为正极方向。试根据表中实验现象完成下列问题:
(1)实验1、2中Al所作的电极(指正极或负极)______ (填“相同”或“不同”)。
(2)对实验3完成下列填空:
①Al为______ 极,电极反应式为______ 。
②石墨为______ 极,电极反应式为______ 。
③电池总反应式为______
(3)实验4中Al作______ 极,理由是______ 。
(4)解释实验5中电流计偏向Al的原因______ 。
(5)根据实验结果总结出影响铝在电池中作正极或负极的因素有______ 。
| 编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、C(石墨) | 稀盐酸 | 偏向石墨 |
| 4 | Mg、Al | NaOH溶液 | 偏向Mg |
| 5 | Al、Cu | 浓硝酸 | 偏向Al |
注:①实验均为常温下完成;②电流计指针偏转方向为正极方向。试根据表中实验现象完成下列问题:
(1)实验1、2中Al所作的电极(指正极或负极)
(2)对实验3完成下列填空:
①Al为
②石墨为
③电池总反应式为
(3)实验4中Al作
(4)解释实验5中电流计偏向Al的原因
(5)根据实验结果总结出影响铝在电池中作正极或负极的因素有
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】根据原电池的构成、原理、以及原电池反应的快慢等知识,结合图中装置填空:
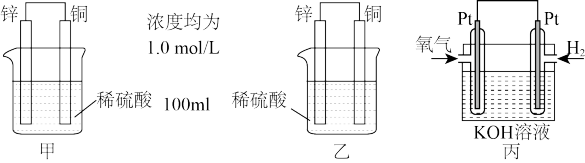
(1)在装置甲和乙中属于原电池装置的是_______ ;(选“甲、乙”作答)
(2)当同时将铜和锌分别按照图示插入甲、乙烧杯中,描述甲、乙烧杯中铜棒上的现象_______ ;乙中锌棒参与反应的离子反应方程式为_______ ;
(3)在图甲装置中,铜(棒)电极上的电极反应式为_______ ,5分钟后甲中溶液质量增重31.5 g,此时转移电子数目为_______ ;
(4)装置丙为氢氧燃料电池的构造图,电解质溶液的溶质是KOH。通入氧气一极的电极反应式为_______ ;当线路中转移4NA个电子时,理论上应消耗H2在标准状况下的体积为_______ 。

(1)在装置甲和乙中属于原电池装置的是
(2)当同时将铜和锌分别按照图示插入甲、乙烧杯中,描述甲、乙烧杯中铜棒上的现象
(3)在图甲装置中,铜(棒)电极上的电极反应式为
(4)装置丙为氢氧燃料电池的构造图,电解质溶液的溶质是KOH。通入氧气一极的电极反应式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】某化学兴趣小组为了探究铝电极在电池中的作用,设计并进行了以实验结果记录如下:
回答下列(1)、(2)小题:
⑴实验1中Al作的电极为____ (填“正极”或“负极”),Cu作的电极为____ (填“正极"或“负极”)。
⑵实验2观察到C(石墨)棒上产生的现象是____ ,负极的电极反应式为____ .如图是电解质为稀硫酸溶液的氢氧燃料电池。该电池的电子从电极____ 经过导线流向电极____ (填a或b)

| 编号 | 电极材料 | 电解质溶液 | 电流表指针偏转方向 |
| 1 | Al、Cu | 稀盐酸 | 偏向Cu |
| 2 | Al、C(石墨) | 稀盐酸 | 偏向石墨 |
回答下列(1)、(2)小题:
⑴实验1中Al作的电极为
⑵实验2观察到C(石墨)棒上产生的现象是

您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】依据氧化还原反应:2Ag+(aq)+Cu(s)=2Ag(s)+Cu2+(aq)设计的原电池如下图所示。
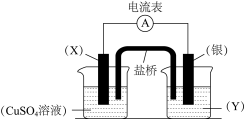
请回答下列问题:
(1)电极X的材料是_______ ,电解质溶液Y是_______ 。
(2)银电极为原电池的_______ 极,发生的电极反应为_______ 。
(3)X电极上发生的电极反应为_______ 。
(4)导线中电流方向是_______ (填“X→银”或“银→X”)。

请回答下列问题:
(1)电极X的材料是
(2)银电极为原电池的
(3)X电极上发生的电极反应为
(4)导线中电流方向是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】回答下列问题
(1)下列五个装置中属于原电池的是___________ 。
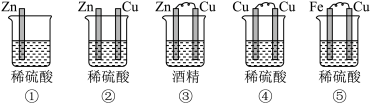
(2)在选出的原电池中,___________ 是负极材料,发生___________ (填“氧化”或“还原”)反应,___________ 是正极材料,该极的现象是___________ 。
(3)在该原电池的内电路中,硫酸根离子移向___________ (填“正”或“负”)极,此电极的电极反应式为___________ 。
(1)下列五个装置中属于原电池的是

(2)在选出的原电池中,
(3)在该原电池的内电路中,硫酸根离子移向
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】下面有四种原电池装置:

回答下面问题:
(1)装置①的负极是___________ (填元素符号,下同),原电池反应的离子方程式为___________ 。
(2)装置②的正极是___________ ,负极发生的电极反应为___________ 。
(3)装置③中有电子流出的电极是___________ ,原电池反应的离子方程式为___________ 。
(4)装置④发生还原反应的电极是___________ ,该极的电极反应为___________ 。

回答下面问题:
(1)装置①的负极是
(2)装置②的正极是
(3)装置③中有电子流出的电极是
(4)装置④发生还原反应的电极是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】某实验室备有如下实验用品:铁片、铜片、锌片、碳棒、FeCl3溶液、ZnCl2溶液、CuSO4溶液、AgNO3溶液以及导线。试回答下列问题:
(1)若选用铁片、铜片、AgNO3溶液及导线,_______ (填“能”或“不能”)构成原电池。
(2)判断该电池的正极材料是_______ ,负极材料是_______ ,正极反应式是_______ ,负极反应式是 _______ ,电池总反应式是_______ 。
(1)若选用铁片、铜片、AgNO3溶液及导线,
(2)判断该电池的正极材料是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】Ⅰ.下图为氢氧燃料电池原理示意图,按下图的提示,回答以下问题:
(1)若电解质溶液为KOH溶液,则写出电极反应式: 极
极 ____________ , 极
极 _______________ 。
(2)若电解质溶液为稀H2SO4,则写出电极反应式: 极
极 _____________ , 极
极 _______________ 。

Ⅱ.氨基甲酸铵分解反应为NH2COONH4(s) 2NH3(g)+CO2(g),在体积不变的密闭容器中发生反应,可以判断该反应已经达到平衡的是
2NH3(g)+CO2(g),在体积不变的密闭容器中发生反应,可以判断该反应已经达到平衡的是__________ 。
A.密闭容器中氨气的体积分数不变 B.1molNH2COONH4分解同时有44gCO2消耗
C.密闭容器中混合气体的密度不变 D.
(1)若电解质溶液为KOH溶液,则写出电极反应式:
 极
极  极
极 (2)若电解质溶液为稀H2SO4,则写出电极反应式:
 极
极  极
极 
Ⅱ.氨基甲酸铵分解反应为NH2COONH4(s)
 2NH3(g)+CO2(g),在体积不变的密闭容器中发生反应,可以判断该反应已经达到平衡的是
2NH3(g)+CO2(g),在体积不变的密闭容器中发生反应,可以判断该反应已经达到平衡的是A.密闭容器中氨气的体积分数不变 B.1molNH2COONH4分解同时有44gCO2消耗
C.密闭容器中混合气体的密度不变 D.

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】I.由A、B、C、D四种金属按下表中装置进行实验。
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是______________________________________ 。
(2)装置乙中正极的电极反应式是________________________________________ 。
(3)四种金属活泼性由强到弱的顺序是______________________ 。
II.分别按图所示甲、乙装置进行实验,图中两个烧杯中的溶液为相同浓度的稀硫酸,甲中A为电流表。
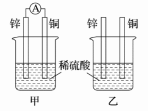
(1)下列叙述正确的是________ 。
A.两烧杯中铜片表面均无气泡产生 B.甲中铜片作正极,乙中铜片作负极
C.两烧杯中溶液中的H+浓度均减小 D.产生气泡的速率甲中的比乙中的慢
(2)甲装置中,某同学发现不仅铜片上有气泡产生,锌片上也产生了气体,原因可能是________________________________________________________________________ 。
(3)甲装置中,若把稀硫酸换成CuSO4溶液,试写出铜电极的电极反应________________________ 。
| 装置 |  | 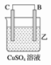 | 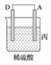 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是
(2)装置乙中正极的电极反应式是
(3)四种金属活泼性由强到弱的顺序是
II.分别按图所示甲、乙装置进行实验,图中两个烧杯中的溶液为相同浓度的稀硫酸,甲中A为电流表。

(1)下列叙述正确的是
A.两烧杯中铜片表面均无气泡产生 B.甲中铜片作正极,乙中铜片作负极
C.两烧杯中溶液中的H+浓度均减小 D.产生气泡的速率甲中的比乙中的慢
(2)甲装置中,某同学发现不仅铜片上有气泡产生,锌片上也产生了气体,原因可能是
(3)甲装置中,若把稀硫酸换成CuSO4溶液,试写出铜电极的电极反应
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】现有A、B、C、D四种金属片,①把A、B用导线连接后同时浸入稀硫酸溶液中,H+向A迁移;②把A、C用导线连接后同时浸入稀硫酸溶液中,电流方向为C→A;③把C、D用导线连接后同时浸入稀硫酸溶液中,C发生氧化反应。根据上述情况,回答下列问题:
(1)上述四种金属的活动性顺序是:_________ ;
(2)③中外电路导线中电子的流向为:________ ;
(3)①中B电极对应的实验现象为:________ 。
(1)上述四种金属的活动性顺序是:
(2)③中外电路导线中电子的流向为:
(3)①中B电极对应的实验现象为:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】某校化学研究性学习小组欲设计实验验证Zn、Fe、Cu的金属活动性,他们提出了以下两种方案。请你帮助他们完成有关实验项目:
(1)用三种金属与盐酸反应的现象来判断,实验中除选择大小相同的金属片外,还需要控制___ 、___ 相同;若选用一种盐溶液验证三种金属的活泼性,该试剂为___ 。
(2)某小组同学采用Zn、Fe作为电极,只用一个原电池证明三种金属的活动性,则电解质溶液最好选用___ 。
A.0.5mol·L-1氯化亚铁溶液
B.0.5mol·L-1氯化铜溶液
C.0.5mol·L-1盐酸
D.0.5mol·L-1氯化亚铁和0.5mol·L-1氯化铜混合溶液
(1)用三种金属与盐酸反应的现象来判断,实验中除选择大小相同的金属片外,还需要控制
(2)某小组同学采用Zn、Fe作为电极,只用一个原电池证明三种金属的活动性,则电解质溶液最好选用
A.0.5mol·L-1氯化亚铁溶液
B.0.5mol·L-1氯化铜溶液
C.0.5mol·L-1盐酸
D.0.5mol·L-1氯化亚铁和0.5mol·L-1氯化铜混合溶液
您最近一年使用:0次



