铝是一种重要金属,从铝土矿(主要成分为Al2O3,Fe2O3、SiO2等)中冶炼Al的工业生产流程如下图:
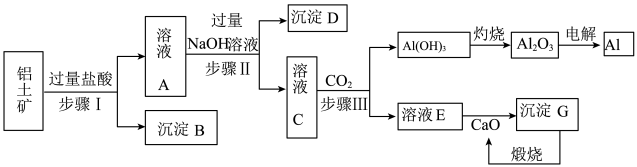
(1)溶液A中含的阳离子主要有________ .
(2)写出步骤II生成溶液C 的离子方程式________ ,步骤I、II、III都要用到的分离方法是________ .
(3)生产过程中,除CaO可以循环使用外,还可以循环使用的物质有________ (填化学式).
(4)生产中曾用铝与氧化铁的混合物形成铝热剂发生铝热反应焊接钢轨(提示:反应中能生成铁单质),则铝与氧化铁在高温下发生反应的化学方程式为:________ .
(5)经分析,a吨铝土矿可以冶炼出b吨的铝(假设各生产环节中无损耗),则原铝土矿中Al2O3的纯度(质量分数)________ (用含a、b的最简式表示).

(1)溶液A中含的阳离子主要有
(2)写出步骤II生成溶液C 的离子方程式
(3)生产过程中,除CaO可以循环使用外,还可以循环使用的物质有
(4)生产中曾用铝与氧化铁的混合物形成铝热剂发生铝热反应焊接钢轨(提示:反应中能生成铁单质),则铝与氧化铁在高温下发生反应的化学方程式为:
(5)经分析,a吨铝土矿可以冶炼出b吨的铝(假设各生产环节中无损耗),则原铝土矿中Al2O3的纯度(质量分数)
19-20高一下·河南漯河·期末 查看更多[4]
更新时间:2020-08-28 09:35:33
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】CoC2O4是制备氧化钴和金属钴的原料。一种利用含钴废料(主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、CaO、MgO、碳及有机物等)制取CoC2O4的工艺流程如下:
(1)为了加快“碱浸”速率,可采用的方法有______ (写两种)。反应的主要化学方程式为______ 。
(2)“钴浸出”过程中加入Na2SO3的作用是______ 。
(3)“除杂1”过程中,在40~50℃加入H2O2,写出加入H2O2反应的主要离子方程式:______ 。
(4)“除杂2”可将钙、镁离子转化为沉淀过滤除去,若所得滤液中c(Ca2+ )=1.0×10-5mol/L,则滤液中c(Mg2+ )为______ [已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10]。
(5)萃取剂对金属离子的萃取率与pH的关系如图所示,经过萃取可除去Mn2+,则控制溶液的pH范围是______ (填字母)。

A.1.0~2.0 B.2.0~3.0 C.3.0~3.5

(1)为了加快“碱浸”速率,可采用的方法有
(2)“钴浸出”过程中加入Na2SO3的作用是
(3)“除杂1”过程中,在40~50℃加入H2O2,写出加入H2O2反应的主要离子方程式:
(4)“除杂2”可将钙、镁离子转化为沉淀过滤除去,若所得滤液中c(Ca2+ )=1.0×10-5mol/L,则滤液中c(Mg2+ )为
(5)萃取剂对金属离子的萃取率与pH的关系如图所示,经过萃取可除去Mn2+,则控制溶液的pH范围是

A.1.0~2.0 B.2.0~3.0 C.3.0~3.5
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】某混合物甲中含有明矾[KAl(SO4)2]、Al2O3和Fe2O3在一定条件下由甲可实现如图所示的物质之间的转化:

请回答下列问题:
(1)写出A,B,D的化学式:A___ ,B___ ,D____ 。
(2)试剂a最好用___ (填名称)。
(3)写出反应①的离子方程式:___ 。
(4)固体E可以作为复合性的化学肥料,E中所含物质的化学式为___ 。

请回答下列问题:
(1)写出A,B,D的化学式:A
(2)试剂a最好用
(3)写出反应①的离子方程式:
(4)固体E可以作为复合性的化学肥料,E中所含物质的化学式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐3】工业上用铝土矿(主要成分为A12O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下:

(1)试剂X是_______________ ,过滤操作的主要玻璃仪器有烧杯、漏斗、_____ 。为了提高经济效益,滤渣还可以用来________ (写一种)。
(2)写出反应②的离子方程式__________________ 。
(3)工业上还可以用提取到的Al2O3为原料,与焦炭、氯气加热制备无水氯化铝,当生成1molAlCl3时消耗0.75mol焦炭,写出发生反应的化学方程式_____________ 。

(1)试剂X是
(2)写出反应②的离子方程式
(3)工业上还可以用提取到的Al2O3为原料,与焦炭、氯气加热制备无水氯化铝,当生成1molAlCl3时消耗0.75mol焦炭,写出发生反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】铝土矿【主要成分为Al2O3,还含有SiO2(不溶于水和酸)、Fe2O3】是工业上制备氧化铝的主要原料。工业上提取氧化铝的工艺流程如下:

(1)沉淀A、B的成分分别是__________ 、__________ ;步骤②中的试剂a是__________ ;(以上均填化学式)
(2)试写出步骤③中发生反应的离子方式__________ 、__________ ;

(1)沉淀A、B的成分分别是
(2)试写出步骤③中发生反应的离子方式
您最近一年使用:0次
【推荐2】工业上用铝土矿(主要成分为Al2O3,含有少量SiO2、FeO∙xFe2O3等杂质)制取铝的一种工艺流程示意图如下:

已知:Al2O3+Na2CO3 2NaAlO2+CO2↑
2NaAlO2+CO2↑
(1)“焙烧”步骤中,不能使用陶瓷坩埚的原因是_________ ;
(2)“滤渣1”中的主要金属元素为_______ ;“滤渣2”成分的化学式为________ ;不能用二氧化碳代替硫酸溶液的原因是_________ ;
(3)写出向“滤液2”滴加氨水至过量的主要的离子反应方程式__________ ;
(4)写出工业冶炼铝的化学反应方程式__________ ;
(5)若现在有at铝土矿,其中铝元素的质量分数为10.8%,最终制得铝锭bkg,则该流程的产率为__________________ %(用含a、b的代数式表示,结果需化简)。

已知:Al2O3+Na2CO3
 2NaAlO2+CO2↑
2NaAlO2+CO2↑(1)“焙烧”步骤中,不能使用陶瓷坩埚的原因是
(2)“滤渣1”中的主要金属元素为
(3)写出向“滤液2”滴加氨水至过量的主要的离子反应方程式
(4)写出工业冶炼铝的化学反应方程式
(5)若现在有at铝土矿,其中铝元素的质量分数为10.8%,最终制得铝锭bkg,则该流程的产率为
您最近一年使用:0次
【推荐3】已知铝土矿的主要成分是 ,含有杂质
,含有杂质 (不溶于盐酸和水)、
(不溶于盐酸和水)、 .工业上从铝土矿中提取铝可采用如图工艺流程:
.工业上从铝土矿中提取铝可采用如图工艺流程:

请回答下列问题:
(1)由物质M制取铝的化学方程式为_______ ;
(2)溶液A转化为溶液D发生的离子方程式为_______ ;
(3)溶液D中通入过量CO2生成沉淀F的离子方程式为_______ ;
(4)沉淀C的成分是_______ ,逐滴向少量沉淀C中加入HI至沉淀全部溶解,所得产物能使淀粉溶液变_______ 色。
 ,含有杂质
,含有杂质 (不溶于盐酸和水)、
(不溶于盐酸和水)、 .工业上从铝土矿中提取铝可采用如图工艺流程:
.工业上从铝土矿中提取铝可采用如图工艺流程:
请回答下列问题:
(1)由物质M制取铝的化学方程式为
(2)溶液A转化为溶液D发生的离子方程式为
(3)溶液D中通入过量CO2生成沉淀F的离子方程式为
(4)沉淀C的成分是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】氯化亚铜(CuCl)广泛应用于冶金、电镀、医药等行业。制备流程如下,已知下列流程中“反应”发生的化学变化是2CuCl2+Na2SO3=2CuCl↓+2NaCl+SO3,回答下列问题:

(1)“滤液1”中除了Na+、SO 外,还存在较多的离子是
外,还存在较多的离子是_________ (写离子符号)。
(2)“一系列操作”的名称是_________ 。
(3)本流程中可以循环利用的物质(水除外)是_________ (填化学式)。
(4)80gCuSO4与足量NaCl经上述制备流程,可生成的CuCl最多是_________ g。

(1)“滤液1”中除了Na+、SO
 外,还存在较多的离子是
外,还存在较多的离子是(2)“一系列操作”的名称是
(3)本流程中可以循环利用的物质(水除外)是
(4)80gCuSO4与足量NaCl经上述制备流程,可生成的CuCl最多是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】铝氢化钠(NaAIH4)是有机合成的重要还原剂,工业上常用铝土矿(主要成分为Al2O3,含有Fe2O3杂质)为原料制备铝氢化钠,其制备工艺流程如图:

已知:AlO +HCO
+HCO +H2O=Al(OH)3↓+CO
+H2O=Al(OH)3↓+CO 。
。
回答下列问题:
(1)“碱浸”前“粉碎”的目的是_______ 。
(2)“碱浸”时发生反应的离子方程式为_______ 。
(3)“滤渣”的主要成分为_______ (填化学式),过滤时用到的主要玻璃仪器有_______ 。
(4)“反应III”中每生成0.1molNaAlH4,生成另一种产物的质量为_______ g。

已知:AlO
 +HCO
+HCO +H2O=Al(OH)3↓+CO
+H2O=Al(OH)3↓+CO 。
。回答下列问题:
(1)“碱浸”前“粉碎”的目的是
(2)“碱浸”时发生反应的离子方程式为
(3)“滤渣”的主要成分为
(4)“反应III”中每生成0.1molNaAlH4,生成另一种产物的质量为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】硫酸渣是硫酸生产过程中产生的固体废料,主要化学成分有 、
、 、
、 等。
等。
I.研究人员可利用硫酸渣制备高纯度硫酸亚铁晶体,流程如下图所示:
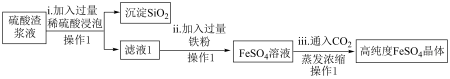
已知: 是难溶于水的酸性氧化物。
是难溶于水的酸性氧化物。
(1)操作1是______ 。
(2)步骤ii中涉及反应的离子方程式有_______ 、_________ 。
(3)步骤iii中的 的作用是
的作用是______ 。
(4)取少量高纯度 晶体配成溶液,
晶体配成溶液,_______ (操作和现象),证明该晶体中不含 。
。
Ⅱ.研究人员还可利用硫酸渣与含氯废气( 和HCl混合气)来制备絮凝剂聚合氯化铁,流程如下图所示:
和HCl混合气)来制备絮凝剂聚合氯化铁,流程如下图所示:
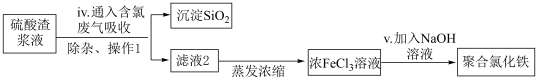
已知:聚合氯化铁的一种形式为 。
。
(5)写出以下物质中加点元素 的化合价: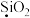
_____ ,
_____ 。
(6)下列关于步骤iv中含氯废气作用的说法中,不正确的是___________ 。
a.盐酸中 作用是使FeO、
作用是使FeO、 溶解
溶解
b.氯气参与反应的离子方程式为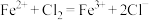
c.盐酸与氯气中的氯元素均转移到 中
中
(7)补全步骤v中涉及到反应的化学方程式______ 。
 。
。
 、
、 、
、 等。
等。I.研究人员可利用硫酸渣制备高纯度硫酸亚铁晶体,流程如下图所示:

已知:
 是难溶于水的酸性氧化物。
是难溶于水的酸性氧化物。(1)操作1是
(2)步骤ii中涉及反应的离子方程式有
(3)步骤iii中的
 的作用是
的作用是(4)取少量高纯度
 晶体配成溶液,
晶体配成溶液, 。
。Ⅱ.研究人员还可利用硫酸渣与含氯废气(
 和HCl混合气)来制备絮凝剂聚合氯化铁,流程如下图所示:
和HCl混合气)来制备絮凝剂聚合氯化铁,流程如下图所示:
已知:聚合氯化铁的一种形式为
 。
。(5)写出以下物质中
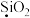

(6)下列关于步骤iv中含氯废气作用的说法中,不正确的是
a.盐酸中
 作用是使FeO、
作用是使FeO、 溶解
溶解b.氯气参与反应的离子方程式为
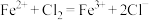
c.盐酸与氯气中的氯元素均转移到
 中
中(7)补全步骤v中涉及到反应的化学方程式
 。
。
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】MgO、Al2O3都是常用的耐火材料,某研究小组取100kg含60%Al的报废汽车的镁铝合金材料来制备MgO、Al2O3,其中甲可由溶液B转化再生,工艺流程如图所示。
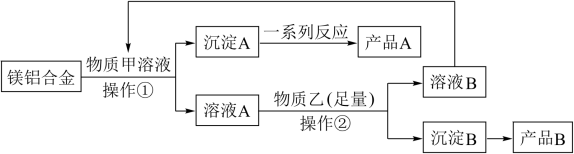
请回答下列问题:
(1)下列对合金材料的说法正确的是___________ (填字母代号)。
A.合金是金属与金属熔合而成的混合物
B.合金的熔点比成分金属更高
C.合金的硬度等机械性能优于成分金属
D.氧化铝熔点高,故可以用氧化铝坩埚熔融氢氧化钠
(2)物质甲是___________ (化学式),产品A是___________ (化学式)。
(3)操作①、②所需的玻璃仪器是___________ 。
(4)足量物质乙与溶液A发生的主要反应的离子方程式为___________ 。
(5)假设不计损耗,可得产品B的质量为___________ kg。(保留一位小数)

请回答下列问题:
(1)下列对合金材料的说法正确的是
A.合金是金属与金属熔合而成的混合物
B.合金的熔点比成分金属更高
C.合金的硬度等机械性能优于成分金属
D.氧化铝熔点高,故可以用氧化铝坩埚熔融氢氧化钠
(2)物质甲是
(3)操作①、②所需的玻璃仪器是
(4)足量物质乙与溶液A发生的主要反应的离子方程式为
(5)假设不计损耗,可得产品B的质量为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】如图是某研究性学习小组设计制取氯气并以氯气为反应物进行特定反应的装置。

(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关反应的化学方程式为_______________________ 。装置B中饱和食盐水的作用是____________________ 。要将C装置接入B和D之间,正确的接法是a→_________ →________ →d。
(2)实验开始先点燃A处的酒精灯,打开活塞K,让Cl2充满整个装置,再点燃D处的酒精灯。Cl2通过C装置后进入D,D装置内盛有炭粉,发生氧化还原反应,生成CO2和HCl(g),发生反应的化学方程式为________________ 。为了使C装置发挥更好的作用,可向烧杯中加入浓硫酸,加入浓硫酸的作用是____________________ 。
(3)D处反应完毕后,关闭弹簧夹K,移去两个酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是_____________________________________ ,B的作用是__________________________ 。

(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关反应的化学方程式为
(2)实验开始先点燃A处的酒精灯,打开活塞K,让Cl2充满整个装置,再点燃D处的酒精灯。Cl2通过C装置后进入D,D装置内盛有炭粉,发生氧化还原反应,生成CO2和HCl(g),发生反应的化学方程式为
(3)D处反应完毕后,关闭弹簧夹K,移去两个酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】电子工业中用过量的FeCl3溶液溶解电路板中的铜箔时,会产生大量废液。由该废液回收铜并得到净水剂(FeCl3•6H2O)的步骤如下:
I.在废液中加入过量铁粉,过滤;
II.向I的滤渣中加入过量试剂A,充分反应后,过滤,得到铜;
III.合并I和II中的滤液,通入足量氯气;
IV.……,得到FeCl3•6H2O晶体。
(1)用FeCl3溶液腐蚀铜箔的离子方程式是_____________ ;
(2)试剂A是______ ;
(3)取少量步骤III所得的溶液于试管中,能够证明通入氯气足量的是______ ;
a. 检验Cl2的存在 b. 检验Fe3+的存在 c. 检验Fe2+的不存在
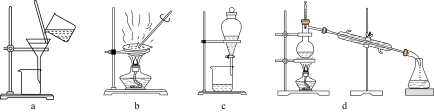
(4)完成步骤IV需要用到的实验装置是______ (填字母)。
I.在废液中加入过量铁粉,过滤;
II.向I的滤渣中加入过量试剂A,充分反应后,过滤,得到铜;
III.合并I和II中的滤液,通入足量氯气;
IV.……,得到FeCl3•6H2O晶体。
(1)用FeCl3溶液腐蚀铜箔的离子方程式是
(2)试剂A是
(3)取少量步骤III所得的溶液于试管中,能够证明通入氯气足量的是
a. 检验Cl2的存在 b. 检验Fe3+的存在 c. 检验Fe2+的不存在
(4)完成步骤IV需要用到的实验装置是

您最近一年使用:0次



