研究K、Ca、Fe、As、T等第四周期元素对生产、生活有重要意义。回答下列问题:
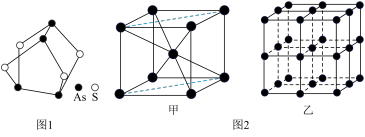
(1)我国中医把雄黄作为解毒剂,用来治疗癣疥、中风等。雄黄的结构如图1.雄黄分子中孤电子对数与成键电子对数之比为___ ,砷酸常用于制备颜料、砷酸盐、杀虫剂等,则AsO 的空间构型是
的空间构型是___ 。
(2)已知KCl、MgO、CaO、TiN的晶体于NaCl的晶体结构相似,且三种离子晶体的晶格能数据如表所示。
①Ti3+的电子排布式为___ 。
②KCl、CaO、TiN三种离子晶体熔点由高到低的顺序为___ ,原因是___ 。
(3)Fe的一种晶体结构如图2甲、乙所示,若按甲虚线方向切割乙,得到的截面图中正确的是___ 。(填字母标号)假设铁原子的半径是rcm,铁的相对原子质量为M,则该晶体的密度为___ g/cm3。(列式即可,设阿伏加 德罗常数的值为NA)


(1)我国中医把雄黄作为解毒剂,用来治疗癣疥、中风等。雄黄的结构如图1.雄黄分子中孤电子对数与成键电子对数之比为
 的空间构型是
的空间构型是(2)已知KCl、MgO、CaO、TiN的晶体于NaCl的晶体结构相似,且三种离子晶体的晶格能数据如表所示。
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ•mol-1 | 786 | 715 | 3401 |
①Ti3+的电子排布式为
②KCl、CaO、TiN三种离子晶体熔点由高到低的顺序为
(3)Fe的一种晶体结构如图2甲、乙所示,若按甲虚线方向切割乙,得到的截面图中正确的是

2020·山东日照·模拟预测 查看更多[2]
更新时间:2020-08-28 19:11:38
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)下列化合物含有手性碳的是___________。
(2)图一~图三是几种物质的微观结构图:
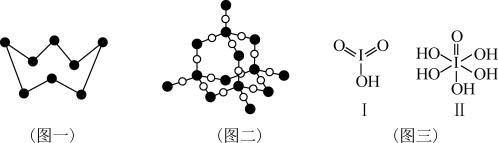
①图一是 ,其晶体类型为
,其晶体类型为___________ 。
②图二是 的微观结构,其中Si原子与
的微观结构,其中Si原子与 键的数目之比为
键的数目之比为___________ ,最小的环上有___________ 个原子。
③图三为碘酸 和高碘酸
和高碘酸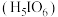 的结构图,请比较二者酸性强弱:
的结构图,请比较二者酸性强弱:
___________ 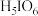 。(选填“>”“<”或“=”)。
。(选填“>”“<”或“=”)。
(3)下列过程中,化学反应速率的增大对人类有益的是___________。
(4)冰化成水的过程中,其焓变、熵变正确的是___________。
(1)下列化合物含有手性碳的是___________。
A.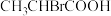 | B.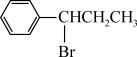 |
C.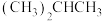 | D.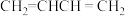 |

①图一是
 ,其晶体类型为
,其晶体类型为②图二是
 的微观结构,其中Si原子与
的微观结构,其中Si原子与 键的数目之比为
键的数目之比为③图三为碘酸
 和高碘酸
和高碘酸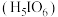 的结构图,请比较二者酸性强弱:
的结构图,请比较二者酸性强弱:
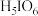 。(选填“>”“<”或“=”)。
。(选填“>”“<”或“=”)。(3)下列过程中,化学反应速率的增大对人类有益的是___________。
| A.金属的腐蚀 | B.塑料的老化 | C.食物的腐败 | D.氨的合成 |
A.  | B.  |
C.  | D.  |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】GaF3的熔点高于1000℃,GaCl3的熔点为77.9℃,其原因是________________________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】非血红素铁是食物中铁元素存在的形式之一,主要是三价铁与蛋白质和羧酸结合成络合物。
(1)Fe2+基态核外电子排布式为________ 。
(2)C、N、O原子的电负性由大到小的顺序为________ 。
(3)乙酸分子中C原子轨道杂化类型为________ 。乙酸的沸点比甲酸甲酯(HCOOCH3)的高,其主要原因是________ 。
(4)把氯气通入黄血盐(K4[Fe(CN)6])溶液中,得到赤血盐(K3[Fe(CN)6]),写出该变化对应的化学方程式:____________________ 。
(5)FeO晶胞结构如右图所示,FeO 晶体中Fe2+周围等距离最近的 Fe2+有________ 个。

(1)Fe2+基态核外电子排布式为
(2)C、N、O原子的电负性由大到小的顺序为
(3)乙酸分子中C原子轨道杂化类型为
(4)把氯气通入黄血盐(K4[Fe(CN)6])溶液中,得到赤血盐(K3[Fe(CN)6]),写出该变化对应的化学方程式:
(5)FeO晶胞结构如右图所示,FeO 晶体中Fe2+周围等距离最近的 Fe2+有

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】碳、氮元素及其化合物与生产、生活密切相关,回答下列问题。
(1)K3[Fe(CN)6]中Fe3+与CN-之间的作用为___ ,该化学键能够形成的原因是___ 。
(2)某有机物的结构简式为 。该有机物分子中采取sp3杂化的原子对应元素的电负性由大到小的顺序为
。该有机物分子中采取sp3杂化的原子对应元素的电负性由大到小的顺序为___ 。
(3)乙二胺(H2NCH2CH2NH2)分子中氮原子杂化类型为___ 。
(4)NH4Cl中阳离子中心原子的价层电子对数为___ ,该物质中不含有___ 。
A.离子键 B.极性共价键 C.非极性共价键 D.配位键 E.σ键 F.π键
(5)NCl3的立体构型为___ ,其中心原子的杂化轨道类型为___ 。
(1)K3[Fe(CN)6]中Fe3+与CN-之间的作用为
(2)某有机物的结构简式为
 。该有机物分子中采取sp3杂化的原子对应元素的电负性由大到小的顺序为
。该有机物分子中采取sp3杂化的原子对应元素的电负性由大到小的顺序为(3)乙二胺(H2NCH2CH2NH2)分子中氮原子杂化类型为
(4)NH4Cl中阳离子中心原子的价层电子对数为
A.离子键 B.极性共价键 C.非极性共价键 D.配位键 E.σ键 F.π键
(5)NCl3的立体构型为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】ZnGeP2和KTiOPO4都是非线性光学晶体材料,在激光技术方面有广泛用途。请回答下列问题:
(1)O、P、K、Zn按电负性由大到小的顺序排列为___________ 。
(2)H2O、PH3、KH按熔点由高到低的顺序排列为___________ ,熔点差异的原因:___________ 。
(3)以Zn为顶点的ZnGeP2晶胞结构如图所示。

①Zn的配位数为___________ 。
②以Ge为顶点的晶胞中,Zn原子位于___________ 。
③原子A、C的坐标参数分别为(1, ,
, )、(0,0,0),则原子B的坐标参数为
)、(0,0,0),则原子B的坐标参数为___________ 。
(1)O、P、K、Zn按电负性由大到小的顺序排列为
(2)H2O、PH3、KH按熔点由高到低的顺序排列为
(3)以Zn为顶点的ZnGeP2晶胞结构如图所示。

①Zn的配位数为
②以Ge为顶点的晶胞中,Zn原子位于
③原子A、C的坐标参数分别为(1,
 ,
, )、(0,0,0),则原子B的坐标参数为
)、(0,0,0),则原子B的坐标参数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】第ⅣA族元素及其化合物在生产、生活中应用广泛。回答下列问题:
(1)基态锗原子的价层电子轨道表示式为______ ,第ⅣA族元素位于______ 区。
(2) 的电负性比
的电负性比 大,其主要原因是
大,其主要原因是_________________ 。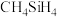 、
、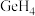 的稳定性依次减弱,其主要原因是
的稳定性依次减弱,其主要原因是______________________ 。
(3) 的VSEPR模型名称为
的VSEPR模型名称为________________________________ 。
(4)碳化硅( )熔点为2700°C,常作砂轮磨料,用于切割金属。由此推知,碳化硅晶体类型为
)熔点为2700°C,常作砂轮磨料,用于切割金属。由此推知,碳化硅晶体类型为______ 。
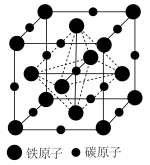
(5)铁和碳能形成如图所示的晶胞。它可以看成是铁晶胞中插入若干个碳原子,晶胞体积不变。铁碳晶体的化学式为______ ,铁晶体转化为铁碳晶体时晶体密度净增______ %(结果保留3位有效数字)。
(1)基态锗原子的价层电子轨道表示式为
(2)
 的电负性比
的电负性比 大,其主要原因是
大,其主要原因是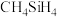 、
、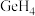 的稳定性依次减弱,其主要原因是
的稳定性依次减弱,其主要原因是(3)
 的VSEPR模型名称为
的VSEPR模型名称为(4)碳化硅(
 )熔点为2700°C,常作砂轮磨料,用于切割金属。由此推知,碳化硅晶体类型为
)熔点为2700°C,常作砂轮磨料,用于切割金属。由此推知,碳化硅晶体类型为(5)铁和碳能形成如图所示的晶胞。它可以看成是铁晶胞中插入若干个碳原子,晶胞体积不变。铁碳晶体的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】如图表示两种晶体的微观结构:
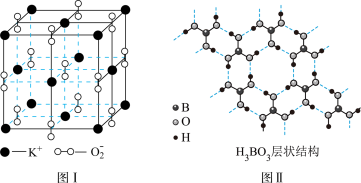
试回答下列有关问题:
(1)高温下,超氧化钾晶体呈立方体结构。晶体中氧的化合价部分为0价,部分为-2价。图I为超氧化钾晶体的一个晶胞(晶体中最小的重复单元)。则晶体中,与每个K+距离最近的K+有_________ 个,0价氧原子与-2价氧原子的数目比为_________ ;
(2)正硼酸(H3BO3)是一种片层结构的白色晶体,层内的H3BO3分子通过氢键相连(如图II)。下列有关说法正确的有_________ 。
①正硼酸晶体属于原子晶体
②H3BO3分子的稳定性与氢键有关
③在H3BO3分子中各原子未能都满足8e-稳定结构
④含1molH3BO3的晶体中有3mol氢键
⑤含1molH3BO3的晶体中有3mol极性共价键
⑥晶体中每个B与相邻的3个O共平面

试回答下列有关问题:
(1)高温下,超氧化钾晶体呈立方体结构。晶体中氧的化合价部分为0价,部分为-2价。图I为超氧化钾晶体的一个晶胞(晶体中最小的重复单元)。则晶体中,与每个K+距离最近的K+有
(2)正硼酸(H3BO3)是一种片层结构的白色晶体,层内的H3BO3分子通过氢键相连(如图II)。下列有关说法正确的有
①正硼酸晶体属于原子晶体
②H3BO3分子的稳定性与氢键有关
③在H3BO3分子中各原子未能都满足8e-稳定结构
④含1molH3BO3的晶体中有3mol氢键
⑤含1molH3BO3的晶体中有3mol极性共价键
⑥晶体中每个B与相邻的3个O共平面
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】碳和硅是自然界中大量存在的元素,硅及其化合物是工业上最重要的材料。设NA代表阿伏加德罗常数的值。粗硅的制备方法有两种:
方法一:
方法二:
(1)基态Si原子中存在_______ 对自旋状态相反的电子,基态Mg原子的最外层电子的电子轮廓图是_______ 。
(2) 晶胞(如图1)可理解成将金刚石晶胞(如图2)中的C原子置换成Si原子,然后在Si—Si键中间插入O原子而形成。
晶胞(如图1)可理解成将金刚石晶胞(如图2)中的C原子置换成Si原子,然后在Si—Si键中间插入O原子而形成。
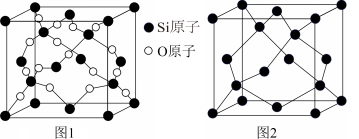
①推测 晶胞O—Si—O的键角为
晶胞O—Si—O的键角为_______ 。
② 晶胞中含有
晶胞中含有_______ 个Si原子和_______ 个O原子。
③假设金刚石晶胞的边长为apm,试计算该晶胞的密度为_______  (写出表达式即可)。
(写出表达式即可)。
方法一:

方法二:

(1)基态Si原子中存在
(2)
 晶胞(如图1)可理解成将金刚石晶胞(如图2)中的C原子置换成Si原子,然后在Si—Si键中间插入O原子而形成。
晶胞(如图1)可理解成将金刚石晶胞(如图2)中的C原子置换成Si原子,然后在Si—Si键中间插入O原子而形成。
①推测
 晶胞O—Si—O的键角为
晶胞O—Si—O的键角为②
 晶胞中含有
晶胞中含有③假设金刚石晶胞的边长为apm,试计算该晶胞的密度为
 (写出表达式即可)。
(写出表达式即可)。
您最近一年使用:0次

 =1.414;结果保留小数点后两位),每个Mg2+周围具有该距离的Mg2+个数为
=1.414;结果保留小数点后两位),每个Mg2+周围具有该距离的Mg2+个数为


