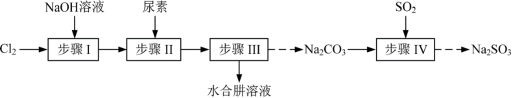
亚硝酸钠可使肉制品色泽粉红,外观上好看诱人,大量食用会致癌。
(1)NaNO2俗称“工业盐”,其外观与食盐相似,误食会中毒,可通过化学实验加以鉴别。如向NaNO2的酸性溶液中加入KI固体,析出的碘单质可以使淀粉溶液变蓝色,据此检验 。
。
①该反应中被氧化的元素是________ 。
②完成下列反应的化学方程式并配平:NaNO2+KI+H2SO4= + +I2+NO↑+ ,________ 。
③标准状况下,该反应中每转移1mol e-,生成气体的体积是________ 。
(2)硝酸工业生产中的尾气可用纯碱溶液吸收,有关的化学反应为:2NO2+Na2CO3=NaNO2+NaNO3+CO2↑。每产生33.6L(标准状况下)CO2,吸收液质量将增加________ g。
(1)NaNO2俗称“工业盐”,其外观与食盐相似,误食会中毒,可通过化学实验加以鉴别。如向NaNO2的酸性溶液中加入KI固体,析出的碘单质可以使淀粉溶液变蓝色,据此检验
 。
。①该反应中被氧化的元素是
②完成下列反应的化学方程式并配平:NaNO2+KI+H2SO4= + +I2+NO↑+ ,
③标准状况下,该反应中每转移1mol e-,生成气体的体积是
(2)硝酸工业生产中的尾气可用纯碱溶液吸收,有关的化学反应为:2NO2+Na2CO3=NaNO2+NaNO3+CO2↑。每产生33.6L(标准状况下)CO2,吸收液质量将增加
更新时间:2020-09-03 06:18:12
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】一定条件下Fe(OH)3与KClO在KOH溶液中反应可制得K2FeO4。生成0.1molK2FeO4转移的电子的物质的量_______ mol。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】向100 mL 浓度均为1 mol·L-1的Fe2(SO4)3和CuSO4的混合溶液中加入一定量铁粉,充分反应后针对下列情况填空,忽略溶液体积的变化。(已知:氧化性Fe3+>Cu2+>Fe2+)
(1)反应完毕后,无固体沉积物存在,则溶液中一定含有的阳离子为___________ 。
(2)无固体沉积物存在时溶液中发生反应的离子方程为___________ 。
(3)该溶液最多能够溶解铁粉的质量为___________ g。
(4)当Cu2+恰好反应后溶液中溶质的物质的量浓度为___________ mol·L-1。
(1)反应完毕后,无固体沉积物存在,则溶液中一定含有的阳离子为
(2)无固体沉积物存在时溶液中发生反应的离子方程为
(3)该溶液最多能够溶解铁粉的质量为
(4)当Cu2+恰好反应后溶液中溶质的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)湿法制各高铁酸钾(K2FeO4)的反应体系中有六种粒子:Fe(OH)3、ClO-、OH-、FeO42—、Cl-、H2O。
①写出并配平湿法制高铁酸钾反应的离子方程式:______________________________
②每生成l mol FeO42-转移__________ mol电子,若反应过程中转移了0.3 mol电子,则还原产物的物质的量为____ mol。
③低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4)原因是__ 。
(2)工业上从海水中提取单质溴可采用如下方法:
①向海水中通入Cl2将海水中溴化物氧化,其离子方程式为____ 。
②向上述混合液中吹入热空气,将生成的溴吹出,用纯碱溶液吸收,其化学方程式为__ 。
③将②所得溶液用H2SO4酸化,使NaBr、NaBrO3中的溴转化为单质溴,再用有机溶剂提取溴后,还可得到副产品Na2SO4。这一过程可用化学方程式表示为____ 。
①写出并配平湿法制高铁酸钾反应的离子方程式:
②每生成l mol FeO42-转移
③低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4)原因是
(2)工业上从海水中提取单质溴可采用如下方法:
①向海水中通入Cl2将海水中溴化物氧化,其离子方程式为
②向上述混合液中吹入热空气,将生成的溴吹出,用纯碱溶液吸收,其化学方程式为
③将②所得溶液用H2SO4酸化,使NaBr、NaBrO3中的溴转化为单质溴,再用有机溶剂提取溴后,还可得到副产品Na2SO4。这一过程可用化学方程式表示为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】铁是应用最广泛的金属,在工农业生产和生活中占有重要的地位。运用铁及其化合物的知识,完成下列问题。
(1)苹果汁中含有 ,它是人们喜欢的一种补铁饮料,现榨苹果汁在空气中由浅绿色变为棕黄色的原因是
,它是人们喜欢的一种补铁饮料,现榨苹果汁在空气中由浅绿色变为棕黄色的原因是___________ 。
(2)中国古代四大发明之一的指南针是由天然磁石制成的,其主要成分是___________ (填化学式)。氧化铁俗称铁红,常用作___________ ;氧化铁与氢碘酸反应的离子方程式为___________ 。
(3)电子工业需要用 的
的 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出 溶液与铜反应的离子方程式:
溶液与铜反应的离子方程式:___________ 。
(4)高铁酸钾( )是一种新型、高效、多功能水处理剂。已知:
)是一种新型、高效、多功能水处理剂。已知:
① 与
与 在强碱性条件下反应可制取
在强碱性条件下反应可制取 ;
;
② 具有强氧化性,在酸性或中性溶液中迅速产生氧气:
具有强氧化性,在酸性或中性溶液中迅速产生氧气: ;
;
制取 的离子方程式为
的离子方程式为______ , 作水处理剂的原因
作水处理剂的原因______ 。
(1)苹果汁中含有
 ,它是人们喜欢的一种补铁饮料,现榨苹果汁在空气中由浅绿色变为棕黄色的原因是
,它是人们喜欢的一种补铁饮料,现榨苹果汁在空气中由浅绿色变为棕黄色的原因是(2)中国古代四大发明之一的指南针是由天然磁石制成的,其主要成分是
(3)电子工业需要用
 的
的 溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出
溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出 溶液与铜反应的离子方程式:
溶液与铜反应的离子方程式:(4)高铁酸钾(
 )是一种新型、高效、多功能水处理剂。已知:
)是一种新型、高效、多功能水处理剂。已知:①
 与
与 在强碱性条件下反应可制取
在强碱性条件下反应可制取 ;
; ②
 具有强氧化性,在酸性或中性溶液中迅速产生氧气:
具有强氧化性,在酸性或中性溶液中迅速产生氧气: ;
;制取
 的离子方程式为
的离子方程式为 作水处理剂的原因
作水处理剂的原因
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】连二亚硫酸钠(Na2S2O4)又称保险粉,是印刷工业中重要的还原剂。某课题小组进行如下实验:
Ⅰ.查阅资料
①连二亚硫酸钠(Na2S2O4)是一种白色粉末,易溶于水,难溶于乙醇。
②2Na2S2O4+4HCl===4NaCl+S↓+3SO2↑+2H2O;
Na2S2O3+2HCl===2NaCl+S↓+SO2↑+H2O。
Ⅱ.制备方法
75 ℃时将甲酸钠和纯碱加入乙醇溶液中,通入SO2进行反应,完成其反应的化学方程式:
________ HCOONa+________ Na2CO3+________ ________ Na2S2O4+________ CO2+______
冷却至40~50 ℃,过滤,用________ 洗涤,干燥制得Na2S2O4。
Ⅲ.Na2S2O4的性质
(1)Na2S2O4溶液在空气中易被氧化。课题小组测定0.050 mol·L-1 Na2S2O4溶液在空气中pH变化如图所示:
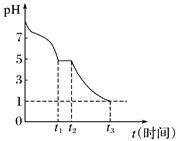
0~t1段主要生成HSO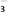 ,根据pH变化图,HSO
,根据pH变化图,HSO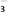 的电离程度
的电离程度________ (填“<”或“>”)水解程度。
0~t1段发生反应的离子方程式为_____________ 。
t3时溶液中存在的主要阴离子的符号是_________________ 。
(2)隔绝空气加热Na2S2O4固体完全分解;得到固体产物Na2SO3、Na2S2O3和________ (填化学式)气体。
请你设计实验验证产物有Na2S2O3存在,完成下表中内容。
(供选择的试剂:稀盐酸、稀硝酸、BaCl2溶液、KMnO4溶液)
Ⅰ.查阅资料
①连二亚硫酸钠(Na2S2O4)是一种白色粉末,易溶于水,难溶于乙醇。
②2Na2S2O4+4HCl===4NaCl+S↓+3SO2↑+2H2O;
Na2S2O3+2HCl===2NaCl+S↓+SO2↑+H2O。
Ⅱ.制备方法
75 ℃时将甲酸钠和纯碱加入乙醇溶液中,通入SO2进行反应,完成其反应的化学方程式:
冷却至40~50 ℃,过滤,用
Ⅲ.Na2S2O4的性质
(1)Na2S2O4溶液在空气中易被氧化。课题小组测定0.050 mol·L-1 Na2S2O4溶液在空气中pH变化如图所示:

0~t1段主要生成HSO
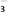 ,根据pH变化图,HSO
,根据pH变化图,HSO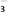 的电离程度
的电离程度0~t1段发生反应的离子方程式为
t3时溶液中存在的主要阴离子的符号是
(2)隔绝空气加热Na2S2O4固体完全分解;得到固体产物Na2SO3、Na2S2O3和
请你设计实验验证产物有Na2S2O3存在,完成下表中内容。
(供选择的试剂:稀盐酸、稀硝酸、BaCl2溶液、KMnO4溶液)
| 实验步骤(不要求写出具体操作过程) | 预期的实验现象和结论 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】某一反应体系中有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。 已知该反应中H2O2只发生如下过程:H2O2→O2
(1)该反应中的还原剂是______________ 。(填化学式)
(2)该反应中,发生还原反应的过程是________ →________ 。(填化学式)
(3)写出该反应的化学方程式,并用单线桥标出电子转移的方向和数目:____________________________________________________________ 。
(4)如反应转移了0.3 mol电子,则产生的气体在标准状况下体积为__________ 。
(5)反应8NH3+3Cl2=6NH4Cl+N2中,氧化剂与还原剂的物质的量之比是_________ 。
(6)KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2,还生成CO2和KHSO4等物质。写出该反应的化学方程式:______________________________________ 。
(1)该反应中的还原剂是
(2)该反应中,发生还原反应的过程是
(3)写出该反应的化学方程式,并用单线桥标出电子转移的方向和数目:
(4)如反应转移了0.3 mol电子,则产生的气体在标准状况下体积为
(5)反应8NH3+3Cl2=6NH4Cl+N2中,氧化剂与还原剂的物质的量之比是
(6)KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2,还生成CO2和KHSO4等物质。写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)湿法制各高铁酸钾(K2FeO4)的反应体系中有六种粒子:Fe(OH)3、ClO-、OH-、FeO42—、Cl-、H2O。
①写出并配平湿法制高铁酸钾反应的离子方程式:______________________________
②每生成l mol FeO42-转移__________ mol电子,若反应过程中转移了0.3 mol电子,则还原产物的物质的量为____ mol。
③低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4)原因是__ 。
(2)工业上从海水中提取单质溴可采用如下方法:
①向海水中通入Cl2将海水中溴化物氧化,其离子方程式为____ 。
②向上述混合液中吹入热空气,将生成的溴吹出,用纯碱溶液吸收,其化学方程式为__ 。
③将②所得溶液用H2SO4酸化,使NaBr、NaBrO3中的溴转化为单质溴,再用有机溶剂提取溴后,还可得到副产品Na2SO4。这一过程可用化学方程式表示为____ 。
①写出并配平湿法制高铁酸钾反应的离子方程式:
②每生成l mol FeO42-转移
③低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4)原因是
(2)工业上从海水中提取单质溴可采用如下方法:
①向海水中通入Cl2将海水中溴化物氧化,其离子方程式为
②向上述混合液中吹入热空气,将生成的溴吹出,用纯碱溶液吸收,其化学方程式为
③将②所得溶液用H2SO4酸化,使NaBr、NaBrO3中的溴转化为单质溴,再用有机溶剂提取溴后,还可得到副产品Na2SO4。这一过程可用化学方程式表示为
您最近一年使用:0次