某一反应体系中有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。 已知该反应中H2O2只发生如下过程:H2O2→O2
(1)该反应中的还原剂是______________ 。(填化学式)
(2)该反应中,发生还原反应的过程是________ →________ 。(填化学式)
(3)写出该反应的化学方程式,并用单线桥标出电子转移的方向和数目:____________________________________________________________ 。
(4)如反应转移了0.3 mol电子,则产生的气体在标准状况下体积为__________ 。
(5)反应8NH3+3Cl2=6NH4Cl+N2中,氧化剂与还原剂的物质的量之比是_________ 。
(6)KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2,还生成CO2和KHSO4等物质。写出该反应的化学方程式:______________________________________ 。
(1)该反应中的还原剂是
(2)该反应中,发生还原反应的过程是
(3)写出该反应的化学方程式,并用单线桥标出电子转移的方向和数目:
(4)如反应转移了0.3 mol电子,则产生的气体在标准状况下体积为
(5)反应8NH3+3Cl2=6NH4Cl+N2中,氧化剂与还原剂的物质的量之比是
(6)KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2,还生成CO2和KHSO4等物质。写出该反应的化学方程式:
更新时间:2019-12-01 11:37:23
|
相似题推荐
【推荐1】I.储氢纳米碳管研究成功体现了科技的进步。但用电弧法合成的碳纳米管常伴有大量的杂质——碳纳米颗粒。这种碳纳米颗粒可用氧化气化法提纯。其反应方程式为3C+2K2Cr2O7+8H2SO4=3CO2↑+2K2SO4+2Cr2(SO4) 3+8H2O。请回答下列问题:
(1)用双线桥法标明上述反应方程式中电子转移的方向和数目___________ 。
3C+2K2Cr2O7+8H2SO4=3CO2↑+2K2SO4+2Cr2(SO4) 3+8H2O。
(2)上述反应中氧化剂是___________ ,被氧化的元素是___________ (填元素符号) 。
(3)H2SO4在上述反应中表现出来的性质是___________(填标号)。
(4)请配平下列离子方程式___________ 。
___________Fe2++___________H++___________ =___________Fe3++___________N2O↑+___________H2O
=___________Fe3++___________N2O↑+___________H2O
II.已知:氮元素有-3、0、+1、+2、+3、+4和+5七种化合价,试据此判断下列六种化合物:①NO;②N2O3;③N2O4;④HNO3;⑤NH3;⑥N2O中:
(5)氮元素只能作还原剂的是___________ (填序号,下同)。
(6)可能是HNO2还原产物的是___________ 。
(7)不可能是N2的氧化产物是___________ 。
(8)已知CuO具有氧化性,能够和氨气反应生成两种单质,请写出在加热条件下CuO和NH3反应的化学方程式___________ 。
(1)用双线桥法标明上述反应方程式中电子转移的方向和数目
3C+2K2Cr2O7+8H2SO4=3CO2↑+2K2SO4+2Cr2(SO4) 3+8H2O。
(2)上述反应中氧化剂是
(3)H2SO4在上述反应中表现出来的性质是___________(填标号)。
| A.酸性 | B.氧化性 | C.氧化性和酸性 | D.还原性和酸性 |
___________Fe2++___________H++___________
 =___________Fe3++___________N2O↑+___________H2O
=___________Fe3++___________N2O↑+___________H2OII.已知:氮元素有-3、0、+1、+2、+3、+4和+5七种化合价,试据此判断下列六种化合物:①NO;②N2O3;③N2O4;④HNO3;⑤NH3;⑥N2O中:
(5)氮元素只能作还原剂的是
(6)可能是HNO2还原产物的是
(7)不可能是N2的氧化产物是
(8)已知CuO具有氧化性,能够和氨气反应生成两种单质,请写出在加热条件下CuO和NH3反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.请回答以下问题:
(1)等质量的两种气体 、
、 分子数之比为
分子数之比为___________ ,相同条件下密度之比为___________ 。
(2)已知CO、 混合气体的质量共12.0g,在标准状况下的体积为6.72L,则混合气体中CO的质量分数为
混合气体的质量共12.0g,在标准状况下的体积为6.72L,则混合气体中CO的质量分数为___________ 。
Ⅱ.用电弧法合成碳纳米管,常伴有大量杂质——碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,其反应方程式为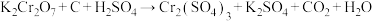 。
。
(3)配平该反应方程式:___________
(4)此反应的氧化产物为___________ 。
(5)要使10mL 1.0mol/L 溶液被还原至少要加入
溶液被还原至少要加入___________ mL 2.0mol/L的 溶液。
溶液。
(6)若产生6.72L (标准状况下)气体,该反应转移电子的物质的量为
(标准状况下)气体,该反应转移电子的物质的量为___________ mol。
(1)等质量的两种气体
 、
、 分子数之比为
分子数之比为(2)已知CO、
 混合气体的质量共12.0g,在标准状况下的体积为6.72L,则混合气体中CO的质量分数为
混合气体的质量共12.0g,在标准状况下的体积为6.72L,则混合气体中CO的质量分数为Ⅱ.用电弧法合成碳纳米管,常伴有大量杂质——碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,其反应方程式为
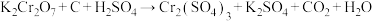 。
。(3)配平该反应方程式:
(4)此反应的氧化产物为
(5)要使10mL 1.0mol/L
 溶液被还原至少要加入
溶液被还原至少要加入 溶液。
溶液。(6)若产生6.72L
 (标准状况下)气体,该反应转移电子的物质的量为
(标准状况下)气体,该反应转移电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】实验所需的 可用
可用 和
和 溶液在稀
溶液在稀 中反应制得,离子反应方程式为
中反应制得,离子反应方程式为_______ 。
 可用
可用 和
和 溶液在稀
溶液在稀 中反应制得,离子反应方程式为
中反应制得,离子反应方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】油画所用颜料含有某种白色铅化物,此颜料置于空气中长时间后就会变成黑色PbS,从而使油画的色彩变暗,若用双氧水H2O2来清洗,则可将PbS变成PbSO4,从而使油画复原。上述清洗反应的化学方程式为 PbS+ 4H2O2 = PbSO4 + 4M(已配平)
(1)生成物M的化学式为_________________________
(2)在此反应中,PbS作_____________ 剂,H2O2作 _____________ 剂
(3)若发生转移的电子数目2mol时,参加反应的H2O2的质量为___________ 。
(1)生成物M的化学式为
(2)在此反应中,PbS作
(3)若发生转移的电子数目2mol时,参加反应的H2O2的质量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】铜的冶炼大致可分为①富集,将硫化物矿进行浮选;②焙烧,主要反应为2CuFeS2+4O2===Cu2S+3SO2+2FeO(炉渣);③制粗铜,在1 200 ℃发生的主要反应为2Cu2S+3O2===2Cu2O+2SO2,2Cu2O+Cu2S===6Cu+SO2↑;④电解精炼铜。
按要求填写下列问题:
(1)上述灼烧过程的尾气回收后可用来制________________________ 。
(2)上述过程中,由6 mol CuFeS2制取6 mol Cu时共消耗O2的物质的量:__________________ 。
(3)在反应2Cu2O+Cu2S===6Cu+SO2↑中,氧化产物与还原产物的物质的量之比:____________________ 。
(4)在反应2Cu2O+Cu2S===6Cu+SO2↑中,氧化剂为________ 、_________ 。
按要求填写下列问题:
(1)上述灼烧过程的尾气回收后可用来制
(2)上述过程中,由6 mol CuFeS2制取6 mol Cu时共消耗O2的物质的量:
(3)在反应2Cu2O+Cu2S===6Cu+SO2↑中,氧化产物与还原产物的物质的量之比:
(4)在反应2Cu2O+Cu2S===6Cu+SO2↑中,氧化剂为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题。
Ⅰ.已知某容器中发生了一个化学反应,反应体系存在 、
、 、
、 、
、 、
、 、
、 六种粒子。在反应过程中,溶液紫红色逐渐褪去。
六种粒子。在反应过程中,溶液紫红色逐渐褪去。
(1)写出该反应的离子方程式:___________ 。
(2)该反应中,氧化剂与还原剂的粒子个数之比为___________ 。
Ⅱ.高铁酸钠 是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为:
是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为: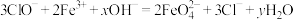 ,回答下列问题:
,回答下列问题:
(3)上述反应中的
___________ ,
___________ 。
(4)上述反应中氧化剂为___________ ;还原产物为___________ 。
(5)由上述反应可知,氧化性强弱:
___________  (填“>”或“<”,下同);还原性强弱:
(填“>”或“<”,下同);还原性强弱:
___________  。
。
(6)请用单线桥法表示该反应中电子的转移情况:___________ 。
Ⅰ.已知某容器中发生了一个化学反应,反应体系存在
 、
、 、
、 、
、 、
、 、
、 六种粒子。在反应过程中,溶液紫红色逐渐褪去。
六种粒子。在反应过程中,溶液紫红色逐渐褪去。(1)写出该反应的离子方程式:
(2)该反应中,氧化剂与还原剂的粒子个数之比为
Ⅱ.高铁酸钠
 是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为:
是一种新型绿色消毒剂,主要用于饮用水处理,工业上有多种制备高铁酸钠的方法,其中一种方法的化学反应原理可用离子方程式表示为: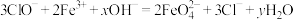 ,回答下列问题:
,回答下列问题:(3)上述反应中的


(4)上述反应中氧化剂为
(5)由上述反应可知,氧化性强弱:

 (填“>”或“<”,下同);还原性强弱:
(填“>”或“<”,下同);还原性强弱:
 。
。(6)请用单线桥法表示该反应中电子的转移情况:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】铁及其化合物在生产、生活中有及其重要的用途,请回答下列问题:
(1)FeCl3溶液呈黄色,FeCl3溶液的分散质是_________ ,分散剂是___________ 。
(2)Fe(OH)3是难溶于水的固体,那么分离Fe(OH)3与水的悬浊液常用的方法是_______
(3)Fe(OH)3胶体呈红褐色,具有良好的净水效果.由饱和FeCl3溶液制备Fe(OH)3胶体的方法是______________________ 。离子方程式是___________________________ 。
(4)鉴别FeCl3溶液和Fe(OH)3胶体,除了可通过观察颜色以外,还有的方法是__________ 。
(5)下列关于Fe(OH)3胶体和Fe(OH)3悬浊液的描述,正确的是_________
A.两者颜色相同 B.两者稳定性相同
C.两者的分子直径均大于100nm D.滴加稀盐酸后,两者现象完全相同
(6)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理,工业制备高铁酸钠有多种方法,其中一种方法的原理可用离子方程式表示为
3ClO—+2Fe3++10OH—= 2 +3Cl—+5H2O,则Na2FeO4中铁元素的化合价为
+3Cl—+5H2O,则Na2FeO4中铁元素的化合价为_______ ,该离子反应中氧化剂与还原剂的个数比为_____ ,生成1个高铁酸钠转移____ 个电子
(1)FeCl3溶液呈黄色,FeCl3溶液的分散质是
(2)Fe(OH)3是难溶于水的固体,那么分离Fe(OH)3与水的悬浊液常用的方法是
(3)Fe(OH)3胶体呈红褐色,具有良好的净水效果.由饱和FeCl3溶液制备Fe(OH)3胶体的方法是
(4)鉴别FeCl3溶液和Fe(OH)3胶体,除了可通过观察颜色以外,还有的方法是
(5)下列关于Fe(OH)3胶体和Fe(OH)3悬浊液的描述,正确的是
A.两者颜色相同 B.两者稳定性相同
C.两者的分子直径均大于100nm D.滴加稀盐酸后,两者现象完全相同
(6)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理,工业制备高铁酸钠有多种方法,其中一种方法的原理可用离子方程式表示为
3ClO—+2Fe3++10OH—= 2
 +3Cl—+5H2O,则Na2FeO4中铁元素的化合价为
+3Cl—+5H2O,则Na2FeO4中铁元素的化合价为
您最近一年使用:0次
【推荐2】NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。
(1)上述反应中氧化剂是__ ,还原性I-__ NO(填“>”或“<”)。
(2)根据上述反应,鉴别NaNO2和NaCl。可选用的物质有①水、②碘化钾淀粉试纸、③淀粉、④白酒、⑤食醋,你认为必须选用的物质有__ (填序号)。
(3)请配平以下化学方程式:__ Al+__ NaNO3+__ NaOH=__ NaAlO2+__ N2↑+_ H2O
若反应过程中转移5mol电子,则生成标准状况下N2的体积为__ L。
(1)上述反应中氧化剂是
(2)根据上述反应,鉴别NaNO2和NaCl。可选用的物质有①水、②碘化钾淀粉试纸、③淀粉、④白酒、⑤食醋,你认为必须选用的物质有
(3)请配平以下化学方程式:
若反应过程中转移5mol电子,则生成标准状况下N2的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】I.已知在溶液中可发生下列反应:
①Cl2+2NaBr=2NaCl+Br2
②Br2+2KI=2KBr+I2
③I2+Na2S=2NaI+S
(1)由此推断下列化学方程式书写错误的是________
A.Cl2+2NaI=2NaCl+I2B.I2+2KBr=2KI+Br2
C.Br2+Na2S=2NaBr+S↓D.Cl2+K2S=2KCl+S↓
II.高铁酸盐是常用的水处理剂。干法制备高铁酸钠(Na2FeO4)可利用Na2O2与FeSO4反应,产物还有硫酸钠、氧气和氧化钠,且反应时消耗的Na2O2与生成的O2的物质的量之比为6:1。
(2)请配平下述制备反应方程式。___________Na2O2+___________FeSO4═___________Na2FeO4+___________Na2SO4+___________O2↑+___________Na2O,___________
(3)反应物Na2O2的作用是___________ (填序号)。
A.氧化剂B.还原剂C.既是氧化剂也是还原剂D.既不是氧化剂也不是还原剂
(4)若生成2.24LO2(标准状况),则转移电子的数目为___________ 。
①Cl2+2NaBr=2NaCl+Br2
②Br2+2KI=2KBr+I2
③I2+Na2S=2NaI+S
(1)由此推断下列化学方程式书写错误的是
A.Cl2+2NaI=2NaCl+I2B.I2+2KBr=2KI+Br2
C.Br2+Na2S=2NaBr+S↓D.Cl2+K2S=2KCl+S↓
II.高铁酸盐是常用的水处理剂。干法制备高铁酸钠(Na2FeO4)可利用Na2O2与FeSO4反应,产物还有硫酸钠、氧气和氧化钠,且反应时消耗的Na2O2与生成的O2的物质的量之比为6:1。
(2)请配平下述制备反应方程式。___________Na2O2+___________FeSO4═___________Na2FeO4+___________Na2SO4+___________O2↑+___________Na2O,
(3)反应物Na2O2的作用是
A.氧化剂B.还原剂C.既是氧化剂也是还原剂D.既不是氧化剂也不是还原剂
(4)若生成2.24LO2(标准状况),则转移电子的数目为
您最近一年使用:0次



