高铁酸钾(K2FeO4)是一种既能杀菌、消毒,又能絮凝净水的水处理剂,工业制备高铁酸钾的反应离子方程式为Fe(OH)3+ClO-+OH-→ +Cl-+H2O(未配平)。下列有关说法不正确的是
+Cl-+H2O(未配平)。下列有关说法不正确的是
 +Cl-+H2O(未配平)。下列有关说法不正确的是
+Cl-+H2O(未配平)。下列有关说法不正确的是A.由上述反应可知,ClO-的氧化性强于 |
| B.高铁酸钾中铁显+6价 |
| C.上述反应中氧化剂和还原剂的物质的量之比为2∶3 |
| D.K2FeO4处理水时,不仅能消毒杀菌,而且生成的Fe3+与水反应形成Fe(OH)3胶体能吸附水中的悬浮杂质 |
更新时间:2020-09-08 18:31:51
|
相似题推荐
单选题
|
容易
(0.94)
解题方法
【推荐1】某元素的原子结构示意图为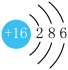 ,下列关于该元素的说法中,不正确的是
,下列关于该元素的说法中,不正确的是
 ,下列关于该元素的说法中,不正确的是
,下列关于该元素的说法中,不正确的是| A.元素符号是S | B.属于短周期元素 |
| C.氧化性比氯的强 | D.最高正化合价是+6价 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
【推荐2】同周期的A、B、D三种元素,其最高价氧化物对应水化物的酸性强弱顺序是HAO4>H2BO4>H3DO4,则下列判断错误的是
| A.气态氢化物稳定性HA>H2B>DH3 | B.原子半径A>B>D |
| C.非金属性A>B>D | D.阴离子还原性B2->A- |
您最近一年使用:0次
单选题
|
容易
(0.94)
【推荐1】在100mL 18 mol·L-1的浓硫酸中,加入过量的铜片,加热,被还原的硫酸的物质的量为
| A.1.8mol | B.大于1.8mol | C.0.9mol | D.小于0.9mol |
您最近一年使用:0次
【推荐2】工业废水中含有的重铬酸根离子(Cr2O )有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)作处理剂,反应的离子方程式为6Fe2++Cr2O
)有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)作处理剂,反应的离子方程式为6Fe2++Cr2O +14H+=6Fe3++2Cr3++7H2O,下列说法不正确的是
+14H+=6Fe3++2Cr3++7H2O,下列说法不正确的是
 )有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)作处理剂,反应的离子方程式为6Fe2++Cr2O
)有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)作处理剂,反应的离子方程式为6Fe2++Cr2O +14H+=6Fe3++2Cr3++7H2O,下列说法不正确的是
+14H+=6Fe3++2Cr3++7H2O,下列说法不正确的是| A.氧化剂与还原剂的物质的量之比为1∶6 |
| B.用绿矾作处理剂,不仅可去除毒性,还可净水 |
C.每处理1mol Cr2O 离子,转移3 mol e- 离子,转移3 mol e- |
| D.由反应可知还原性强弱顺序:Fe2+>Cr3+ |
您最近一年使用:0次
【推荐1】铅元素位于周期表ⅣA族,其氧化物铅丹(Pb3O4)可作防锈涂料,围绕铅丹的制备与性质有如下流程。下列有关说法错误的是
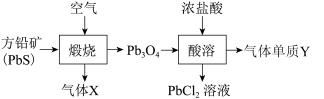

| A.Pb3O4可表示为2PbO·PbO2 |
| B.“煅烧”时PbS只作还原剂,Cl2的氧化性强于Pb3O4 |
| C.气体X既是氧化产物又是还原产物,气体Y为氧化产物 |
| D.“酸溶”时0.1 mol Pb3O4与足量的浓盐酸反应,生成0.1 mol Cl2 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐2】下列化学反应对应的离子方程式表示正确的是
| A.Fe(OH)2溶于稀硝酸Fe(OH)2+2H+=Fe2++2H2O |
B.NH4HCO3溶于过量的NaOH溶液中:HCO +OH-=CO +OH-=CO +H2O +H2O |
C.KAl(SO4)2中滴加Ba(OH)2使SO 恰好完全沉淀:2Al3++3SO 恰好完全沉淀:2Al3++3SO +3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ +3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ |
| D.FeBr2溶液与等物质的量的Cl2反应:2Fe2++2Br-+2Cl2=2Fe3++4Cl-+Br2 |
您最近一年使用:0次
单选题
|
容易
(0.94)
解题方法
【推荐1】新型净水剂高铁酸钠制备原理为:3NaClO+Fe2(SO4)3+10NaOH=2Na2FeO4+3NaCl+3Na2SO4+5H2O,其中氧化剂是
| A.NaClO | B.Fe2(SO4)3 | C.Na2FeO4 | D.NaCl |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐2】Na2FeO4是一种新型水处理剂,既可杀菌消毒,又可净水。其中Fe元素的化合价为
| A.+6 | B.+3 | C.+2 | D.+2、+3 |
您最近一年使用:0次


 Na2FeO4+Na2O(未配平),下列说法不正确的是( )
Na2FeO4+Na2O(未配平),下列说法不正确的是( ) )在水处理过程中涉及的变化有:氧化还原反应、蛋白质变性、盐类水解、胶体聚沉
)在水处理过程中涉及的变化有:氧化还原反应、蛋白质变性、盐类水解、胶体聚沉

