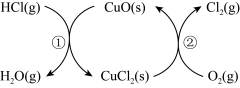
回答下列问题:
(1)已知下列反应的焓变:

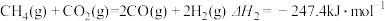
则 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为_________________________________ 。
(2)用甲烷制备合成气的反应:①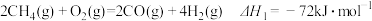 ;
;
② 。现有1mol由
。现有1mol由 与O2组成的混合气,且O2的体积分数为x,将此混合气与足量
与O2组成的混合气,且O2的体积分数为x,将此混合气与足量 充分反应。若
充分反应。若 时,反应①放出的能量为
时,反应①放出的能量为___________ kJ;若
__________ 时,反应①与②放出(或吸收)的总能量为0。
(1)已知下列反应的焓变:

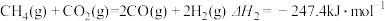
则
 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为(2)用甲烷制备合成气的反应:①
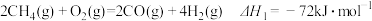 ;
;②
 。现有1mol由
。现有1mol由 与O2组成的混合气,且O2的体积分数为x,将此混合气与足量
与O2组成的混合气,且O2的体积分数为x,将此混合气与足量 充分反应。若
充分反应。若 时,反应①放出的能量为
时,反应①放出的能量为
更新时间:2020-09-13 16:42:16
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】燃煤能排放大量的CO、CO2、SO2,PM2.5(可入肺颗粒物)。污染跟冬季燃煤密切相关,SO2.CO、CO2也是对环境影响较大的气体,对它们的合理控制、利用是优化我们生存环境的有效途径。
(1)工业上可用CO2和H2反应合成甲醇。已知25°C、101 kPa下:
H2(g)+1/2O2(g)=H2O (g) △H1=-242kJ/mol
CH3OH+3/2O2(g) =CO2(g)+2H2O △H2=-676kJ/mol
写出CO2与H2反应生成CH3OH(g)与H2O (g)的热化学方程式_________________ 。
(2)工业上还可以通过下列反应制备甲醇:CO (g) +2H2 (g) CH3OH (g)。在一容积可变的密闭容器中充入l0molCO和20molH2,CO的平衡转化率随温度(T)、压强(P)的变化如图所示。
CH3OH (g)。在一容积可变的密闭容器中充入l0molCO和20molH2,CO的平衡转化率随温度(T)、压强(P)的变化如图所示。
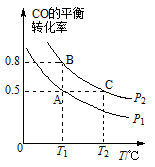
①下列说法不能判断该反应达到化学平衡状态的是____ (填字母)。
a. H2的消耗速率等于CH3OH的生成速率的2倍
b.H2的体积分数不再改变
c.体系中H2的转化率和CO的转化率相等
d.体系中气体的平均摩尔质量不再改变
②比较A、B两点压强大小PA____ PB(填“>”“<”或“=”)。
③若达到化学平衡状态A时,容器的体积为20 L。如果反应开始时仍充入10 mol CO和20molH2,则在平衡状态B时容器的体积V(B)=________ L。
(3)SO2在一定条件下可与氧气构成原电池。下图是利用该电池在铁表面镀铜的装置示意图: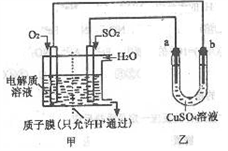
①该电池的负极反应:___________________ ;
②当甲中消耗2.24LO2(标准状况)时,乙中a极增重____ g。
(1)工业上可用CO2和H2反应合成甲醇。已知25°C、101 kPa下:
H2(g)+1/2O2(g)=H2O (g) △H1=-242kJ/mol
CH3OH+3/2O2(g) =CO2(g)+2H2O △H2=-676kJ/mol
写出CO2与H2反应生成CH3OH(g)与H2O (g)的热化学方程式
(2)工业上还可以通过下列反应制备甲醇:CO (g) +2H2 (g)
 CH3OH (g)。在一容积可变的密闭容器中充入l0molCO和20molH2,CO的平衡转化率随温度(T)、压强(P)的变化如图所示。
CH3OH (g)。在一容积可变的密闭容器中充入l0molCO和20molH2,CO的平衡转化率随温度(T)、压强(P)的变化如图所示。
①下列说法不能判断该反应达到化学平衡状态的是
a. H2的消耗速率等于CH3OH的生成速率的2倍
b.H2的体积分数不再改变
c.体系中H2的转化率和CO的转化率相等
d.体系中气体的平均摩尔质量不再改变
②比较A、B两点压强大小PA
③若达到化学平衡状态A时,容器的体积为20 L。如果反应开始时仍充入10 mol CO和20molH2,则在平衡状态B时容器的体积V(B)=
(3)SO2在一定条件下可与氧气构成原电池。下图是利用该电池在铁表面镀铜的装置示意图:

①该电池的负极反应:
②当甲中消耗2.24LO2(标准状况)时,乙中a极增重
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】氢元素的单质及其化合物与人们的日常生活及化工生产息息相关。回答下列问题:
(1)已知氢气与氧气反应生成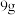 液态水时放出的热量为
液态水时放出的热量为 ,生成
,生成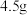 气态水时放出的热量为
气态水时放出的热量为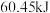 。
。
①写出表示 燃烧热的热化学方程式:
燃烧热的热化学方程式:__________ 。
②

__________  。
。
(2)利用甲烷将氮的氧化物转化为 和
和 ,有关反应的热化学方程式为:
,有关反应的热化学方程式为:
ⅰ.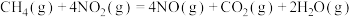
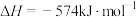 ;
;
ⅱ.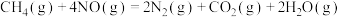
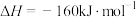
①反应ⅰ中生成物的总键能______ (填“>”“<”或“=”)反应物的总键能,利于该反应自发进行的条件为__________ (填“高温”“低温”或“任意条件”)。
② 直接将
直接将 还原为
还原为 并生成气态水的热化学方程式为
并生成气态水的热化学方程式为__________ 。
(3)在25℃、 下,
下,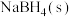 与
与 反应生成
反应生成 和
和 ,已知每消耗
,已知每消耗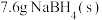 放热
放热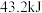 ,该反应的热化学方程式为
,该反应的热化学方程式为__________ 。
(1)已知氢气与氧气反应生成
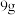 液态水时放出的热量为
液态水时放出的热量为 ,生成
,生成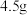 气态水时放出的热量为
气态水时放出的热量为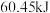 。
。①写出表示
 燃烧热的热化学方程式:
燃烧热的热化学方程式:②


 。
。(2)利用甲烷将氮的氧化物转化为
 和
和 ,有关反应的热化学方程式为:
,有关反应的热化学方程式为:ⅰ.
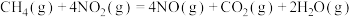
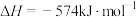 ;
;ⅱ.
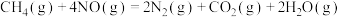
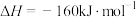
①反应ⅰ中生成物的总键能
②
 直接将
直接将 还原为
还原为 并生成气态水的热化学方程式为
并生成气态水的热化学方程式为(3)在25℃、
 下,
下,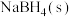 与
与 反应生成
反应生成 和
和 ,已知每消耗
,已知每消耗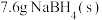 放热
放热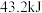 ,该反应的热化学方程式为
,该反应的热化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】绿色能源是未来能源发展的重要方向,氢能是重要的绿色能源,利用生物乙醇来制取氢气的部分反应过程如图所示。
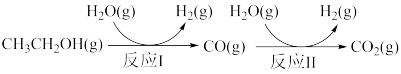
已知:总反应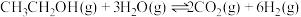
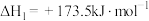 ;反应Ⅱ
;反应Ⅱ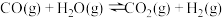
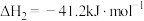 。
。
(1)则反应Ⅰ的热化学方程式为_______ 。
(2)研究氮和碳的化合物对工业生产和防治污染有重要意义,相关化学键的键能数据如表所示:
合成氨反应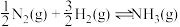 的活化能
的活化能 ,由此计算氨分解反应
,由此计算氨分解反应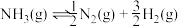 的活化能
的活化能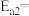
_______ 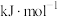 。
。
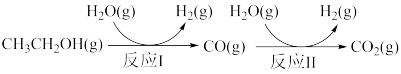
已知:总反应
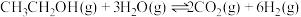
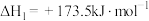 ;反应Ⅱ
;反应Ⅱ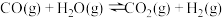
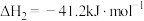 。
。(1)则反应Ⅰ的热化学方程式为
(2)研究氮和碳的化合物对工业生产和防治污染有重要意义,相关化学键的键能数据如表所示:
| 化学键 |  |  |  |
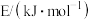 | 436 | 946 | 391 |
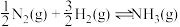 的活化能
的活化能 ,由此计算氨分解反应
,由此计算氨分解反应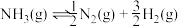 的活化能
的活化能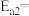
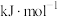 。
。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】已知:Ⅰ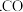 的燃烧热为
的燃烧热为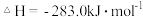
Ⅱ


Ⅲ

则
______ 。
 对于可逆反应
对于可逆反应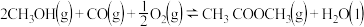 采取以下措施可以提高
采取以下措施可以提高 产率的是
产率的是______  填字母
填字母
A.降低体系的温度 压缩容器的体积
压缩容器的体积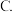 减少水量
减少水量  选用适当的催化剂
选用适当的催化剂
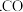 的燃烧热为
的燃烧热为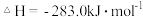
Ⅱ



Ⅲ


则

 对于可逆反应
对于可逆反应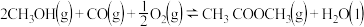 采取以下措施可以提高
采取以下措施可以提高 产率的是
产率的是 填字母
填字母
A.降低体系的温度
 压缩容器的体积
压缩容器的体积 减少水量
减少水量  选用适当的催化剂
选用适当的催化剂
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】研究大气中含硫化合物(主要是 和
和 )的转化具有重要意义。
)的转化具有重要意义。
(1)土壤中的微生物可将大气中的 经两步反应氧化成
经两步反应氧化成 ,两步反应的能量变化示意图如下:
,两步反应的能量变化示意图如下:
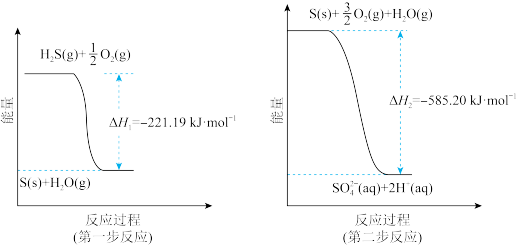
 全部氧化成
全部氧化成 的热化学方程式为
的热化学方程式为_______ 。
(2)二氧化硫-空气质子交换膜燃料电池可以利用大气所含 快速启动,其装置示意图如下:
快速启动,其装置示意图如下:
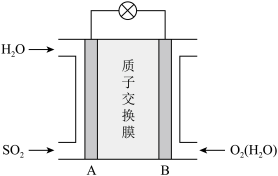
①质子的流动方向为_______ (填“从A到B”或“从B到A”)。
②负极的电极反应式为_______ 。
 和
和 )的转化具有重要意义。
)的转化具有重要意义。(1)土壤中的微生物可将大气中的
 经两步反应氧化成
经两步反应氧化成 ,两步反应的能量变化示意图如下:
,两步反应的能量变化示意图如下:
 全部氧化成
全部氧化成 的热化学方程式为
的热化学方程式为(2)二氧化硫-空气质子交换膜燃料电池可以利用大气所含
 快速启动,其装置示意图如下:
快速启动,其装置示意图如下:
①质子的流动方向为
②负极的电极反应式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】饮用水中的NO 主要来自于NH
主要来自于NH 。已知在微生物的作用下,NH
。已知在微生物的作用下,NH 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
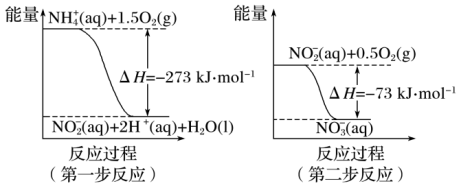
1 mol NH 全部被氧化成NO
全部被氧化成NO 的热化学方程式为
的热化学方程式为___________ 。
 主要来自于NH
主要来自于NH 。已知在微生物的作用下,NH
。已知在微生物的作用下,NH 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
1 mol NH
 全部被氧化成NO
全部被氧化成NO 的热化学方程式为
的热化学方程式为
您最近一年使用:0次
【推荐2】请认真观察图,然后回答问题:
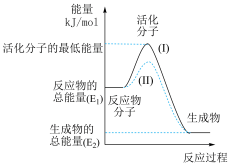
(1)图中所示反应是___ (填“吸热”或“放热”)反应
(2)图中所示反应的ΔH=___ (用含E1、E2的代数式表示)。
(3)下列4个反应中,符合示意图描述的反应的是____ (填代号)。
A.盐酸与NaOH反应 B.Na与H2O反应生成H2
C.铝热反应 D.灼热的炭与水蒸气反应生成CO和H2
(4)以甲烷为原料制取氢气是工业上常用的制氢方法。已知:
CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH=+206.2kJ/mol
CH4(g)+CO2(g)=2CO(g)+2H2(g) ΔH=+247.4kJ/mol
CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为:___ 。

(1)图中所示反应是
(2)图中所示反应的ΔH=
(3)下列4个反应中,符合示意图描述的反应的是
A.盐酸与NaOH反应 B.Na与H2O反应生成H2
C.铝热反应 D.灼热的炭与水蒸气反应生成CO和H2
(4)以甲烷为原料制取氢气是工业上常用的制氢方法。已知:
CH4(g)+H2O(g)=CO(g)+3H2(g) ΔH=+206.2kJ/mol
CH4(g)+CO2(g)=2CO(g)+2H2(g) ΔH=+247.4kJ/mol
CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】CO、CO2、CH3OH等一碳物质是重要的基础化工原料。回答下列问题:
(1)CH3OH(l)气化时吸收的热量为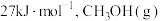 的燃烧热为
的燃烧热为 ,写出CH3OH(l)完全燃烧的热化学方程式:
,写出CH3OH(l)完全燃烧的热化学方程式:___________ 。
(2)甲醇水蒸气重整的热化学方程式为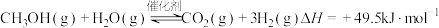 。已知不同温度下相关反应的
。已知不同温度下相关反应的 (用平衡分压代替平衡浓度计算得到的平衡常数)如下表所示。
(用平衡分压代替平衡浓度计算得到的平衡常数)如下表所示。
根据表计算398K时,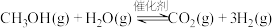 的
的
___________ 。利用该反应产生的H2可设计以H2为燃料、熔融Li2CO3与K2CO3混合物为电解质的高温型燃料电池,写出该电池负极的电极反应式:___________ 。
(3)利用CO、CH3OH等原料可合成草酸二甲酯( ),其加氢可转化为乙二醇(HOCH2CH2OH),制备草酸二甲酯的总反应为4CO+4CH3OH+O2
),其加氢可转化为乙二醇(HOCH2CH2OH),制备草酸二甲酯的总反应为4CO+4CH3OH+O2
 +2H2O
+2H2O
,其反应机理的一部分如图所示。
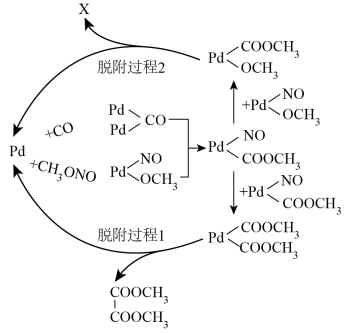
①由机理图可推知,化合物X的结构简式为___________ 。
②若CO中混有少量H2,H2在Pd表面易形成Pd—H中间体,结合机理图,推测因H2导致生成的有机副产物是___________ (任写一种)。
(4)草酸二甲酯催化加氢制乙二醇的反应体系中,发生的主要反应如下:
反应Ⅰ: ;
;
反应Ⅱ: ;
;
一定压强下,将(COOCH3)2、H2按一定比例、流速通过装有催化剂的反应管,测得(COOCH3)2的转化率及CH3OOCCH2OH、HOCH2CH2OH的选择性{ }与温度的关系如图所示。
}与温度的关系如图所示。
①表示HOCH2CH2OH的选择性随温度变化的曲线是___________ ,理由为___________ 。
②194℃时,其他条件一定,若加快气体的流速,则(COOCH3)2的转化率降低,其原因是___________ 。

(1)CH3OH(l)气化时吸收的热量为
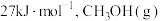 的燃烧热为
的燃烧热为 ,写出CH3OH(l)完全燃烧的热化学方程式:
,写出CH3OH(l)完全燃烧的热化学方程式:(2)甲醇水蒸气重整的热化学方程式为
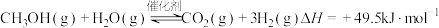 。已知不同温度下相关反应的
。已知不同温度下相关反应的 (用平衡分压代替平衡浓度计算得到的平衡常数)如下表所示。
(用平衡分压代替平衡浓度计算得到的平衡常数)如下表所示。| 相关反应 | 398K | 498K | 598K | 698K |
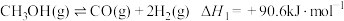 | 5.0 | 185.8 | 9939.5 | 1.8×105 |
 | 157.5 | 137.5 | 28.14 | 9.339 |
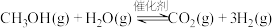 的
的
(3)利用CO、CH3OH等原料可合成草酸二甲酯(
 ),其加氢可转化为乙二醇(HOCH2CH2OH),制备草酸二甲酯的总反应为4CO+4CH3OH+O2
),其加氢可转化为乙二醇(HOCH2CH2OH),制备草酸二甲酯的总反应为4CO+4CH3OH+O2
 +2H2O
+2H2O ,其反应机理的一部分如图所示。

①由机理图可推知,化合物X的结构简式为
②若CO中混有少量H2,H2在Pd表面易形成Pd—H中间体,结合机理图,推测因H2导致生成的有机副产物是
(4)草酸二甲酯催化加氢制乙二醇的反应体系中,发生的主要反应如下:
反应Ⅰ:
 ;
;反应Ⅱ:
 ;
;一定压强下,将(COOCH3)2、H2按一定比例、流速通过装有催化剂的反应管,测得(COOCH3)2的转化率及CH3OOCCH2OH、HOCH2CH2OH的选择性{
 }与温度的关系如图所示。
}与温度的关系如图所示。①表示HOCH2CH2OH的选择性随温度变化的曲线是
②194℃时,其他条件一定,若加快气体的流速,则(COOCH3)2的转化率降低,其原因是

您最近一年使用:0次
【推荐1】(1)电解池是将_______ 的装置;
(2)电解精炼铜的阳极为_______ ;铁钥匙上镀铜,镀件为:_______ 极;
(3)100℃时,KW=1×10-12,溶液显中性时,c(H+)=_______ ;pH=_______ ;
(4)钢铁表面容易发生电化学腐蚀,发生腐蚀时,铁是_______ 极,电极方程式为_______ ,杂质碳为_______ 极,发生_______ (氧化或还原)反应。
(5)为保护地下钢管不受腐蚀,可使它与直流电源的_______ 极相连。
(6)环戊二烯( )是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:
)是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:
已知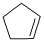 (g)=
(g)=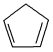 (g)+H2(g)ΔH1=+100.3kJ·mol-1 ①
(g)+H2(g)ΔH1=+100.3kJ·mol-1 ①
H2(g)+I2(g)=2HI(g)ΔH2=-11.0kJ·mol-1 ②
对于反应: (g)+I2(g)=
(g)+I2(g)= (g)+2HI(g) ③的ΔH3=
(g)+2HI(g) ③的ΔH3=_______ kJ·mol-1
(2)电解精炼铜的阳极为
(3)100℃时,KW=1×10-12,溶液显中性时,c(H+)=
(4)钢铁表面容易发生电化学腐蚀,发生腐蚀时,铁是
(5)为保护地下钢管不受腐蚀,可使它与直流电源的
(6)环戊二烯(
 )是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:
)是重要的有机化工原料,广泛用于农药、橡胶、塑料等生产。回答下列问题:已知
 (g)=
(g)= (g)+H2(g)ΔH1=+100.3kJ·mol-1 ①
(g)+H2(g)ΔH1=+100.3kJ·mol-1 ①H2(g)+I2(g)=2HI(g)ΔH2=-11.0kJ·mol-1 ②
对于反应:
 (g)+I2(g)=
(g)+I2(g)= (g)+2HI(g) ③的ΔH3=
(g)+2HI(g) ③的ΔH3=
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】2SO2+O2 2SO3△H=-akJmol-1,反应过程的能量变化如图所示。已知1molSO2完全转化为1molSO3放热99kJ。请回答:
2SO3△H=-akJmol-1,反应过程的能量变化如图所示。已知1molSO2完全转化为1molSO3放热99kJ。请回答:
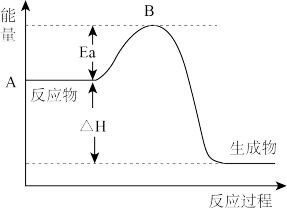
(1)a=___ 。升高温度,该反应中SO2的转化率变___ (填“大”或“小”)。
(2)Ea的大小对该反应的△H___ (填“有”或“无”)影响。该反应常用V2O5作催化剂,加入V2O5会使图中B点__ (填“升高”、“降低”或“不变”)。
(3)已知在一定条件下SO3(g)也可分解生成SO2(g)和O2(g),试写出该反应的热化学方程式:___ 。
 2SO3△H=-akJmol-1,反应过程的能量变化如图所示。已知1molSO2完全转化为1molSO3放热99kJ。请回答:
2SO3△H=-akJmol-1,反应过程的能量变化如图所示。已知1molSO2完全转化为1molSO3放热99kJ。请回答:
(1)a=
(2)Ea的大小对该反应的△H
(3)已知在一定条件下SO3(g)也可分解生成SO2(g)和O2(g),试写出该反应的热化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】燃煤能排放大量的CO、CO2、SO2,PM2.5(可入肺颗粒物)。污染跟冬季燃煤密切相关,SO2.CO、CO2也是对环境影响较大的气体,对它们的合理控制、利用是优化我们生存环境的有效途径。
(1)工业上可用CO2和H2反应合成甲醇。已知25°C、101 kPa下:
H2(g)+1/2O2(g)=H2O (g) △H1=-242kJ/mol
CH3OH+3/2O2(g) =CO2(g)+2H2O △H2=-676kJ/mol
写出CO2与H2反应生成CH3OH(g)与H2O (g)的热化学方程式_________________ 。
(2)工业上还可以通过下列反应制备甲醇:CO (g) +2H2 (g) CH3OH (g)。在一容积可变的密闭容器中充入l0molCO和20molH2,CO的平衡转化率随温度(T)、压强(P)的变化如图所示。
CH3OH (g)。在一容积可变的密闭容器中充入l0molCO和20molH2,CO的平衡转化率随温度(T)、压强(P)的变化如图所示。

①下列说法不能判断该反应达到化学平衡状态的是____ (填字母)。
a. H2的消耗速率等于CH3OH的生成速率的2倍
b.H2的体积分数不再改变
c.体系中H2的转化率和CO的转化率相等
d.体系中气体的平均摩尔质量不再改变
②比较A、B两点压强大小PA____ PB(填“>”“<”或“=”)。
③若达到化学平衡状态A时,容器的体积为20 L。如果反应开始时仍充入10 mol CO和20molH2,则在平衡状态B时容器的体积V(B)=________ L。
(3)SO2在一定条件下可与氧气构成原电池。下图是利用该电池在铁表面镀铜的装置示意图:
①该电池的负极反应:___________________ ;
②当甲中消耗2.24LO2(标准状况)时,乙中a极增重____ g。
(1)工业上可用CO2和H2反应合成甲醇。已知25°C、101 kPa下:
H2(g)+1/2O2(g)=H2O (g) △H1=-242kJ/mol
CH3OH+3/2O2(g) =CO2(g)+2H2O △H2=-676kJ/mol
写出CO2与H2反应生成CH3OH(g)与H2O (g)的热化学方程式
(2)工业上还可以通过下列反应制备甲醇:CO (g) +2H2 (g)
 CH3OH (g)。在一容积可变的密闭容器中充入l0molCO和20molH2,CO的平衡转化率随温度(T)、压强(P)的变化如图所示。
CH3OH (g)。在一容积可变的密闭容器中充入l0molCO和20molH2,CO的平衡转化率随温度(T)、压强(P)的变化如图所示。
①下列说法不能判断该反应达到化学平衡状态的是
a. H2的消耗速率等于CH3OH的生成速率的2倍
b.H2的体积分数不再改变
c.体系中H2的转化率和CO的转化率相等
d.体系中气体的平均摩尔质量不再改变
②比较A、B两点压强大小PA
③若达到化学平衡状态A时,容器的体积为20 L。如果反应开始时仍充入10 mol CO和20molH2,则在平衡状态B时容器的体积V(B)=
(3)SO2在一定条件下可与氧气构成原电池。下图是利用该电池在铁表面镀铜的装置示意图:

①该电池的负极反应:
②当甲中消耗2.24LO2(标准状况)时,乙中a极增重
您最近一年使用:0次