已知:Ⅰ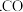 的燃烧热为
的燃烧热为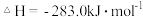
Ⅱ


Ⅲ

则
______ 。
 对于可逆反应
对于可逆反应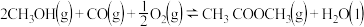 采取以下措施可以提高
采取以下措施可以提高 产率的是
产率的是______  填字母
填字母
A.降低体系的温度 压缩容器的体积
压缩容器的体积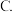 减少水量
减少水量  选用适当的催化剂
选用适当的催化剂
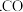 的燃烧热为
的燃烧热为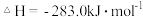
Ⅱ



Ⅲ


则

 对于可逆反应
对于可逆反应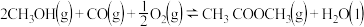 采取以下措施可以提高
采取以下措施可以提高 产率的是
产率的是 填字母
填字母
A.降低体系的温度
 压缩容器的体积
压缩容器的体积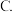 减少水量
减少水量  选用适当的催化剂
选用适当的催化剂
更新时间:2020-01-29 15:14:00
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】(1)1mol 乙烷在氧气中完全燃烧生成二氧化碳和液态水,放出热量 1558.3kJ。写出 乙烷燃烧的热化学方程式:__________________ 。
(2)已知:2SO2(g)+O2(g)=2SO3(g) ΔH=-196.6 kJ·mol-1
2NO(g)+O2(g)=2NO2(g) ΔH=-113.0 kJ·mol-1
则反应 NO2(g)+SO2(g)=SO3(g)+NO(g)的 ΔH=_______________ kJ·mol-1。
(3)向盛有10mL0.01 mol/L 的硫氰化钾溶液的小烧杯中,加入10mol0.01mol/L的FeCl3溶液,混合液立即___ 。写出上述反应的离子方程式____________________ 。
(2)已知:2SO2(g)+O2(g)=2SO3(g) ΔH=-196.6 kJ·mol-1
2NO(g)+O2(g)=2NO2(g) ΔH=-113.0 kJ·mol-1
则反应 NO2(g)+SO2(g)=SO3(g)+NO(g)的 ΔH=
(3)向盛有10mL0.01 mol/L 的硫氰化钾溶液的小烧杯中,加入10mol0.01mol/L的FeCl3溶液,混合液立即
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】已知在常温常压下:
①2CH3OH(l)+2O2(g)═2CO(g)+4H2O(g) △H=﹣akJ•mol﹣1
②2CO(g)+O2(g)═2CO2(g) △H=﹣bkJ•mol﹣1
③H2O(g)═H2O(l) △H=﹣ckJ•mol﹣1
则表示CH3OH(l)燃烧热的热化学方程式为_______ 。
①2CH3OH(l)+2O2(g)═2CO(g)+4H2O(g) △H=﹣akJ•mol﹣1
②2CO(g)+O2(g)═2CO2(g) △H=﹣bkJ•mol﹣1
③H2O(g)═H2O(l) △H=﹣ckJ•mol﹣1
则表示CH3OH(l)燃烧热的热化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】按要求完成下列问题。
(1)工业上用CO生产燃料甲醇。一定条件下发生反应:CO(g)+2H2(g) CH3OH(g)。如图表示反应中能量的变化;在图中,曲线
CH3OH(g)。如图表示反应中能量的变化;在图中,曲线____ (填“a”或“b”)表示使用了催化剂;该反应属于____ 反应。(填“吸热”或“放热”)。

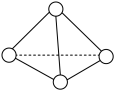
(2)科学家已获得了极具理论研究意义的N4气体分子,其结构为正四面体(如图所示),与白磷分子相似,化学性质比较活泼。已知断裂1molN-N键吸收193kJ热量,断裂1molN≡N键吸收941kJ热量,断裂1molN-H键吸收391kJ热量,断裂1molH-H键吸收436kJ热量,则:写出N4与H2反应生成NH3的热化学方程式:____ 。
(3)试运用盖斯定律回答下列问题:(已知Q1、Q2、Q3为正值)
已知:H2O(g)=H2O(l) ΔH1=-Q1kJ/mol
C2H5OH(g)=C2H5OH(l) ΔH2=-Q2kJ/mol
C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g) ΔH3=-Q3kJ/mol
则表示液态无水酒精燃烧热的热化学方程式为____ 。
(1)工业上用CO生产燃料甲醇。一定条件下发生反应:CO(g)+2H2(g)
 CH3OH(g)。如图表示反应中能量的变化;在图中,曲线
CH3OH(g)。如图表示反应中能量的变化;在图中,曲线
(2)科学家已获得了极具理论研究意义的N4气体分子,其结构为正四面体(如图所示),与白磷分子相似,化学性质比较活泼。已知断裂1molN-N键吸收193kJ热量,断裂1molN≡N键吸收941kJ热量,断裂1molN-H键吸收391kJ热量,断裂1molH-H键吸收436kJ热量,则:写出N4与H2反应生成NH3的热化学方程式:

(3)试运用盖斯定律回答下列问题:(已知Q1、Q2、Q3为正值)
已知:H2O(g)=H2O(l) ΔH1=-Q1kJ/mol
C2H5OH(g)=C2H5OH(l) ΔH2=-Q2kJ/mol
C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g) ΔH3=-Q3kJ/mol
则表示液态无水酒精燃烧热的热化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】3H2(g) + 3CO(g) CH3OCH3(g) + CO2(g) ΔH>0一定条件下的密闭容器中,该反应达到平衡后,若要提高CO的转化率,可以采取的措施是
CH3OCH3(g) + CO2(g) ΔH>0一定条件下的密闭容器中,该反应达到平衡后,若要提高CO的转化率,可以采取的措施是___________ (填字母代号)。
a.高温高压 b.加入催化剂 c.减少CO2的浓度 d.增加CO的浓度 e.分离出二甲醚
 CH3OCH3(g) + CO2(g) ΔH>0一定条件下的密闭容器中,该反应达到平衡后,若要提高CO的转化率,可以采取的措施是
CH3OCH3(g) + CO2(g) ΔH>0一定条件下的密闭容器中,该反应达到平衡后,若要提高CO的转化率,可以采取的措施是a.高温高压 b.加入催化剂 c.减少CO2的浓度 d.增加CO的浓度 e.分离出二甲醚
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】科学家研究高效催化剂对汽车尾气进行无害化处理,其反应原理为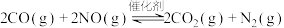
 。回答下列问题:
。回答下列问题:
(1)某温度下,在密闭容器中该反应达到化学平衡后,只改变一种条件对该反应的正、逆反应速率的影响如图甲所示。

①加催化剂对反应速率影响的图像是______ (填字母,下同)。
②适当升高温度对反应速率影响的图像是A,该反应的正反应是__________ 反应(填“吸热”或“放热”)。
③图像D改变的条件是__________ (任写一条)。
(2)在 密闭容器中充入CO和NO共
密闭容器中充入CO和NO共 ,发生反应
,发生反应
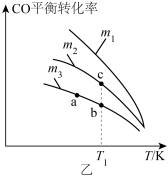
 ,CO的平衡转化率与温度、起始投料比m的关系如图乙所示[起始投料比
,CO的平衡转化率与温度、起始投料比m的关系如图乙所示[起始投料比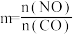 ]。
]。
①该反应的化学平衡常数表达式是__________ 。
②图中a、b、c三点对应的平衡常数 、
、 、
、 相对大小关系是
相对大小关系是__________ , 、
、 、
、 相对大小关系是
相对大小关系是__________ 。
③若 ,温度为
,温度为 ,反应达到平衡所用的时间为
,反应达到平衡所用的时间为 ,CO的平衡转化率为40%。达平衡过程中平均反应速率
,CO的平衡转化率为40%。达平衡过程中平均反应速率
__________  ,平衡时混合气体总物质的量=
,平衡时混合气体总物质的量=__________  ;若
;若 时,该容器中此四种物质均为
时,该容器中此四种物质均为 ,则此时v(正)
,则此时v(正)______ (填“>”“<”或“=”)v(逆)。
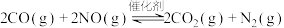
 。回答下列问题:
。回答下列问题:(1)某温度下,在密闭容器中该反应达到化学平衡后,只改变一种条件对该反应的正、逆反应速率的影响如图甲所示。


①加催化剂对反应速率影响的图像是
②适当升高温度对反应速率影响的图像是A,该反应的正反应是
③图像D改变的条件是
(2)在
 密闭容器中充入CO和NO共
密闭容器中充入CO和NO共 ,发生反应
,发生反应
 ,CO的平衡转化率与温度、起始投料比m的关系如图乙所示[起始投料比
,CO的平衡转化率与温度、起始投料比m的关系如图乙所示[起始投料比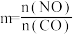 ]。
]。①该反应的化学平衡常数表达式是
②图中a、b、c三点对应的平衡常数
 、
、 、
、 相对大小关系是
相对大小关系是 、
、 、
、 相对大小关系是
相对大小关系是③若
 ,温度为
,温度为 ,反应达到平衡所用的时间为
,反应达到平衡所用的时间为 ,CO的平衡转化率为40%。达平衡过程中平均反应速率
,CO的平衡转化率为40%。达平衡过程中平均反应速率
 ,平衡时混合气体总物质的量=
,平衡时混合气体总物质的量= ;若
;若 时,该容器中此四种物质均为
时,该容器中此四种物质均为 ,则此时v(正)
,则此时v(正)
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】向黄色的 溶液中加入无色的
溶液中加入无色的 溶液,溶液变成红色。该反应在有的教材中用方程式
溶液,溶液变成红色。该反应在有的教材中用方程式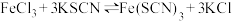 表示。
表示。
(1)向上述红色溶液中继续加入浓 溶液,溶液红色加深,这是由于
溶液,溶液红色加深,这是由于_______________ (填字母).
A.与 配合的
配合的 数目增多
数目增多
B.红色离子的数目增多
C.红色离子的浓度增加
(2)向上述红色溶液中加入 溶液振荡,只观察到红色溶液迅速褪成无色,表示该反应的离子方程式为
溶液振荡,只观察到红色溶液迅速褪成无色,表示该反应的离子方程式为_______________ ;能使该反应发生的可能原因是_______________ 。
 溶液中加入无色的
溶液中加入无色的 溶液,溶液变成红色。该反应在有的教材中用方程式
溶液,溶液变成红色。该反应在有的教材中用方程式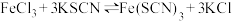 表示。
表示。(1)向上述红色溶液中继续加入浓
 溶液,溶液红色加深,这是由于
溶液,溶液红色加深,这是由于A.与
 配合的
配合的 数目增多
数目增多B.红色离子的数目增多
C.红色离子的浓度增加
(2)向上述红色溶液中加入
 溶液振荡,只观察到红色溶液迅速褪成无色,表示该反应的离子方程式为
溶液振荡,只观察到红色溶液迅速褪成无色,表示该反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】硫酸是重要的化工材料,二氧化硫与氧气反应生成三氧化硫是工业制硫酸的重要反应之一。
(1)将0.050molSO2(g)和0.030molO2(g)放入容积为1L的密闭容器中,反应2SO2(g)+O2(g) 2SO3(g)在一定条件下经20分钟达到平衡,测得c(SO3)=0.040mol/L。
2SO3(g)在一定条件下经20分钟达到平衡,测得c(SO3)=0.040mol/L。
①从反应开始到达到平衡,用SO2表示的平均反应速率为________________
②从平衡角度分析采用过量O2的目的是____________ ;
③该反应的平衡常数表达式为K=___________ 。
④已知:K(300℃)>K(350℃),该反应是________ (选填“吸”或“放”)热反应。若反应温度升高,SO2的转化率将_______ (填“增大”、“减小”或“不变”)。
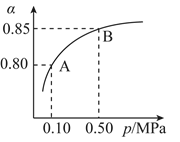
(2)某温度下,SO2的平衡转化率(α)与体系总压强(P)的关系如图所示。平衡状态由A变到B时,平衡常数K(A)_______ K(B)(填“>”、“<”或“=”,下同)。
(1)将0.050molSO2(g)和0.030molO2(g)放入容积为1L的密闭容器中,反应2SO2(g)+O2(g)
 2SO3(g)在一定条件下经20分钟达到平衡,测得c(SO3)=0.040mol/L。
2SO3(g)在一定条件下经20分钟达到平衡,测得c(SO3)=0.040mol/L。①从反应开始到达到平衡,用SO2表示的平均反应速率为
②从平衡角度分析采用过量O2的目的是
③该反应的平衡常数表达式为K=
④已知:K(300℃)>K(350℃),该反应是

(2)某温度下,SO2的平衡转化率(α)与体系总压强(P)的关系如图所示。平衡状态由A变到B时,平衡常数K(A)
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
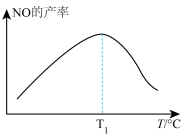
【推荐2】向一体积恒定盛有催化剂的密闭容器中充入一定量的NH3和O2,测得一定时间内NO的产率与温度(T)的关系如图所示,该反应的ΔH___________ 0(填“>”或“<”),温度低于T1℃时,NO的产率___________ (填“是”或“不是”)对应温度下的平衡产率,理由为___________ 。

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】I.恒温下,将amolN2与bmolH2的混合气体通入一个恒容密闭容器中,发生如下反应:N2(g)+3H2(g) 2NH3(g)
2NH3(g)
(1)反应进行到某时刻t时,n(N2)=13mol,n(NH3)=6mol,则a=___________ 。
(2)反应达平衡时,混合气体的体积为716.8L(标准状况),其中NH3的含量(体积分数)为25%,平衡时NH3的物质的量为___________ mol。
(3)原混合气体与平衡时混合气体的总物质的量之比,n(始)∶n(平) =________ (最简整数比)
(4)达到平衡时,N2和H2的转化率之比α(N2): α(H2)=___________ (写出最简整数比)。
II.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表格。
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表格。
(5)该反应的化学平衡常数表达式为K=___________ 。
(6)该反应正反应为___________ 反应(选填吸热、放热)。
 2NH3(g)
2NH3(g)(1)反应进行到某时刻t时,n(N2)=13mol,n(NH3)=6mol,则a=
(2)反应达平衡时,混合气体的体积为716.8L(标准状况),其中NH3的含量(体积分数)为25%,平衡时NH3的物质的量为
(3)原混合气体与平衡时混合气体的总物质的量之比,n(始)∶n(平) =
(4)达到平衡时,N2和H2的转化率之比α(N2): α(H2)=
II.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)
 CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表格。
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表格。| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(6)该反应正反应为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】请分析讨论在恒温下,压缩容器的体积,增大压强,下列三个反应浓度商Q的变化和平衡移动的方向,填写下表。
| 化学反应 | Q值变化 | Q与K关系 | 平衡移动方向 |
C(s)+H2O(g) CO(g)+H2(g) CO(g)+H2(g) | |||
N2(g)+3H2(g) 2NH3(g) 2NH3(g) | |||
N2(g)+O2(g) 2NO(g) 2NO(g) |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】现有反应

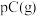 ,ΔH<0,达到平衡后,减小压强,混合物体系中C的质量分数减小,则:
,ΔH<0,达到平衡后,减小压强,混合物体系中C的质量分数减小,则:
(1)该反应
_______ p(填“>”“=”或“<”)。
(2)该反应在一定条件下能否自发进行_______ (填“能”或“不能”),说明理由_______ 。
(3)若B是有色物质,A、C均无色,则加入C(容器容积不变)时混合物的颜色_______ (填“变深”、“变浅”或“不变”);若容器容积不变,充入氖气时,容器内压强增大,这时化学平衡_______ 移动(填“正向”、“逆向”或“不”)。


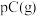 ,ΔH<0,达到平衡后,减小压强,混合物体系中C的质量分数减小,则:
,ΔH<0,达到平衡后,减小压强,混合物体系中C的质量分数减小,则:(1)该反应

(2)该反应在一定条件下能否自发进行
(3)若B是有色物质,A、C均无色,则加入C(容器容积不变)时混合物的颜色
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】现代制备乙烯常用乙烷氧化裂解法,主反应为C2H6(g)+ O2(g)
O2(g) C2H4(g)+H2O(g) ΔH=−110kJ·mol-1,反应时还会生成CH4、CO、CO2等副产物(副反应均为放热反应),如图所示为温度对乙烷氧化裂解反应的影响。[乙烯选择性=
C2H4(g)+H2O(g) ΔH=−110kJ·mol-1,反应时还会生成CH4、CO、CO2等副产物(副反应均为放热反应),如图所示为温度对乙烷氧化裂解反应的影响。[乙烯选择性= ×100%;乙烯收率=乙烷转化率×乙烯选择性]
×100%;乙烯收率=乙烷转化率×乙烯选择性]________ ,反应的最佳温度为_________ 。
A.650℃ B.700℃ C.775℃ D.850℃
(2)工业上,保持体系总压强恒定在100kPa下进行该反应,且通常在乙烷和氧气的混合气体中掺入惰性气体(惰性气体的体积分数为70%),掺入惰性气体的目的是___________ 。
 O2(g)
O2(g) C2H4(g)+H2O(g) ΔH=−110kJ·mol-1,反应时还会生成CH4、CO、CO2等副产物(副反应均为放热反应),如图所示为温度对乙烷氧化裂解反应的影响。[乙烯选择性=
C2H4(g)+H2O(g) ΔH=−110kJ·mol-1,反应时还会生成CH4、CO、CO2等副产物(副反应均为放热反应),如图所示为温度对乙烷氧化裂解反应的影响。[乙烯选择性= ×100%;乙烯收率=乙烷转化率×乙烯选择性]
×100%;乙烯收率=乙烷转化率×乙烯选择性]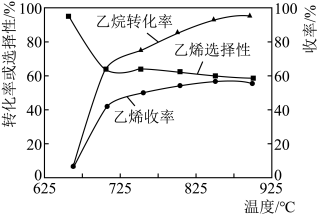
A.650℃ B.700℃ C.775℃ D.850℃
(2)工业上,保持体系总压强恒定在100kPa下进行该反应,且通常在乙烷和氧气的混合气体中掺入惰性气体(惰性气体的体积分数为70%),掺入惰性气体的目的是
您最近一年使用:0次



